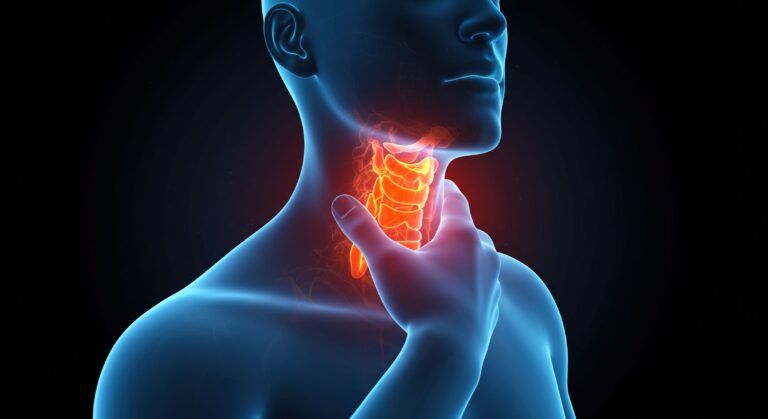
Uporczywa chrypka, ból gardła utrzymujący się tygodniami, powiększone węzły chłonne na szyi – to objawy, które łatwo przypisać przewlekłej infekcji. Tymczasem mogą one sygnalizować raka gardła – nowotwór złośliwy rozwijający się w nosogardle, części ustnej lub krtaniowej gardła. W artykule wyjaśnimy, jak rozpoznać pierwsze symptomy nowotworu, kto jest szczególnie narażony i jakie badania pozwalają postawić pewną diagnozę. Dowiesz się też, jak współczesna medycyna łączy chirurgię, radioterapię i chemioterapię, aby skutecznie walczyć z tą jednostką chorobową. Jeśli chcesz świadomie dbać o swoje zdrowie, czytaj dalej – szybka reakcja może uratować życie.
Spis treści:
- Czym jest rak gardła?
- Rodzaje raka gardła
- Przyczyny raka gardła
- Jak objawia się rak gardła?
- Leczenie raka gardła
- Rak gardła – często zadawane pytania
- Rak gardła – podsumowanie
Czym jest rak gardła?
Rak gardła to nowotwór złośliwy, który rozwija się z komórek nabłonka wyścielającego gardło. Dochodzi do niekontrolowanego podziału tych komórek, co prowadzi do powstania guza. W ponad 90% przypadków mamy do czynienia z rakiem płaskonabłonkowym (kolczystokomórkowym), czyli nowotworem wywodzącym się z komórek nabłonka wielowarstwowego płaskiego. Pozostałe przypadki to rzadziej występujące typy, takie jak gruczolakoraki, czerniaki śluzówek czy nowotwory gruczołów ślinowych.
Gardło można podzielić anatomicznie na trzy części: górną (nosogardło), środkową (część ustna, okolica migdałków) oraz dolną (część krtaniowa). Każda z tych części różni się funkcją, budową oraz podatnością na konkretne typy nowotworów.
Rodzaje raka gardła
Trzy lokalizacje choroby różnią się objawami i rokowaniem:
- Nosogardle (część górna) – obejmuje tylną ścianę jamy nosowej i ujścia trąbek słuchowych. Nowotwory tej lokalizacji często mają związek z wirusem Epstein-Barr (EBV). Objawy mogą obejmować krwawienia z nosa, niedrożność nosa, pogorszenie słuchu i wysięk do ucha środkowego.
- Gardło środkowe (ustna część) – obejmuje tylną ścianę jamy ustnej, migdałki podniebienne i nasadę języka. Coraz częściej nowotwory tej okolicy są związane z wirusem HPV 16. Bywa, że jedynym pierwszym objawem choroby jest bezbolesne powiększenie węzła chłonnego na szyi.
- Gardło dolne (część krtaniowa) – długo bezobjawowe; w chwili rozpoznania często zaawansowane, powoduje dysfagię (utrudnione połykanie pokarmów lub płynów) i chrypkę.
| Zapamiętaj: położenie guza wpływa na wczesne symptomy, sposób leczenia oraz rokowanie. |
Przyczyny raka gardła
Do zachorowania na raka gardła przyczyniają się głównie czynniki środowiskowe i styl życia:
- Palenie tytoniu – ryzyko rośnie nawet 10‑krotnie.
- Nadużywanie alkoholu – działa synergistycznie z dymem papierosowym.
- Długotrwałe zakażenie onkogennymi typami HPV (16, 18).
- Ekspozycja zawodowa na pyły drewna, nikiel, azbest czy opary kwasu siarkowego.
- Wiek > 50 lat i płeć męska.
Zminimalizowanie tych czynników znacząco obniża ryzyko zachorowania.
>> Przeczytaj również: Wirus HPV (Human papillomavirus) – co trzeba wiedzieć?
Rak gardła a HPV
Wariant HPV‑zależny dotyczy zwykle młodszych, niepalących pacjentów, u których nie występują inne klasyczne czynniki ryzyka, takie jak palenie czy alkohol. Nowotwory te najczęściej lokalizują się w gardle środkowym (okolice migdałków i nasady języka). Charakteryzują się dobrą odpowiedzią na leczenie oraz znacznie wyższym odsetkiem przeżyć 5‑letnich, sięgającym ponad 80%.

Jak objawia się rak gardła?
Pierwsze sygnały są niespecyficzne, dlatego łatwo je przeoczyć. Zwróć uwagę szczególnie na:
- ból lub drapanie w gardle trwające > 3 tygodnie,
- przewlekłą chrypkę lub zmianę barwy głosu,
- trudności czy ból przy połykaniu,
- jednostronny ból ucha bez zapalenia,
- powiększone, twarde węzły chłonne szyi,
- niezamierzoną utratę masy ciała.
Utrzymywanie się tych dolegliwości przez ponad dwa tygodnie jest wskazaniem do pilnej konsultacji laryngologicznej.

>> Zobacz również: Powiększone węzły chłonne (limfadenopatia) – przyczyny, diagnostyka
Leczenie raka gardła
Zakres terapii zależy od lokalizacji guza, stopnia zaawansowania (TNM8), wyniku biopsji oraz ogólnego stanu chorego.
- Stadium I–II – chirurgia endoskopowa lub laserowa albo radioterapia wysokiej precyzji (IMRT).
- Stadium III–IVa – leczenie skojarzone: operacja + radioterapia ± chemioterapia (cisplatyna) lub radykalna chemioradioterapia.
- Stadium IVb–IVc / nawroty – leczenie paliatywne: chemioterapia, immunoterapia (nivolumab, pembrolizumab) lub terapia celowana (cetuximab).
Każdy przypadek omawia zespół interdyscyplinarny, aby dobrać strategię maksymalizującą szanse na wyleczenie i zachowanie funkcji mowy oraz połykania.
Rak gardła – często zadawane pytania
Ile żyje się z rakiem gardła?
W Polsce 5-letnie przeżycie względne dla raka gardła wynosi od 20% (dla nowotworów części krtaniowej) do ponad 60% w lokalizacjach o lepszym rokowaniu. Wczesne rozpoznanie znacząco zwiększa szanse na skuteczne leczenie.
Z czym można pomylić raka gardła?
Najczęściej z przewlekłym zapaleniem gardła, anginą, refluksem krtaniowo‑gardłowym lub powiększonymi migdałkami.
Czy rak gardła jest wyleczalny?
Tak, zwłaszcza w stadium I–II oraz w przypadkach HPV‑dodatnich.
Jaki jest marker nowotworowy gardła?
Nie istnieje specyficzny marker wykrywany w badaniu krwi, który jednoznacznie wskazywałby na raka gardła. W raku gardła środkowego oznacza się ekspresję białka p16 jako pośredni dowód zakażenia HPV.
Jak diagnozować raka gardła?
Podstawą jest laryngoskopia z biopsją, a następnie obrazowanie (CT, MRI, PET/CT) w celu określenia stopnia zaawansowania.
Rak gardła – podsumowanie
- Rak gardła rozwija się najczęściej z nabłonka płaskiego, pokrywającego wewnętrzne ściany gardła.
- Główne czynniki ryzyka to palenie, alkohol oraz zakażenie HPV.
- Objawy są niespecyficzne i łatwe do przeoczenia, dlatego przedłużające się dolegliwości powinny skłonić do wizyty u laryngologa.
- Skuteczne leczenie obejmuje chirurgię, radioterapię i chemioterapię, o wyborze decyduje zespół specjalistów.
- Wczesne wykrycie znacząco zwiększa szanse na całkowite wyleczenie.
Bibliografia
- Komorowski A. Nowotwory złośliwe gardła. mp.pl.
- Poon C.S., Stenson K.M. Overview of the diagnosis and staging of head and neck cancer. UpToDate, 2025.
- Brockstein B.E. i wsp. Overview of treatment for head and neck cancer. UpToDate, 2025.
- Krajowy Rejestr Nowotworów, 2022