Liszaj twardzinowy to schorzenie dermatologiczne, które wiąże się z występowaniem objawów klinicznych istotnie oddziałujących na codzienne funkcjonowanie pacjenta. Jakie są przyczyny liszaja twardzinowego? Jak objawia się ta jednostka chorobowa? Dowiedz się, z jakimi zagrożeniami dla zdrowia może wiązać się liszaj twardzinowy i co robić w przypadku jego wystąpienia.
Spis treści:
- Co to jest liszaj twardzinowy?
- Jak wygląda liszaj twardzinowy?
- Jakie są przyczyny liszaja twardzinowego sromu?
- Liszaj twardzinowy – jakie daje objawy?
- Jak leczyć liszaja twardzinowego?
- Czy liszaj twardzinowy sromu jest uleczalny?
- Liszaj twardzinowy – często zadawane pytania
- Liszaj twardzinowy – podsumowanie
Co to jest liszaj twardzinowy?
Liszaj twardzinowy to przewlekłe, zapalne schorzenie dermatologiczne, które po raz pierwszy zostało opisane w 1887 roku przez Hallopeau. Dawniej choroba ta była określana mianem liszaja twardzinowego zanikowego, a także liszaja białego. Z liszajem twardzinowym zdecydowanie częściej borykają się kobiety (aż 85% przypadków dotyczy płci żeńskiej). Choroba może rozwinąć się w każdym wieku, zarówno u dzieci, jak i starszych pacjentów. Warto jednak wiedzieć, że liszaj twardzinowy cechuje się dwoma szczytami zachorowań, które przypadają na 8.-13. rok życia, a także na piątą i szóstą dekadę życia.
>> Przeczytaj także: Liszaj płaski – objawy, rodzaje, diagnostyka i leczenie
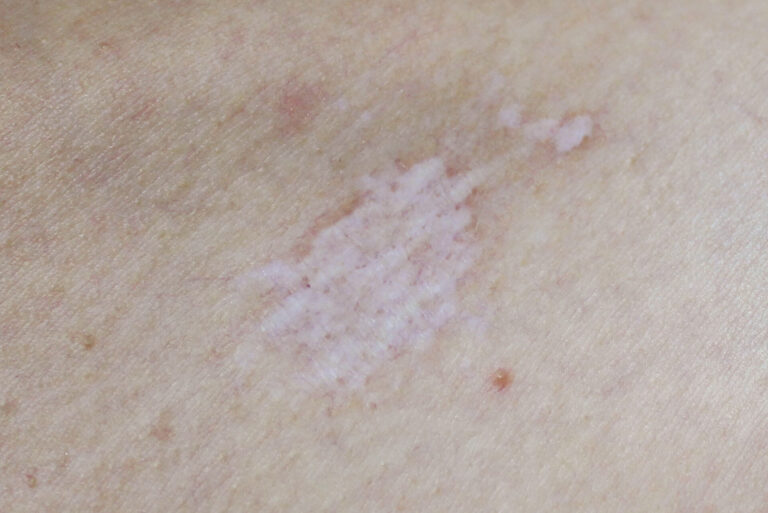
Jak wygląda liszaj twardzinowy?
Zmiany skórne w przebiegu liszaja twardzinowego w większości przypadków zajmują okolice anogenitalną, tylko około 15% przypadków choroby dotyczy skóry poza tym obszarem. U kobiet najczęściej obserwuje się liszaj twardzinowy sromu. Należy zaznaczyć, że zmiany chorobowe mogą pojawić się również w obrębie błony śluzowej jamy ustnej.
W obrazie klinicznym liszaja twardzinowego zlokalizowanego w okolicy płciowej dominują wykwity w postaci białawych grudek, które z czasem przekształcają się porcelanowe, stwardniałe blaszki. Skóra w okolicy anogenitalnej może być ścieńczała, zanikowa i przypominać pergamin.
Liszaj twardzinowy u mężczyzn najczęściej manifestuje się jako liszaj twardzinowy napletka i liszaj twardzinowy prącia. Zmiany skórne w postaci stwardnień i zaników mogą nawet grozić rozwojem stulejki.
W postaci pozagenitalnej można zaobserwować obecność dobrze odgraniczonych od skóry niezmienionej, hiperkeratotycznych blaszek. W tej odmianie choroby zmiany skórne najczęściej lokalizują się w obrębie:
- tułowia,
- okolicy podsutkowej,
- karku,
- górnej części pleców,
- pach,
- nadgarstków
- pośladków i ud,
- rzadziej w obrębie dłoni, podeszew i twarzy.
Jakie są przyczyny liszaja twardzinowego sromu?
Mimo wielu lat badań, konkretna przyczyna pojawiania się liszaja twardzinowego nadal nie została zidentyfikowana. Liszaj twardzinowy należy do chorób autoimmunologicznych, o czym świadczy między innymi obecność w surowicy pacjentów przeciwciał przeciwko białku macierzy zewnątrzkomórkowej typu I oraz przeciwciał skierowanych przeciwko składowym błony podstawnej. Jednak etiopatogeneza liszaja twardzinowego to nie tylko tło autoimmunologiczne. Przyczyn schorzenia upatruje się również w:
- czynnikach genetycznych – zauważono, że liszaj twardzinowy może mieć tendencje do występowania rodzinnego i być związany z antygenami zgodności tkankowej,
- czynnikach infekcyjnych – w tym zakażeniu wirusem HCV, wirusem brodawczaka ludzkiego, czy też krętkami z rodzaju Borrelia. Należy jednak zaznaczyć, że badania naukowe nie potwierdziły wprost związku między tymi infekcjami, a wzrostem ryzyka rozwoju liszaja twardzinowego,
- stresie oksydacyjnym – na poparcie tej tezy ma wskazywać obecność w obrazie histologicznym zwiększonej liczby produktów peroksydacji lipidów i białek, a także oksydacyjnego uszkodzenia materiału DNA.
Warto również wspomnieć, że liszaj twardzinowy częściej współwystępuje z innymi schorzeniami autoimmunologicznymi, w tym na przykład z autoimmunologicznym zapaleniem tarczycy (choroba Hashimoto), a także niedokrwistością złośliwą.

Liszaj twardzinowy – jakie daje objawy?
Liszaj twardzinowy to nie tylko zmiany skórne. Wykwity chorobowe w okolicy płciowej wiążą się również z dyskomfortem pod postacią silnego świądu i pieczenia. Co więcej, w zaawansowanych postaciach choroby u kobiet może dojść do zrastania się warg sromowych, a także zwężenia wejścia do pochwy. U obu płci może wystąpić ból w czasie oddawania moczu. Objawy te wiążą się z istotnych obniżeniem jakości życia, co wymaga włączenia odpowiedniego leczenia.
Jak leczyć liszaja twardzinowego?
W leczeniu liszaja twardzinowego zastosowanie znajdują takie substancje i metody terapeutyczne jak:
- miejscowe, silne glikokortykosteroidy (klobetazol),
- glikokortykosteroidy podawane bezpośrednio do zmian skórnych (doogniskowo),
- miejscowe inhibitory kalcyneuryny (pimekrolimus i takrolimus),
- fototerapia PUVA,
- terapia fotodynamiczna,
- preparaty hormonalne (w tym estrogen, progesteron),
- leczenie ogólne z wykorzystaniem doustnej acytretyny (jest to retinoid).
Czy liszaj twardzinowy sromu jest uleczalny?
W liszaju twardzinowym może dochodzić do trwałego wyciszenia objawów chorobowych, jednak możliwe są również nawroty. Pacjent z postawionym rozpoznaniem liszaja twardzinowego wymaga regularnych kontroli dermatologicznych.
>> Warto wiedzieć: Liszajec zakaźny u dzieci i dorosłych. Objawy, diagnostyka, leczenie
Liszaj twardzinowy – często zadawane pytania
Liszaj twardzinowy nie jest powszechnia znaną chorobą, co sprawia, że wzbudza wiele wątpliwości. Odpowiedzi na najczęściej zadawane przez pacjentów pytania znajdziemy w poniższych akapitach.
Skąd bierze się liszaj twardzinowy?
Liszaj twardzinowy to schorzenie o złożonej etiopatogenezie. Do jego rozwoju predysponują zarówno czynniki genetyczne, immunologiczne, jak i prawdopodobnie środowiskowe (narażenie na niektóre infekcje). Nie ma jednej konkretnej przyczyny, która zapoczątkowuje pojawienie się objawów liszaja twardzinowego. Największą rolę w pojawieniu się zmian skórnych odgrywają jednak czynniki immunologiczne.
Jak pozbyć się liszaja twardzinowego?
Podejrzenie liszaja twardzinowego wymaga zrealizowania konsultacji dermatologicznej. Lekarz specjalista po ocenie stanu dermatologicznego zadecyduje o dalszych krokach. Może skierować pacjenta na biopsję skóry, której celem jest pobranie wycinka do badania histopatologicznego, co potwierdzi rozpoznanie liszaja twardzinowego.
Czy liszaj to grzybica?
Liszaj twardzinowy nie jest schorzeniem tożsamym z grzybicą skóry. Jest to przewlekła, zapalna choroba o podłożu autoimmunologicznym, która nie jest wywoływana przez infekcję grzybiczą. Jeżeli lekarz podejrzewa u pacjenta grzybicę skóry to zadecyduje o konieczności wykonania badania mykologicznego.
Czym grozi nieleczony liszaj?
Nieleczony liszaj twardzinowy grozi wieloma powikłaniami. Z jednej strony zagrożenie stanowią zmiany bliznowate, które mogą doprowadzić do zrośnięcia warg sromowych, a u mężczyzn do stulejki. Z drugiej strony, należy mieć świadomość, że przewlekły liszaj twardzinowy może być związany z ryzykiem nowotworzenia. W obrębie zmian skórnych w przebiegu liszaja twardzinowego mogą pojawić się bowiem ogniska raka kolczystokomórkowego (SCC).
>> Dowiedz się więcej: Choroby skóry u człowieka. Najczęściej występujące dermatozy
Czy liszaj twardzinowy jest zaraźliwy?
Liszaj twardzinowy nie jest chorobą zakaźną, co sprawia, że pośredni lub bezpośredni kontakt ze zmianami skórnymi nie grozi zachorowaniem. Nie można się również zarazić drogą kontaktów seksualnych.
Czy liszaj twardzinowy nawraca?
Liszaj twardzinowy jest chorobą, która może przebiegać z okresami remisji, czyli wyciszenia objawów chorobowych, ale również z okresami zaostrzeń. Przebieg bywa niekiedy trudny do przewidzenia, jednak odpowiednio dobrane leczenie dermatologiczne daje szansę na trwałą poprawę. Jeżeli na naszej skórze pojawiają się jakiekolwiek niepokojące zmiany skórne, to należy udać się do gabinetu lekarza dermatologa i skonsultować swoje obawy.
Liszaj twardzinowy – podsumowanie
- Liszaj twardzinowy to schorzenie dermatologiczne, którego etiopatogeneza obejmuje zarówno zaburzenia immunologiczne, genetyczne, jak i czynniki środowiskowe.
- Objawy skórne związane z liszajem twardzinowym pojawiają się przede wszystkim w okolicy anogenitalnej, jednak mogą również pojawić się w dowolnym obszarze na skórze ciała, a także na śluzówkach jamy ustnej.
- W obrazie klinicznym obserwuje się między innymi białawe grudki, zlewające się w większe tarczki, skóra z czasem staje się ścieńczała, zanikowa, pergaminowa. Zmianom skórnym często towarzyszy silny świąd i pieczenie.
- W diagnostyce ważną rolę odgrywa badanie histopatologiczne wycinka skóry.
- Leczeniem liszaja twardzinowego zajmują się lekarze dermatolodzy. W terapii zastosowanie znajdują leki miejscowe, leki ogólne, a także specjalistyczne procedury takie jak terapia fotodynamiczna.
Bibliografia
- M. Bencal-Kusińska i inni, Liszaj twardzinowy — postać hiperkeratotyczna, Forum Dermatologiczne 2015, tom 1, nr 1, 28–31,
- A. Cegielska i inni, The role of genetic, autoimmune, infective and hormonal factors in pathogenesis of lichen sclerosus – review of the literature. Dermatology Review/Przegląd Dermatologiczny. 2011;98(4):355-361,
- A. Leibovitz i inni, Vulvovaginal examinations in eldery nursing home women residents. Arch Gerontol Geriatr 2000, 31, 1-4,
- L. Rudnicka i inni, Współczesna Dermatologia, PZWL, Warszawa 2022,
- J. L. Bolognia i inni, Fourth Edition Dermatologia, Medipage, Warszawa 2022.