Składniki odżywcze to substancje chemiczne, które muszą być dostarczone organizmowi człowieka wraz z pożywieniem. Podstawowe składniki odżywcze to węglowodany, białka i tłuszcze. Składnikami odżywczymi są również witaminy i składniki mineralne. Artykuł opisuje węglowodany, które stanowią podstawowy składnik odżywczy i energetyczny.
Spis treści:
- Co to są węglowodany? Rodzaje węglowodanów
- Funkcje węglowodanów
- Źródła węglowodanów w diecie
- Zapotrzebowanie organizmu człowieka na węglowodany
- Podsumowanie
Co to są węglowodany? Rodzaje węglowodanów
Węglowodany – inaczej cukry – to związki chemiczne składające się z węgla, wodoru i tlenu.
Podział węglowodanów oparty jest na ich budowie chemicznej. Zaliczamy do nich cukry proste i cukry złożone.
Cukry proste to monosacharydy.
Cukry złożone to:
- oligosacharydy – zbudowane z 2-10 cząsteczek cukrów prostych,
- polisacharydy – wielocukry.
Cukry proste – monosacharydy
Cukry proste – czyli monosacharydy – to grupa węglowodanów zawierająca od 3 do 6 atomów węgla w jednej cząsteczce.
Najbardziej rozpowszechnione są heksozy – czyli cukry zawierające 6 atomów węgla, cukry z krótszym łańcuchem węglowym spotykane są rzadziej.
Przykłady cukrów prostych:
- heksozy – glukoza, fruktoza, galaktoza,
- pentozy – zawierające 5 atomów węgla: ryboza, rybuloza, ksyloza, arabinoza,
- tetrozy – zawierające 4 atomy węgla: treoza,
- triozy – zawierające 3 atomy węgla: aldehyd glicerynowy.
Najbardziej rozpowszechnionym w przyrodzie cukrem prostym, występującym w stanie wolnym, jest glukoza. Jest to cukier obecny w sokach owocowych i miodzie, zawierają go także tkanki zwierzęce – krew i płyny ustrojowe. Glukoza to również podstawowa jednostka wielu oligosacharydów i polisacharydów.
Fruktoza jest cukrem prostym występującym w stanie wolnym w miodzie. Od zawartości fruktozy w miodzie zależy m.in. jego indeks glikemiczny – im więcej fruktozy, tym IG miodu niższe. Fruktoza to także składnik wielu owoców i warzyw. Fruktoza jest również składnikiem oligosacharydów, np. sacharozy i polisacharydów, np. inuliny.
>>> Przeczytaj też: Miód i jego właściwości. Czy miód jest zdrowy? Miód a cukrzyca
Galaktoza to najczęściej składnik oligosacharydów, np. laktozy i polisacharydów, np. galaktanów i agaru. Galaktoza występuje również w połączeniu z białkami, jako glikoproteiny i tłuszczami, jako glikolipidy.
Monosacharydy zawierające 5 atomów węgla nie występują w przyrodzie samodzielnie. Ryboza jest składnikiem DNA i RNA, jest także elementem ATP – związku, który jest głównym nośnikiem energii w komórkach. Ksyloza to cząstka ksylanów budujących zdrewniałe tkanki roślinne, a arabinoza obecna jest w gumach roślinnych.
Cukry złożone – oligosacharydy
Oligosacharydy to cukry złożone z dwóch do dziesięciu cząsteczek cukrów prostych.
Oligosacharydy złożone z dwóch cząsteczek to dwucukry, wśród których najważniejsze są sacharoza i laktoza.
- Sacharoza – cukier buraczany – składa się w glukozy i fruktozy. Najwięcej sacharozy jest w burakach cukrowych i trzcinie cukrowej. Słodycz sacharozy to podstawowa jednostka, do której porównuje się słodycz innych cukrów.
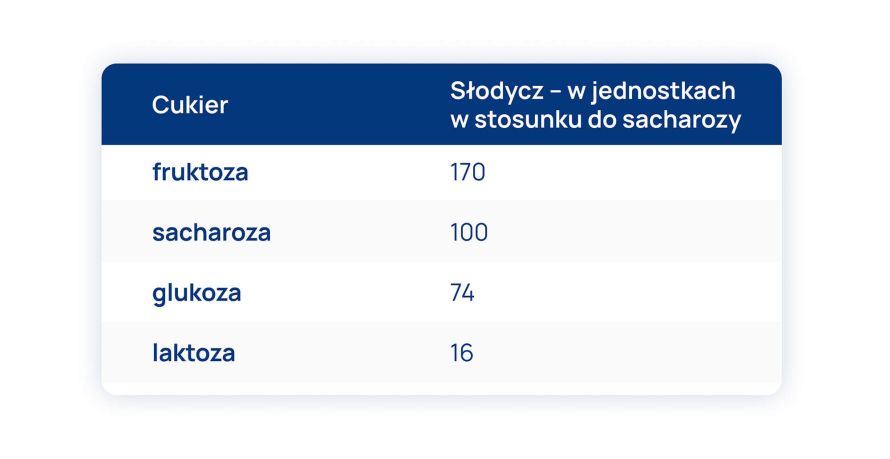
- Laktoza – cukier mleczny – składa się z glukozy i galaktozy. Laktoza jest słabiej rozpuszczalna w wodzie od sacharozy, występuje w mleku wszystkich ssaków. W przewodzie pokarmowym człowieka rozkładana jest przez enzym laktazę. Brak lub niedobór tego enzymu wywołuje nietolerancję laktozy.
- Maltoza – zbudowana jest z dwóch cząsteczek glukozy, obecna w organizmach roślinnych i zwierzęcych. Duże ilości maltozy występują w słodzie.
Do oligosacharydów o większej liczbie cząsteczek zaliczamy:
- rafinozę (trójcukier),
- stachiozę (czterocukier),
- werbaskozę (pięcokier).
Obecne w roślinach strączkowych, nie są hydrolizowane przez enzymy trawienne przewodu pokarmowego. Ulegają rozkładowi pod wpływem drobnoustrojów obecnych w jelicie, co jest przyczyną wzdęć występujących po spożyciu strączków.
Cukry złożone – polisacharydy
Grupa węglowodanów zbudowana z wielu cząsteczek cukrów prostych lub ich pochodych.
Z żywieniowego punktu widzenia można wyróżnić:
- polisacharydy skrobiowe – skrobia, glikogen, inulina,
- polisacharydy nie skrobiowe – grupa węglowodanów stanowiąca część błonnika pokarmowego.
Skrobia występuje w komórkach roślin, zbudowana jest z licznych – liczonych nawet w tysiące –cząsteczek glukozy. W budowie strukturalnej skrobi występuje amyloza i amylopektyna. Amylopektyna nie rozpuszcza się w wodzie, lecz w niej pęcznieje, przy ogrzewaniu wytwarzając kleik. Skrobia w największych ilościach występuje w ziarnach zbóż, ziemniakach i warzywach okopowych.
Błonnik pokarmowy – polisacharyd obecny w produktach roślinnych. Z żywieniowego punktu widzenia możemy wyróżnić:
- błonnik nierozpuszczalny (celuloza i lignina) – nie jest rozkładany przez bakterie jelitowe, wywiera pozytywny wpływ na motorykę przewodu pokarmowego, jednak w zbyt dużych ilościach może powodować wzdęcia,
- błonnik rozpuszczalny (pektyny, gumy, hemicelulozy, beta-glukany) – rozkładany przez bakterie jelitowe przewodu pokarmowego.
Funkcje węglowodanów
Rola i znaczenie węglowodanów w organizmie człowieka zależy od ich budowy oraz stopnia przyswajalności.
Węglowodany przyswajalne to podstawowe źródło energii – spalanie 1 g węglowodanów dostarcza 4 kcal.

Energia uzyskiwana z węglowodanów zużywana jest na utrzymanie prawidłowej ciepłoty ciała, pracy narządów wewnętrznych oraz aktywności ruchowej. Ważnym narządem w metabolizmie węglowodanów jest wątroba, w której wchłonięte z przewodu pokarmowego monosacharydy przekształcane są w glukozę, która jest paliwem dla mózgu, rdzenia kręgowego, erytrocytów, ale również serca, mięśni i jelit.
Mózg zużywa ok. 140 g glukozy na dobę, co stanowi aż 20% podstawowej przemiany energii. Erytrocyty potrzebują 40 g glukozy na dobę.
Węglowodany są również niezbędne do metabolizmu tłuszczów i białek. Przy niedostatecznej podaży cukrów kwasy tłuszczowe nie są całkowicie spalane, powstają ciała ketonowe, które przyczyniają się do zakwaszenia organizmu. Małe spożycie węglowodanów powoduje również, iż organizm zmuszony jest do pozyskiwania glukozy z aminokwasów – glukoneogeneza – co powoduje rozpad białek mięśniowych. Zbyt wysokie spożyciu cukrów skutkuje zjawiskiem odwrotnym i prowadzi do syntezy niektórych aminokwasów (np. alaniny) i tłuszczów, odkładanych następnie jako tłuszcz zapasowy.
Część węglowodanów magazynowana jest w postaci glikogenu zawartego w mięśniach i wątrobie. Inne cukry – ryboza i dezoksyryboza stanowią element struktury kwasów DNA i RNA. Cukier mleczny – laktoza – pomaga we wchłanianiu wapnia.
Źródła węglowodanów w diecie
Największe ilości węglowodanów występują w produktach pochodzenia roślinnego.
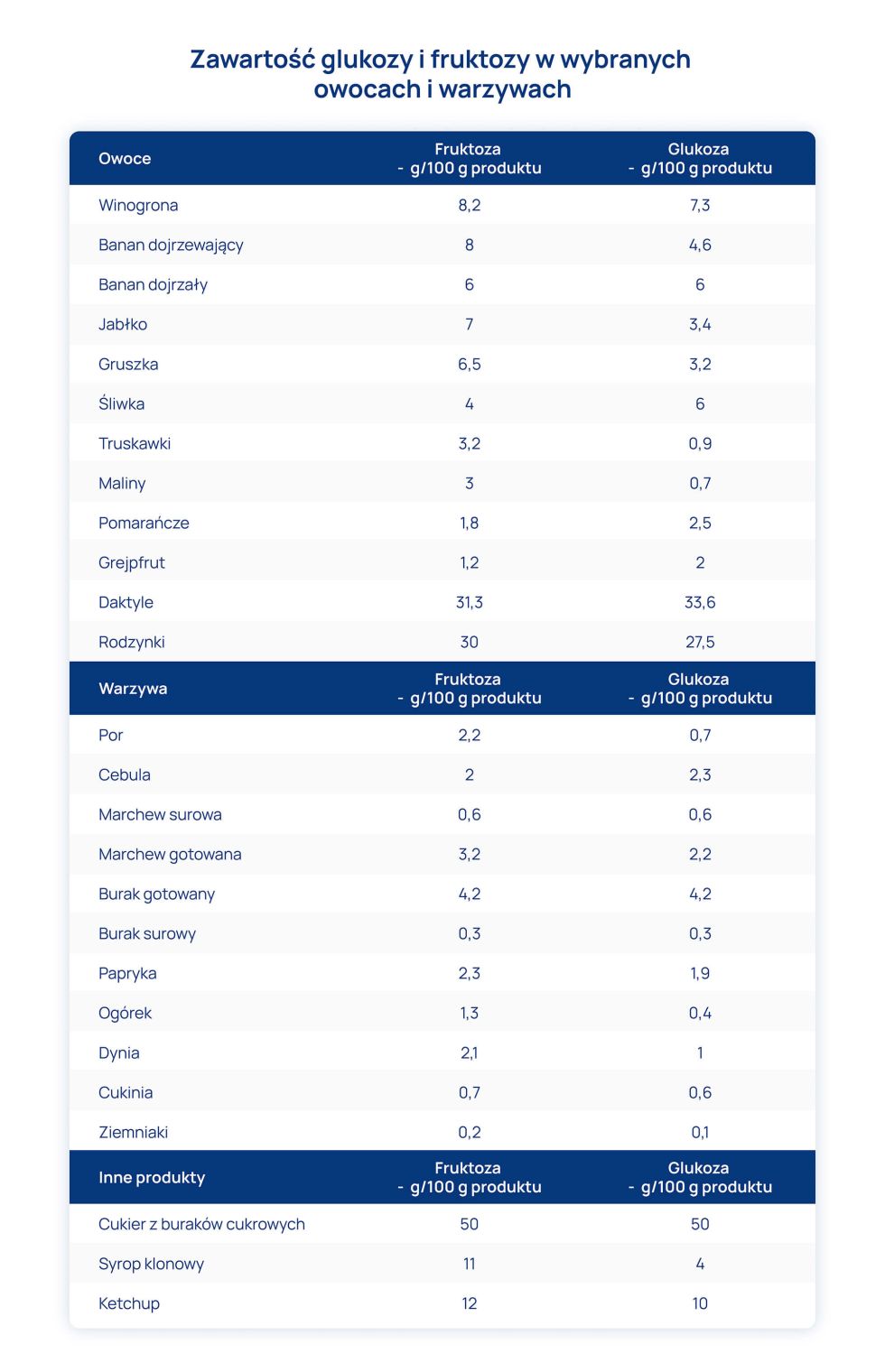
Cukry proste – glukoza i fruktoza – w postaci wolnej występują w owocach, warzywach, przetworach owocowych i warzywnych oraz w miodzie.
Zawartość cukrów w tych produktach jest zróżnicowana, zależy od rodzaju i odmiany danej rośliny i od stopnia ich dojrzałości. Owoce zawierają więcej cukrów prostych niż warzywa. Należy pamiętać, iż glukoza i fruktoza są również dodawane do żywności jako syrop glukozowo-fruktozowy.
Sacharoza występuje przede wszystkim w przetworzonej żywności jako cukier dodany oraz używana w gospodarstwach domowych (cukier rafinowany), w wyrobach ciastkarskich i cukierniczych.
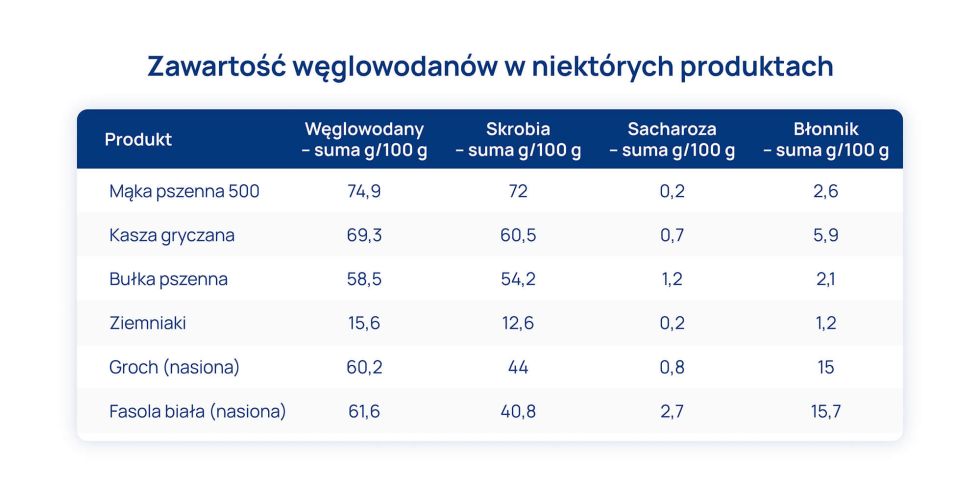
Z żywieniowego punktu widzenia podstawowym źródłem węglowodanów są jednak produkty zbożowe, ziemniaki i nasiona roślin strączkowych.
Zapotrzebowanie organizmu człowieka na węglowodany
Węglowodany są traktowane jako źródło energii. Podstawą wyliczenia ile węglowodanów dziennie powinno być w diecie jest założenie, iż po zaspokojeniu zapotrzebowania organizmu na białko (10-20% całodziennej energii) i tłuszcz (20-35% całodziennej energii) pozostałe potrzeby powinny być pokryte przez węglowodany.
Należy pamiętać, iż węglowodany muszą być obecne w diecie, glukoza to podstawowy składnik energetyczny organizmu. Długotrwały niedobór węglowodanów powoduje, iż organizm – poszukując źródła glukozy – zaczyna wykorzystywać do tego celu białko. W rezultacie białko – zamiast służyć celom budulcowym – jest wykorzystywane jako źródło energii.
Oczywiście problemem jest również nadmiar węglowodanów w diecie, który jest jednym z elementów prowadzących do choroby, jaką jest otyłość.
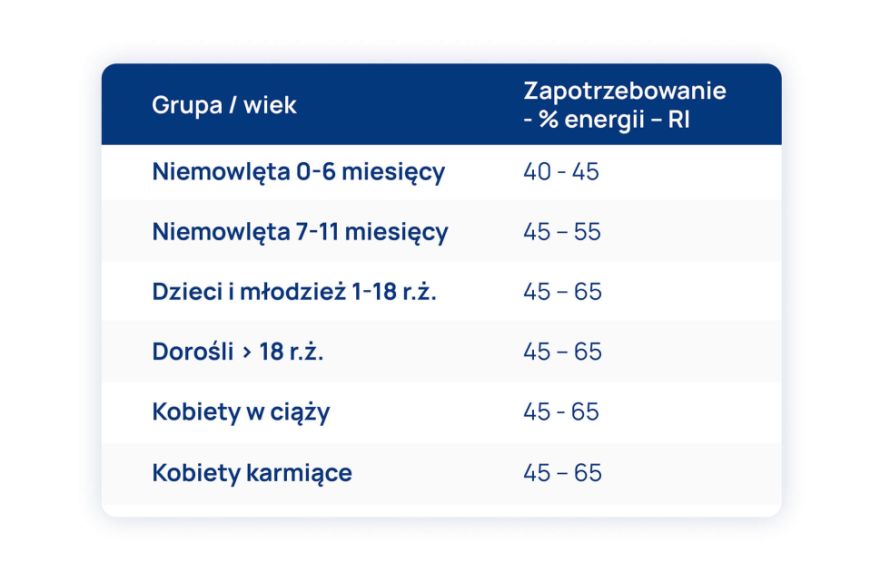
Szczegółowe dane przedstawia tabela.
Normy na węglowodany ustalone jako referencyjny zakres spożycia

Podsumowanie
Węglowodany to bardzo ważny składnik pokarmowy, który musi być obecny w diecie człowieka. Zarówno nadmiar węglowodanów, jak i niedobór węglowodanów, nie są korzystne dla zdrowia, dlatego trzeba w tej kwestii zachować zdrowy rozsądek.
Bibliografia
- Gertig H., Przysławski J., Bromatologia. Zarys nauki o żywności i żywieniu. Wydawnictwo Lekarskie PZWL, Warszawa 2015, 31-42. (dostęp 30.01.2025)
- Jarosz M., Rychlik E., Stoś K., Charzewska J. (red.), Normy żywienia dla populacji Polski i ich zastosowanie. Narodowy Instytut Zdrowia Publicznego – Państwowy Zakład Higieny, 2020, 134-147. (dostęp 30.01.2025)
- https://www.alergiapokarmowa.pl/wp-content/uploads/2017/12/tabela-nietolerancji.pdf. (dostęp 30.01.2025)