Artykuł powstał 27.09.2021 r., ostatnia aktualizacja: 06.03.2026 r.
Alergia pokarmowa to dynamicznie narastający problem zdrowotny, który dotyka miliony osób na całym świecie, znacząco wpływając na ich codzienne funkcjonowanie. Zrozumienie mechanizmów tej choroby oraz jej rozpoznania jest niezwykle istotne, aby uniknąć groźnych dla zdrowia i życia powikłań, takich jak wstrząs anafilaktyczny.
| Z tego artykułu dowiesz się: >> co to jest alergia pokarmowa i czy to częsty problem, >> czym jest wielka ósemka alergenów, >> jaka jest różnica między alergią a nietolerancją pokarmową, >> na czym polega przełom w diagnostyce molekularnej i jak pozwala ona przewidzieć ryzyko ciężkich reakcji, >> czy z alergii pokarmowej można „wyrosnąć” i jakie są obecnie dostępne metody profilaktyki oraz leczenia. |
Spis treści:
- Co to jest alergia pokarmowa?
- Skala alergii pokarmowej na świecie
- Alergia pokarmowa a nietolerancja pokarmowa – czym się różnią?
- Alergia pokarmowa – lista najczęstszych alergenów pokarmowych
- Przyczyny alergii pokarmowej
- Alergia pokarmowa – od czego zależy przebieg reakcji alergicznej?
- Alergia pokarmowa – objawy
- Diagnostyka alergii pokarmowej – jakie badania i testy należy wykonać?
- Alergia pokarmowa – profilaktyka
- Dieta eliminacyjna przy alergii pokarmowej
- Ile trwa alergia pokarmowa?
- Czy dziecko może wyrosnąć z alergii pokarmowej?
- Zespół pyłkowo-pokarmowy a alergia pokarmowa
- Leczenie alergii pokarmowej u dorosłych i u dzieci
- Zakończenie
- Alergia pokarmowa – sekcja FAQ
Co to jest alergia pokarmowa?
Alergia pokarmowa to nieprawidłowa i powtarzalna odpowiedź układu odpornościowego na konkretny składnik żywności (zazwyczaj białko), który dla osób zdrowych jest nieszkodliwy. W przeciwieństwie do nietolerancji pokarmowych (np. laktozy), w proces ten zaangażowane są mechanizmy immunologiczne.
W literaturze medycznej alergię pokarmową dzieli się na trzy główne typy w zależności od sposobu, w jaki reaguje organizm:
- Alergia IgE-zależna – najczęstsza i najbardziej gwałtowna. Układ odpornościowy wytwarza przeciwciała klasy E (IgE), które po kontakcie z alergenem powodują natychmiastowe uwolnienie histaminy. Objawy pojawiają się w ciągu kilku minut do dwóch godzin (np. pokrzywka, obrzęk, a w skrajnych przypadkach anafilaksja),
- Alergia IgE-niezależna – reakcja zachodzi bez udziału przeciwciał IgE, głównie za pośrednictwem limfocytów T. Objawy są zazwyczaj opóźnione (pojawiają się po kilku godzinach lub dniach) i dotyczą głównie układu pokarmowego (np. zapalenie jelit wywołane białkami pokarmowymi – FPIES),
- Alergia mieszana – łączy oba powyższe mechanizmy (np. eozynofilowe zapalenie przełyku lub atopowe zapalenie skóry zaostrzane przez pokarmy).
>> Może Cię zainteresować: Nietolerancja histaminy czy alergia? Czym się różnią i dlaczego łatwo je pomylić?
Skala alergii pokarmowej na świecie
Na całym świecie problem alergii na pokarmy staje się coraz poważniejszy, dotyczy to szczególnie krajów rozwiniętych. Narastający problem uzależniony jest od zmian klimatycznych, zanieczyszczeń gleby i powietrza, upatruje się go w paleniu papierosów, nadużywaniu antybiotyków. Bardzo duże znaczenie ma styl życia, w tym dieta i kontakt z patogenami.
| To ciekawe: Według Światowej Organizacji Zdrowia (WHO) z powodu alergii pokarmowych IgE-zależnych może cierpieć już ponad 20 proc. populacji świata. Szacuje się, że alergia pokarmowa dotyka około 8% dzieci i do 10% dorosłych w krajach rozwiniętych. Większość z nich (60 %) to kobiety, a częstotliwość ich występowania wśród dzieci do 5. roku życia zwiększyła się dwukrotnie w ostatniej dekadzie. W Polsce nie mamy dokładnych danych epidemiologicznych o skali alergii pokarmowej, jednak obserwujemy trendy zbieżne z globalnymi. |
Alergia pokarmowa a nietolerancja pokarmowa – czym się różnią?
Alergia pokarmowa to nie to samo, co nietolerancja pokarmowa. Nie można używać tych pojęć zamiennie.
W alergii pokarmowej układ odpornościowy traktuje białka obecne w pożywieniu jako zagrożenie. Silne objawy mogą wystąpić po śladowej ilości pokarmu, a nawet wystarczy samo wdychanie oparów zawierających dany alergen. Mogą to być reakcje zagrażające życiu.
Natomiast nietolerancja pokarmowa wiąże się z niedoborem lub brakiem enzymów. Najczęściej mówimy o nietolerancji laktozy, fruktozy czy histaminy, nie ma tutaj udziału układ immunologiczny. Zazwyczaj objawy występują po zjedzeniu znacznej ilości problematycznej żywności, a także w przeciwieństwie do alergii, nie są to reakcje zagrażające życiu.
Alergia pokarmowa – lista najczęstszych alergenów pokarmowych
Alergia pokarmowa może ujawniać się szeregiem rozmaitych objawów, w tym w postaci biegunek, wymiotów, pokrzywki, duszności, obrzęku języka czy groźnego wstrząsu anafilaktycznego. Objawy alergii pokarmowej występują najczęściej u niemowląt i dzieci, ale mogą pojawić się w każdym wieku. Najczęstsze alergie pokarmowe u dorosłych to alergia na skorupiaki i mięczaki, a także orzechy, orzeszki ziemne i ryby.
Istnieje ponad 170 pokarmów, które według doniesień wywołują reakcję alergiczną, ale osiem określonych rodzajów żywności odpowiada za ponad 90% z nich. Wielka ósemka to:
- mleko,
- jajka,
- orzeszki ziemne,
- orzechy,
- pszenica,
- soja,
- ryby,
- skorupiaki.
Amerykańska instytucja rządowa FDA – Agencja Żywności i Leków – rozszerzyła dotychczasową listę o dziewiąty alergen, którym jest sezam. Amerykańskie prawo od 1 stycznia 2023 wymaga od producentów żywności deklarowania obecności sezamu jako głównego alergenu pokarmowego na etykiecie każdej żywności. Ponadto rozporządzenie Parlamentu Europejskiego i Rady Unii Europejskiej w liście najpopularniejszych alergenów wymienia również selera, gorczycę i ich produkty pochodne.
>> Przeczytaj również: Alergia na jajko i orzechy, czyli dieta eliminacyjna w praktyce
Przyczyny alergii pokarmowej
Przyczyny rozwoju alergii pokarmowej są wieloczynnikowe. Bardzo ważną rolę odgrywa genetyka (rodzinne występowanie alergii) oraz czynniki środowiskowe, w tym styl życia i nadmierna higienizacja środowiska. Najnowsza hipoteza bariery nabłonkowej (ang. epithelial barrier hypothesis), sugeruje wzrost alergii w wyniku uszkodzenia bariery skórnej, np. w przebiegu atopowego zapalenia skóry (AZS), ale także jelitowej czy dróg oddechowych w wyniku działania detergentów, zanieczyszczeń (np. smog) czy mikroplastiku. Wnikające do organizmu alergeny wywołują przewlekłe zapalenie i nadmierną reakcję układu odpornościowego.
Ważnym aspektem jest również opóźnione wprowadzanie pokarmów uzupełniających do diety niemowląt podczas rozszerzania diety, co paradoksalnie może zwiększać ryzyko alergii.
Alergia pokarmowa – od czego zależy przebieg reakcji alergicznej?
Przebieg reakcji alergicznej zależy od wielu czynników i nie jest stały u danego pacjenta – ta sama osoba może raz zareagować łagodnie, a innym razem doznać wstrząsu anafilaktycznego. Według aktualnych badań nasilenie reakcji alergicznej zależy to od trzech grup czynników:
1. Czynniki związane z samym pokarmem:
- dawka alergenu – choć u osób silnie uczulonych nawet śladowe ilości wywołują reakcję, istnieje tzw. dawka progowa, powyżej której ryzyko ciężkiej anafilaksji drastycznie rośnie,
- rodzaju pokarmu – tłuszcze zawarte w pokarmie mogą opóźniać wchłanianie alergenu, co czasem przesuwa reakcję w czasie, ale czyni ją trudniejszą do opanowania,
- obróbka termiczna – wysoka temperatura może niszczyć niektóre alergeny (np. w owocach), ale wzmacniać inne (np. pieczenie orzeszków ziemnych zwiększa ich zdolność do wiązania przeciwciał IgE).
2. Kofaktory (czynniki wzmacniające):
To elementy, które same nie uczulają, ale mogą nasilać objawy alergii. Należą do nich, m.in.:
- wysiłek fizyczny – zwiększa przepuszczalność jelit i szybkość krążenia krwi,
- alkohol oraz niesterydowe leki przeciwzapalne (NLPZ) – obniżają próg wrażliwości komórek tucznych,
- infekcje i stres – osłabienie organizmu oraz zmiany hormonalne mogą nasilić wyrzut histaminy.
3. Stan kliniczny pacjenta:
- współistniejąca astma – jest najważniejszym czynnikiem zwiększającym ryzyko zgonu z powodu alergii pokarmowej, zwłaszcza jeśli nie jest ona prawidłowo kontrolowana lekami,
- wiek – u małych dzieci dominują objawy skórne i gastryczne, natomiast u nastolatków i dorosłych częściej dochodzi do groźnych objawów ze strony układu oddechowego i krążenia,
- dysbioza jelitowa – najnowsze badania wykazały, że zaburzenia mikrobioty jelitowej sprzyjają gwałtowniejszym odpowiedziom układu odpornościowego na alergen.
>> Może Cię zainteresować: Postaw na zdrowe jelita!
Alergia pokarmowa – objawy
Objawy alergii mogą wystąpić w różnym czasie. W przypadku alergii IgE-zależnej objawy pojawiają się zazwyczaj bardzo szybko – od kilku minut do dwóch godzin po spożyciu pokarmu. W reakcjach opóźnionych (IgE-niezależnych) objawy mogą wystąpić po wielu godzinach, a nawet dniach. Wyróżnia się dwa główne symptomy:
- zmiany skórne – to najczęstszy sygnał uczulenia. Mogą przybierać formę ostrej pokrzywki (swędzące bąble), obrzęku naczynioruchowego (opuchlizna warg, powiek) lub zaostrzenia atopowego zapalenia skóry (AZS). Często pojawia się również świąd skóry i zaczerwienienie.
- objawy ze strony układu pokarmowego – manifestacje gastryczne obejmują m.in. zespół alergii jamy ustnej (świąd ust i gardła), nudności, wymioty, bóle brzucha o charakterze kolkowym oraz biegunkę. U niemowląt sygnałem może być krew w stolcu lub przewlekłe zaparcia.
Diagnostyka alergii pokarmowej – jakie badania i testy należy wykonać?
Diagnostyka molekularna w alergii pokarmowej
Aby skutecznie zapobiegać reakcji alergicznej najważniejsza jest prawidłowa identyfikacja pokarmu wywołującego alergię. Zaleca się wykonanie ocena profilu uczulenia z krwi np. w badaniach panelowych, obejmujących wiele alergenów, w tym wziewnych, jak i pokarmowych.
Zarówno klasyczne testy serologiczne, jak i szeroko wykorzystywane w gabinetach lekarskich testy skórne oparte są na ekstraktach alergenów. Ten ekstrakt to tzw. wodny wyciąg, który jest mieszaniną wielu białek danego alergenu. Dla tej mieszaniny oznaczany jest poziom przeciwciał IgE.
Oba rodzaje testów są kluczowym elementem na początkowym etapie diagnostyki alergii. Wskazują one źródła uporczywych objawów. Jednak należy pamiętać, że szczególnie u pacjentów wielouczuleniowych nie zawsze robią to wiarygodnie. Dopiero precyzyjna diagnostyka z wykorzystaniem molekularnych cząstek alergenów, dla których mierzony jest poziom przeciwciał, pozwala ujawnić reaktywność krzyżową i wskazać prawdziwy czynnik alergizujący.
Ponadto wykorzystanie diagnostyki molekularnej pozwala przewidzieć ciężkość reakcji. To wszystko sprawia, że diagnoza w połączeniu z objawami klinicznymi będzie pewna, a zastosowane leczenie czy zalecenia dietetyczne skuteczne.
Alergologia molekularna to zarówno pojedyncze oznaczenia molekuł, jak i duże ich panele – platformy molekularne. System ten usprawnia procedurę postępowania z pacjentem w gabinecie alergologa, dostarczając kompleksowy i szczegółowy profil uczuleniowy, a wszystko za pomocą jednorazowego pobrania krwi. Testy molekularne mają swój szczególny udział w alergii pokarmowej, tutaj poznanie cząstek uczulających jest niezwykle ważne nie tylko dla zdrowia, ale i życia pacjenta.
Profil uczuleniowy
Poniższa tabela zawiera wybrane białka uczulające, które wiążą się z ciężkim przebiegiem alergii. Jeżeli dana osoba jest uczulona na poniższe alergeny, istnieje wysokie prawdopodobieństwo ciężkich reakcji ogólnoustrojowych. Ustalenie tak dokładnego profilu uczuleniowego możliwe jest dopiero dzięki zastosowaniu diagnostyki molekularnej.
| Mleko | Kazeina – Bos d 8 |
| Jajko | Owomukoid – Gal d 1 |
| Orzeszki ziemne | Białka zapasowe – Ara h 1, Ara h 2, Ara h 3, Ara h 6, Oleozyna – Ara h 15 |
| Soja | Białka zapasowe – Gly m 5, Gly m 6, Gly m 8 |
| Orzech nerkowca | Białka zapasowe – Ana o 2 , Ana o 3 |
| Pszenica zwyczajna | Inhibitor alfa-amylazy I trypsyny – Tri aA_TI, Omega 5-gliadyna – Tri a 19 |
| Krewetka | Tropomiozyna – Pen m 1, Inne- Pen m 2, Pen m 3, Pen m 4 |
| Dorsz | Parwalbumina – Gad c 1/ Gad m 1 |
Wśród dużych paneli molekularnych na szczególną uwagę zasługuje test ALEX. ALEX to największy panel molekularny – aż 300 alergenów w jednym teście. Badanie można wykonać bez skierowania i przerywania stosowanego leczenia. Test jest odpowiedni dla każdej osoby, od 6. miesiąca życia. Test ALEX to kompletna diagnostyka dla alergenów wziewnych – pyłki roślin (trawy, chwasty, drzewa), sierści zwierząt, mikroorganizmów i zarodników pleśni. Dla alergenów pokarmowych, w tym orzechów i roślin strączkowych, ryb, owoców morza czy protein zwierzęcych. Test zapewnia diagnostykę alergii również dla jadu owadów i lateksu.
Test ALEX – wykonaj test:
• aby ustalić przyczynę reakcji alergicznej,
• aby zidentyfikować reakcje krzyżowe,
• jeśli podejrzewasz alergię pokarmową,
• aby znaleźć przyczynę reakcji anafilaktycznych,
• w celu określenia ryzyka ciężkich reakcji na alergeny,
• aby przewidzieć skuteczność swoistej immunoterapii,
• aby dopasować odpowiednie zalecenia dietetyczne,
• u dzieci z objawami alergii,
• jeżeli jesteś w ciąży.

Alergia pokarmowa – profilaktyka
Według najnowszych badań wczesne wprowadzanie alergenów (np. orzeszki ziemne, jajka) do diety niemowląt między 4. a 11. miesiącem życia może znacząco zredukować ryzyko rozwoju alergii. Ważna jest również dbanie o barierę skórną i unikanie zbędnych antybiotykoterapii oraz sterylizacji otoczenia.
Dieta eliminacyjna przy alergii pokarmowej
Dieta eliminacyjna powinna być stosowana wyłącznie pod nadzorem lekarza i dietetyka, po potwierdzeniu alergii. Nieuzasadnione wykluczanie grup produktów może prowadzić do niedoborów żywieniowych i zaburzeń wzrastania u dzieci.
>> Więcej informacji przeczytasz w artykule o diecie eliminacyjnej: Dieta eliminacyjna – na czym polega i kto powinien ją stosować? Niepożądane skutki
Ile trwa alergia pokarmowa?
Czas trwania alergii jest cechą indywidualną. Niektóre alergie mają charakter przetrwały (np. na orzechy czy owoce morza), inne wygasają wraz z dojrzewaniem układu odpornościowego. Monitorowanie poziomu swoistych przeciwciał IgE przeciwko konkretnym molekułom pozwala ocenić szansę na ustąpienie uczulenia.
Czy dziecko może wyrosnąć z alergii pokarmowej?
Z alergii można wyrosnąć, ale to zależy od jej rodzaju i ciężkości. Badania wykazały, że od 60% do 80% dzieci z alergią na mleko lub jajka wyrośnie z alergii na te pokarmy przed ukończeniem 16. roku życia. Obecne możliwości diagnostyczne pozwalają kontrolować ten proces. I tak okresowe mierzenie poziomu przeciwciał dla owomukoidu – jaja czy kazeiny, głównego białka mleka – oraz ich spadek będzie świadczył o nabywaniu tolerancji, czyli „wyrastaniu z alergii”.
W przypadku pozostałych alergenów odsetek pacjentów, którzy wyrosną z alergii nie jest tak optymistyczny. Dla orzeszków ziemnych będzie to tylko 20% dzieci, dla orzechów 14%, a w przypadku alergii na ryby i skorupiaki tylko 4-5%.
| Warto wiedzieć: Jak wskazuje WHO, badania epidemiologiczne pokazują, że wśród niemowląt uczulonych na pokarmy około 80% dzieci osiągnie tolerancję do piątych urodzin, ale u 35% z nich może dojść do nadwrażliwości na inne produkty. |
Zespół pyłkowo-pokarmowy a alergia pokarmowa
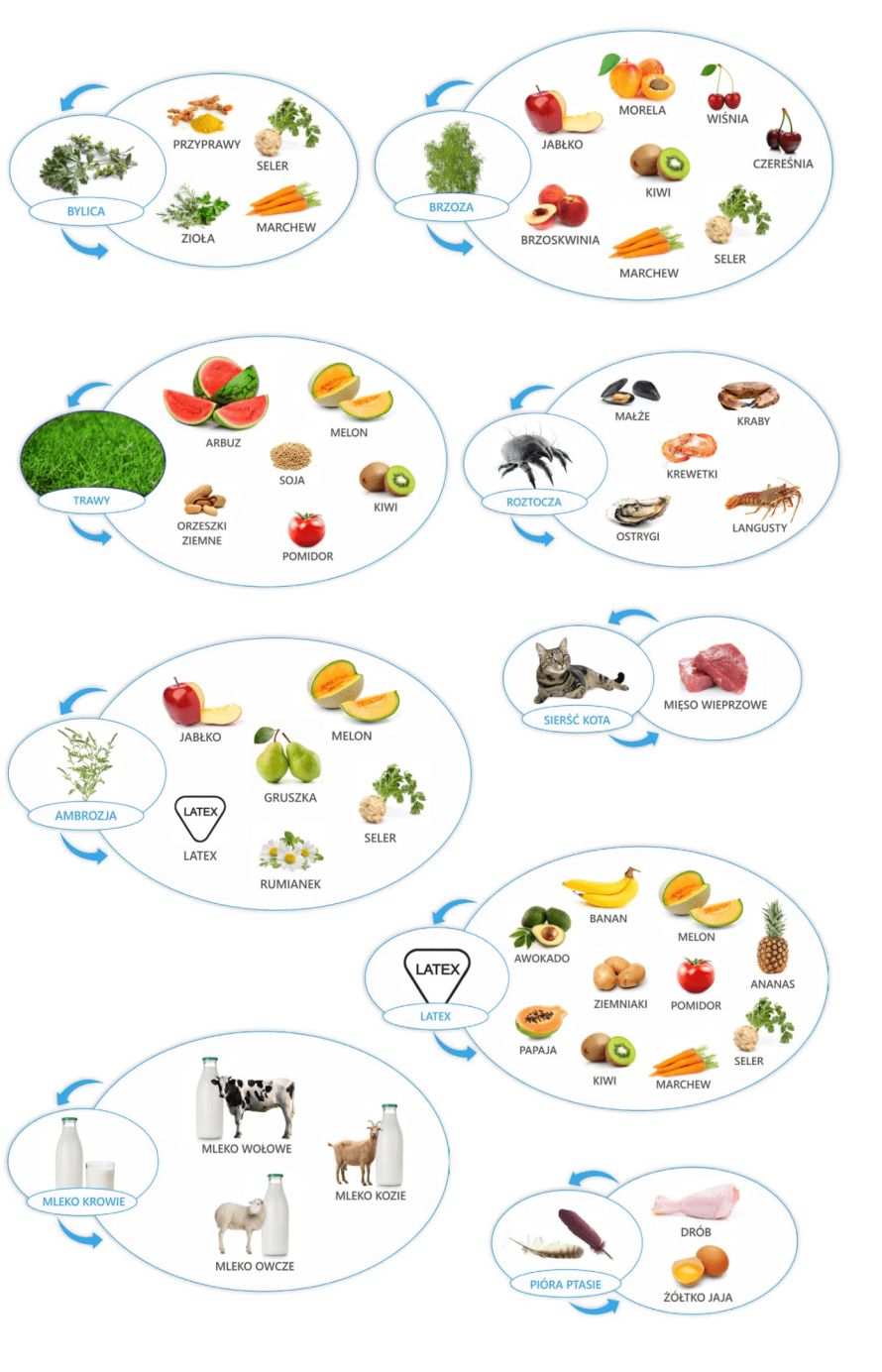
Niektórzy pacjenci odczuwają swędzenie w jamie ustnej i gardle, czasami z łagodnym obrzękiem, bezpośrednio po zjedzeniu świeżych owoców lub warzyw. Jest to tzw. zespół pyłkowo-pokarmowy, wywołany przez alergeny reagujące krzyżowo, obecne zarówno w pyłku, jak i surowych owocach czy warzywach. Nie jest to alergia pokarmowa, chociaż objawy występują po pożywieniu, co może być mylące. Prawdziwą przyczyną jest alergia na pyłki.
>> Warto sprawdzić też: Alergia na pyłki traw. Objawy i leczenie alergii na trawy
O reakcji krzyżowej mówimy wtedy, gdy alergeny wykazują znaczne podobieństwo w budowie między sobą. Na przykład osoby uczulone na pyłek brzozy mogą reagować objawami po spożyciu jabłka (alergeny brzozy i jabłka mają w składzie białko o zbliżonej budowie). Prawdziwą przyczyną uczulenia jest pyłek brzozy, natomiast uczulenie na jabłko to wynik krzyżowej. Ustalenie charakteru alergii, daje nam również informacje, że to samo jabłko z dużym prawdopodobieństwem poza okresem pylenia brzozy będzie dobrze tolerowane, jak również to, że obróbka termiczna zniweluje właściwości alergizujące, a czasami wystarczy samo obranie jabłka ze skórki, aby było dobrze tolerowane.
Leczenie alergii pokarmowej u dorosłych i u dzieci
Współczesna medycyna odchodzi od modelu opartego wyłącznie na pasywnym unikaniu alergenów na rzecz aktywnych strategii terapeutycznych, które mają na celu zwiększenie bezpieczeństwa pacjenta i poprawę jakości jego życia. Kluczowym elementem leczenia, niezależnie od wieku, pozostaje edukacja w zakresie rozpoznawania wczesnych objawów anafilaksji oraz bezwzględna konieczność posiadania przy sobie adrenaliny w autostrzykawce. Jest ona lekiem pierwszego rzutu, który jako jedyny potrafi skutecznie odwrócić groźne dla życia objawy wstrząsu, podczas gdy leki przeciwhistaminowe i sterydy pełnią jedynie funkcję pomocniczą w łagodzeniu objawów skórnych czy późnych reakcji zapalnych.
U dzieci priorytetem jest dążenie do indukcji trwałej tolerancji pokarmowej. Układ odpornościowy najmłodszych pacjentów wykazuje dużą plastyczność, co lekarze wykorzystują, wprowadzając coraz częściej immunoterapię doustną. Polega ona na podawaniu precyzyjnie odmierzonych, stopniowo zwiększanych dawek alergenu pod ścisłym nadzorem specjalisty. Celem tej metody nie zawsze jest całkowite wyleczenie, ale podniesienie tzw. progu reaktywności, co chroni dziecko przed gwałtowną reakcją po przypadkowym spożyciu śladowych ilości produktu, na przykład w szkole czy w przedszkolu.
W przypadku alergii na mleko lub jajka u dzieci często stosuje się metodę „drabiny pokarmowej”, polegającą na stopniowym wprowadzaniu produktów poddanych silnej obróbce termicznej, które są zazwyczaj lepiej tolerowane i pomagają organizmowi szybciej „wyrosnąć” z alergii.
U osób dorosłych sytuacja wygląda inaczej, ponieważ alergie nabyte w dojrzałym wieku (np. na skorupiaki, ryby czy orzechy) rzadko ustępują samoistnie i częściej wiążą się z ryzykiem ciężkich reakcji ogólnoustrojowych. Leczenie u dorosłych skupia się przede wszystkim na rygorystycznej diecie eliminacyjnej oraz identyfikacji i unikaniu tzw. kofaktorów.
Najnowsze badania podkreślają, że u dorosłych przebieg reakcji zależy w ogromnej mierze od czynników dodatkowych, takich jak wysiłek fizyczny, spożycie alkoholu, stres czy przyjmowanie leków z grupy NLPZ, które mogą drastycznie obniżyć próg tolerancji na alergen. Przełomem w terapii obu grup wiekowych stało się wprowadzenie leczenia biologicznego, np. przeciwciał monoklonalnych (omalizumab), które „wyciszają” odpowiedź immunologiczną i stanowią dodatkowy parasol ochronny dla pacjentów z grup wysokiego ryzyka.
>> Sprawdź też: Jak wzmocnić układ immunologiczny u dorosłych i dzieci?
Zakończenie
Alergia pokarmowa to złożony problem zdrowotny, którego nie należy lekceważyć. Dynamiczny rozwój alergologii molekularnej sprawiła, że dzisiejsi pacjenci mają dostęp do diagnostyki o niespotykanej dotąd precyzji. Identyfikacja konkretnych cząsteczek uczulających pozwala na zaplanowanie bezpiecznego postępowania terapeutycznego – od dopasowanej diety eliminacyjnej, przez ocenę ryzyka anafilaksji, aż po skuteczną immunoterapię. Wczesne wykrycie i monitorowanie alergii pod okiem specjalistów pozwala na minimalizację ryzyka i znaczną poprawą komfortu życia osób z alergią.
Alergia pokarmowa – sekcja FAQ
Nieleczona alergia pokarmowa może prowadzić do przewlekłych stanów zapalnych, niedożywienia, a przede wszystkim do ryzyka wystąpienia zagrażającej życiu reakcji anafilaktycznej.
Czas trwania alergii zależy to od alergenu. Alergia na mleko często mija w dzieciństwie, natomiast uczulenie na orzechy czy ryby zazwyczaj pozostaje na całe życie.
Stolec przy alergii pokarmowej może być luźny, zawierać domieszkę śluzu lub krwi, a u dzieci często występują bolesne odparzenia okolicy odbytu.
Obecnie podstawowym postępowaniem terapeutycznym w przypadku alergii pokarmowych jest dieta eliminacyjna. W niektórych przypadkach pod nadzorem lekarza stosuje się próby doustnej immunoterapii.
Alergię pokarmową można pomylić przede wszystkim z nietolerancją pokarmową (np. laktozy), zatruciem pokarmowym albo celiakią.
W celu diagnostyki alergii należy udać się do alergologa, który zleci testy skórne, oznaczenie przeciwciał IgE z surowicy lub precyzyjną diagnostykę molekularną (np. test ALEX).
Piśmiennictwo
- HundS.K., Sampath V., ZhouX. i in. Scientific developments in understanding food allergy prevention, diagnosis, and treatment. Front Immunol, 2025, 22, 16, 572283,
- Peters R.L., Krawiec M., Koplin J.J i in. Update on food allergy. Pediatr Allergy Immunol, 2021 Jan 21;32(4):647–657,
- TednerS.G., AsarnojA., Thulin H. i in. Food allergy and hypersensitivity reactions in children and adults-A review. J Intern Med., 2022, 291(3), 283-302,
- BarthaI., AlmulhemN., Santos A.F. Feast for thought: A comprehensive review of food allergy 2021-2023. J Allergy Clin Immunol, 2024, 153(3), 576-594.