Rumień guzowaty to najczęstsze schorzenie należące do zapaleń tkanki podskórnej. Jak wygląda rumień guzowaty? Z jakimi jednostkami chorobowymi jest powiązany? Czy rumień guzowaty może być objawem gruźlicy? Jak leczy się to schorzenie? Przeczytaj poniższy artykuł i dowiedz się więcej na temat rumienia guzowatego.
Spis treści:
- Co to jest rumień guzowaty?
- Jakie są przyczyny rumienia guzowatego?
- Objawy rumienia guzowatego
- Rumień guzowaty u dzieci
- Rumień guzowaty w ciąży
- Jak leczyć rumień guzowaty?
- FAQ. Rumień guzowaty – często zadawane pytania
- Rumień guzowaty – podsumowanie
Co to jest rumień guzowaty?
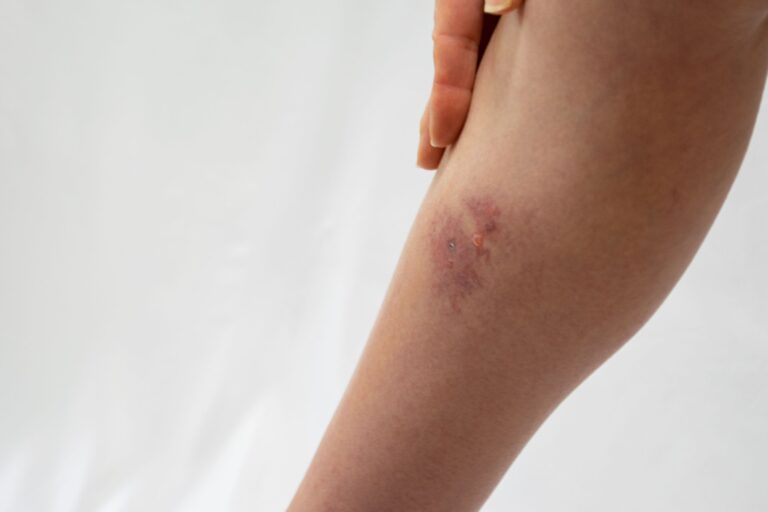
Rumień guzowaty (erythema nodosum) to schorzenie zapalne dotyczące tkanki podskórnej, które w literaturze medycznej bywa określane jako reakcja nadwrażliwości na różnego rodzaju antygeny. Pierwszy opis choroby został wykonany przez Roberta Willana w 1798 roku. Schorzenie to najczęściej pojawia się u kobiet w wieku rozrodczym. Istotą schorzenia jest pojawienie się bolesnych guzów, które mają zazwyczaj 1-6 cm i cechują się wzmożonym uciepleniem. Zmiany te lokalizują się najczęściej na podudziach, jednak mogą również pojawić się w obrębie kostek, ud, czy przedramion.
Jakie są przyczyny rumienia guzowatego?
W etiopatogenezie rumienia guzowatego kluczową rolę odgrywa reakcja nadwrażliwości na bodźce antygenowe, która prowadzi do odkładania się kompleksów immunologicznych w obrębie naczyń krwionośnych przegród tkanki podskórnej. W obrębie tkanki podskórnej mogą pojawiać się nacieki neutrofilowe, a także reaktywne formy tlenu, czego konsekwencją jest uszkodzenie komórek i rozwój stanu zapalnego. Rumień guzowaty jest wiązany z wieloma schorzeniami współistniejącymi i często określany jako objaw innej przypadłości. Stany kliniczne i choroby, które mogą objawiać się jako rumień guzowaty to przede wszystkim:
- infekcje bakteryjne – w tym najczęściej wywołane przez paciorkowce,
- grzybice układowe,
- infekcje wirusowe – w tym spowodowane przez cytomegalowirusa, czy wirusa Epsteina-Barr (EBV),
- infekcje pasożytnicze – w tym wywoływane przez pierwotniaka Giardia lamblia,
- gruźlica,
- sarkoidoza,
- wirusowe zapalenie wątroby typu B i C,
- przyjmowanie niektórych leków – w tym najczęściej sulfonamidów, doustnych leków antykoncepcyjnych, penicylin, jodków i bromków,
- choroba Leśniowskiego-Crohna,
- choroba Behçeta,
- wrzodziejące zapalenie jelita grubego,
- okres ciąży,
- zespół Sweeta,
- nowotwory – w tym najczęściej ostra białaczka szpikowa i zespół Hodgkina, ale również guzy lite, w tym nowotwory złośliwe trzustki, żołądka, czy nerek.

Warto jednak podkreślić, że w około połowie przypadków (mimo przeprowadzonej diagnostyki) nie udaje się znaleźć czynnika wyzwalającego objawy rumienia guzowatego.
Objawy rumienia guzowatego
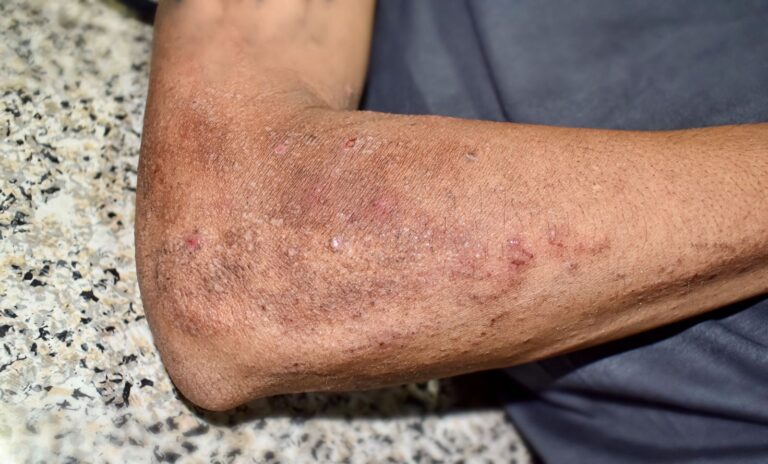
Klasycznym objawem rumienia guzowatego jest pojawienie się czerwonawych, niekiedy lekko brunatnych guzów zlokalizowanych w obrębie podudzi. Guzy te są słabo odgraniczone od niezmienionej chorobowo skóry i cechują się wzmożonym uciepleniem, a także bolesnością palpacyjną. Guzy są wykwitem, który typowo pozostawia po sobie blizny, jednak w przypadku rumienia guzowatego mamy do czynienia z wyjątkiem. W przebiegu tej jednostki chorobowej nie powstają blizny, lecz po guzach pozostają jedynie przebarwienia. Rumień guzowaty ma tendencję do samoograniczania się, guzy zanikają bowiem w ciągu 2-8 tygodni.
Zmianom na skórze mogą towarzyszyć jednak objawy dodatkowe takie jak:
- gorączka,
- osłabienie,
- ból głowy,
- dolegliwości żołądkowo-jelitowe,
- niekiedy powiększenie węzłów chłonnych,
- bóle mięśni i stawów,
- obrzęk stawów – najczęściej skokowych, kolanowych i nadgarstkowych.
Rozpoznanie rumienia guzowatego stawiane jest na podstawie prezentowanego przez pacjenta obrazu klinicznego. Konieczne jest wykonanie RTG klatki piersiowej w celu poszukiwania znamion sarkoidozy. W diagnostyce przydatne są również takie badania laboratoryjne jak:
- stężenie białka CRP,
- oznaczenie OB,
- morfologia krwi obwodowej,
- oznaczenie antygenu HbS, przeciwciał anty-HCV,
- badania serologiczne, w tym oznaczenie przeciwciał w kierunku antygenów drobnoustrojów – na przykład w kierunku zakażenia Mycoplasma pneumoniae,
- niekiedy badania w kierunku gruźlicy, w tym test Quantiferon,
- oznaczenie ASO (miano antystreptolizyny) – badanie wykonywane jest w kierunku identyfikacji infekcji paciorkowcowej,
- badania kału w kierunku pasożytów i G. lamblia.


Rumień guzowaty u dzieci
Rumień guzowaty występuje również w populacji pediatrycznej. W tym przypadku przyczyną objawów są przede wszystkim infekcje, w tym wywołane przez:
- paciorkowce,
- bakterie z rodzaju Mycoplasma,
- bakterie z rodzajuSalmonella, Yersinia,
- wirusy – w tym adenowirusy, wirus EBV, Cytomegalowirus.
Rumień guzowaty u dzieci może również być manifestacją reakcji poszczepiennej. W przypadku wystąpienia zmian skórnych, które mogą odpowiadać rumieniowi guzowatemu, należy pilnie skonsultować się ze swoim pediatrą.
Rumień guzowaty w ciąży
Okres ciąży wiąże się z większym ryzykiem wystąpienia rumienia guzowatego. Wynika to między innymi z wahań stężenia hormonów, a mianowicie estrogenów i progesteronu. Zmiany te mogą wpływać na układ immunologiczny ciężarnej i pobudzać makrofagi, a także limfocyty T do produkcji interleukin prozapalnych (w tym przede wszystkim IL-10, I L-6). Jednak rumień guzowaty w ciąży może być również manifestacją kliniczną innych schorzeń, co sprawia, że ciąża nie zwalania z przeprowadzenia odpowiedniej diagnostyki.
Jak leczyć rumień guzowaty?
Leczenie rumienia guzowatego opiera się na terapii choroby podstawowej, o ile czynnik wywołujący został zidentyfikowany w badaniach. Poza tym w leczeniu objawowym tej jednostki chorobowej stosuje się między innymi:
- niesteroidowe leki przeciwzapalne (naproksen, indometacyna),
- doustne glikokortykosteroidy,
- dapson,
- niekiedy leki immunosupresyjne, w tym cyklosporynę, metotreksat,
- antybiotykoterapię – w przypadku infekcji bakteryjnej.
W leczeniu miejscowym zastosowanie znajdują okłady w taniny (działanie przeciwzapalne), a także miejscowe glikokortykosteroidy w postaci kremu lub maści.
FAQ. Rumień guzowaty – często zadawane pytania
Rumień guzowaty to jednostka chorobowa o złożonych przyczynach, nic więc dziwnego, że rodzi wśród pacjentów wiele pytań. Poniżej odpowiedzi na najczęstsze z nich.
Rumień guzowaty może być objawem infekcji bakteryjnych, wirusowych, jak i grzybiczych, ale również reakcją na przyjmowanej leki, czy objawem schorzeń ogólnoustrojowych, w tym gruźlicy, sarkoidozy, czy też zapalnych schorzeń jelit. Pojawienie się rumienia guzowatego wymaga wnikliwej diagnostyki laboratoryjnej, jak i obrazowej.
Sam niedobór żelaza nie jest czynnikiem spustowym do pojawienia się objawów rumienia guzowatego. Należy mieć jednak świadomość, że obniżenie stężenia hemoglobiny i niedobór żelaza może być związany ze schorzeniami towarzyszącymi rumieniowi guzowatemu, w tym gruźlicy, nowotworom złośliwym, schorzeniom autoimmunologicznym, a także zapalnym chorobom jelit.
Rumień guzowaty nie jest schorzeniem, które typowo prowadzi do choroby zakrzepowo-zatorowej. Jednak w niektórych przypadkach stan kliniczny pacjenta z rumieniem guzowatym może sprzyjać incydentom zakrzepowym. Zwiększone ryzyko zakrzepicy występuje między innymi w przypadku:
– unieruchomienia chorego, na przykład na skutek silnych dolegliwości bólowych w obrębie kończyn dolnych,
– ciąży,
– otyłości,
– współistnienia schorzeń przewlekłych, w tym infekcji, czy schorzeń zapalnych jelit.
Konieczność profilaktyki przeciwzakrzepowej (na przykład pod postacią podawania podskórnie heparyny) powinna zostać oceniona i wprowadzona przez lekarza.
Rumień guzowaty powinien być różnicowany z takimi jednostkami chorobowymi jak:
– rumień stwardniały,
– guzkowe zapalenie tętnic,
– zapalenie tkanki podskórnej w przebiegu niedoboru alfa-1-antytrypsyny,
– toczeń rumieniowaty głęboki,
– zakrzepowe zapalenie naczyń żylnych kończyn dolnych.
Rumień guzowaty może towarzyszyć zarówno schorzeniom infekcyjnym, zapalnym, jak autoimmunologicznym. Może również współistnieć ze stanami fizjologicznymi, takimi jak na przykład ciąża. W wielu przypadkach nie udaje się jednak powiązać objawów rumienia guzowatego z żadną jednostką chorobową. Wówczas schorzenie ma charakter idiopatyczny.
Rumień guzowaty ma charakter samoograniczający. Aby zapobiegać nawrotom choroby, konieczne jest leczenie schorzenia podstawowego pod opieką lekarza.
Rumień guzowaty – podsumowanie
- Rumień guzowaty to schorzenie dotyczące tkanki podskórnej, które objawia się typowo pod postacią bolesnych, czerwonych guzów pojawiających się w obrębie kończyn dolnych.
- Rumień guzowaty może współistnieć z wieloma jednostkami chorobowymi, w tym schorzeniami infekcyjnymi, zapalnymi i onkologicznymi.
- Diagnostyka rumienia guzowatego obejmuje poszukiwanie ewentualnych schorzeń współistniejących i obejmuje zarówno badania laboratoryjne, jak i również obrazowe.
- Leczenie rumienia guzowatego powinno dotyczyć nie tylko objawów choroby, ale również schorzenia podstawowego.
- Objawy rumienia guzowatego wymagają pilnej konsultacji lekarskiej, a w wielu przypadkach również hospitalizacji.
Bibliografia
- M. Chowaniec i inni, Erythema Nodosum – review of the literature. Reumatologia 2016; 54(2): 79-82,
- A. Olejnik, Rumień guzowaty w przebiegu półpaśca twarzy – wyzwania terapeutyczne na podstawie opisu przypadku, Dermatologia Praktyczna, Wydawnictwo Czelej, 2024,
- M. Wolska-Wasińska, A. Całka, Rumień guzowaty – o czym należy pamiętać w trakcie diagnostyki? Analiza Przypadków Pediatria, Wydawnictwo PZWL, 2022,
- M. Potempa-Jeziorowska i inni, Erythema nodosum – complicated way to get the cause. Forum Medycyny Rodzinnej 2018; 12(6): 234-241,
- C. De Simone i inni, Clinical, histopathological, and immunological evaluation of a series of patients with erythema nodosum. Int J Dermatol 2016; 55(5): e289-e294.