Chłoniak Hodgkina, nazywany również ziarnicą złośliwą, to nowotwór układu limfatycznego, który charakteryzuje się obecnością specyficznych komórek (tzw. Reed-Sternberga). Wczesne wykrycie choroby znacząco zwiększa szanse na skuteczne leczenie i długotrwałą remisję.
Dowiesz się, jakie są metody diagnozowania, leczenia oraz rokowania w zależności od stopnia zaawansowania choroby. Poniższe krótkie kompendium wiedzy umożliwi Ci rozpoznawanie, kiedy należy się zbadać – cóż ratuje lepiej niż wiedza?
Spis treści:
- Czym jest chłoniak Hodgkina?
- Chłoniak Hodgkina – objawy
- Chłoniak Hodgkina – objawy u dzieci
- Przyczyny zachorowania na chłoniaka Hodgkina
- Stadia chłoniaka Hodgkina i ich charakterystyka
- Diagnostyka chłoniaka Hodgkina
- Jak przebiega i ile trwa leczenie chłoniaka Hodgkina?
- Chłoniak Hodgkina – rokowania
- Chłoniak Hodgkina – często zadawane pytania (FAQ)
- Chłoniak Hodgkina – podsumowanie
Czym jest chłoniak Hodgkina?
Chłoniak Hodgkina to nowotwór wywodzący się z układu chłonnego, w którym dochodzi do niekontrolowanego rozrostu zmienionych nowotworowo limfocytów B. Charakterystyczną cechą tego typu chłoniaka jest obecność patologicznych komórek Reed-Sternberga, które można wykryć w badaniu histopatologicznym.
Choroba najczęściej dotyka młodych dorosłych (20-30 lat) oraz osoby po 55. roku życia. Wyróżnia się dwa główne typy chłoniaka Hodgkina:
- klasyczny chłoniak Hodgkina (95% przypadków), który dzieli się na podtypy: stwardnienie guzowate, postać mieszanokomórkowa z przewagą limfocytów oraz z zanikiem limfocytów,
- chłoniak Hodgkina z przewagą limfocytów (5% przypadków), który ma łagodniejszy przebieg.
Chłoniak Hodgkina jest jednym z najlepiej rokujących nowotworów układu limfatycznego, a wczesne rozpoznanie pozwala na skuteczne leczenie.
>> Przeczytaj: Najczęstsze nowotwory u kobiet i mężczyzn
Chłoniak Hodgkina – objawy
Objawy chłoniaka Hodgkina można podzielić na dwie główne grupy:
- miejscowe (związane z powiększeniem węzłów chłonnych),
- ogólnoustrojowe.
Wczesne symptomy mogą być niespecyficzne, co utrudnia szybką diagnozę. Poniżej omówiamy te najważniejsze z nich.
>> Sprawdź też: Powiększone węzły chłonne na szyi – przyczyny, objawy i diagnostyka
Najbardziej charakterystyczne objawy miejscowe chłoniaka Hodgkina
Do najczęstszych objawów miejscowych należą:
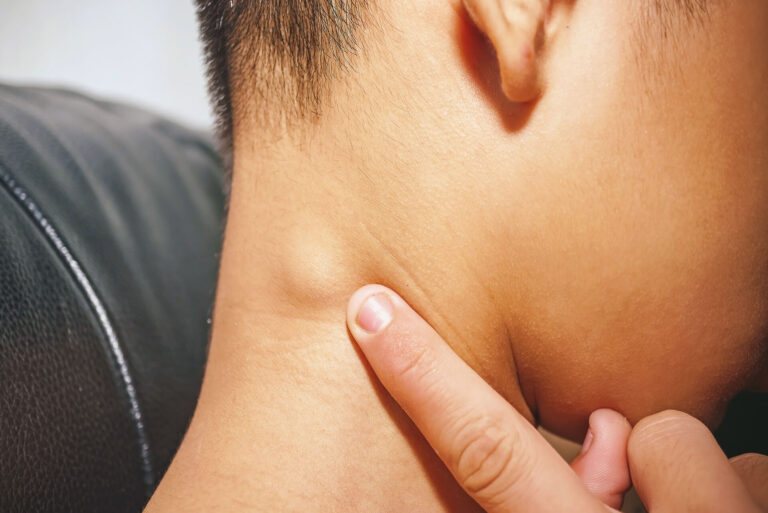
- powiększone węzły chłonne – najczęściej w okolicy szyi, pach lub pachwin; są one niebolesne, twarde i mogą stopniowo powiększać się.
- ucisk na sąsiednie narządy – powiększone węzły mogą uciskać drogi oddechowe (duszność, kaszel) lub żyły (obrzęk twarzy i szyi).
- powiększenie śledziony (splenomegalia) i/lub wątroby (hepatomegalia) – występuje w bardziej zaawansowanych stadiach.
>> Zobacz: Objawy chorej wątroby. Na co zwrócić uwagę i jakie badania wykonać?
Ogólne objawy chłoniaka Hodgkina
Do objawów ogólnoustrojowych (tzw. objawów B) zalicza się:
- gorączkę (powyżej 38°C), bez wyraźnej przyczyny,
- nocne poty – intensywne, zmuszające do zmiany piżamy lub pościeli,
- utratę masy ciała (jako punkt odniesienia przyjmuje się wartość straty ponad 10% masy w ciągu 6 miesięcy),
- świąd skóry – u niektórych pacjentów występuje uporczywe swędzenie,
- zmęczenie i osłabienie.
Obecność tych objawów może wskazywać na bardziej agresywny przebieg choroby.
>> Przeczytaj też: Ciągłe zmęczenie – problem XXI wieku. Czy to może być objaw choroby?
Chłoniak Hodgkina – objawy u dzieci
U dzieci chłoniak Hodgkina objawia się podobnie jak u dorosłych, jednak mogą wystąpić dodatkowe symptomy:
- bóle brzucha (związane z powiększeniem wątroby lub śledziony),
- zahamowanie wzrostu,
- częstsze infekcje z powodu osłabienia układu odpornościowego.
Dzieci zwykle lepiej odpowiadają na leczenie, a rokowania są korzystniejsze niż u dorosłych.
>> To może Cię zainteresować: Jak wzmocnić układ immunologiczny u dorosłych i dzieci?
Przyczyny zachorowania na chłoniaka Hodgkina
Etiologia choroby nie jest w pełni poznana, ale wyróżnia się kilka czynników ryzyka:
- zakażenie wirusem Epsteina-Barr (EBV) – u części pacjentów stwierdza się związek z przebytą mononukleozą,
- osłabienie układu odpornościowego (np. u osób z HIV lub po przeszczepach),
- czynniki genetyczne – występowanie chłoniaka w rodzinie zwiększa ryzyko zachorowania,
- wiek i płeć – częściej chorują mężczyźni oraz osoby w wieku 20-30 i po 55. roku życia.
Stadia chłoniaka Hodgkina i ich charakterystyka
Stopień zaawansowania choroby określa się wg klasyfikacji Ann Arbor:
I stadium chłoniaka Hodgkina
Nowotwór obejmuje jedną grupę węzłów chłonnych lub jeden narząd poza węzłami. Rokowanie jest bardzo dobre, a wyleczalność przekracza 90%.
II stadium chłoniaka Hodgkina
Zmiany występują w dwóch lub więcej grupach węzłów chłonnych po tej samej stronie przepony (np. szyja i pachy). Leczenie jest skuteczne, ale wymaga intensywniejszej terapii niż w I stadium.
Chłoniak Hodgkina – III stadium
Choroba zajmuje węzły chłonne po obu stronach przepony (np. szyja i pachwiny). Może występować zajęcie śledziony lub innych narządów limfatycznych.
>> Zobacz: Układ limfatyczny człowieka – budowa, funkcje, najczęstsze choroby
Chłoniak Hodgkina – IV stadium
Nowotwór rozprzestrzenia się poza węzły chłonne (np. do szpiku kostnego, wątroby, płuc). Jest to najbardziej zaawansowane stadium, wymagające agresywnego leczenia.

Diagnostyka chłoniaka Hodgkina
Proces diagnostyczny obejmuje:
- badanie fizykalne (ocena węzłów chłonnych, śledziony, wątroby) – element kluczowy, każdorazowo nie może zostać zaniedbany.
- biopsję węzła chłonnego – kluczowe badanie potwierdzające obecność komórek Reed-Sternberga.
- badania obrazowe (TK, PET, RTG klatki piersiowej) – ocena stopnia zaawansowania.
- badanie szpiku kostnego – w celu wykluczenia zajęcia układu krwiotwórczego.
- badania dodatkowe: morfologia z rozmazem, glukoza na czczo, elektrolity (sód, potas), mocznik, kwas moczowy, dehydrogenaza mleczanowa, koagulogram.
>> Morfologię krwi zrobisz w ALAB laboratoria – sprawdź zakres pakietu:

Jak przebiega i ile trwa leczenie chłoniaka Hodgkina?
Leczenie zależy od stadium choroby i obejmuje:
- chemioterapię (najczęściej schemat ABVD lub BEACOPP),
- radioterapię – stosowana miejscowo, szczególnie w I i II stadium,
- immunoterapię (np. przeciwciała monoklonalne anty-CD30),
- przeszczep szpiku – w przypadku nawrotów.
Terapia trwa zwykle 4-6 miesięcy, a w zaawansowanych przypadkach nawet rok.
Chłoniak Hodgkina – rokowania
Rokowania zależą od stadium:
- I-II stadium – wyleczalność sięga 90%.
- III stadium – 5-letnie przeżycie wynosi 70-80%.
- IV stadium – szanse na remisję to 50-60%.
Warto dodać, iż nawroty występują u ok. 10-15% pacjentów.
Chłoniak Hodgkina – często zadawane pytania (FAQ)
Tak, chłoniak Hodgkina jest jednym z najbardziej uleczalnych nowotworów, zwłaszcza przy wczesnym wykryciu.
Nie. Rak to nowotwór pochodzący z tkanki nabłonkowej; niemniej chłoniak Hodgkina to rodzaj nowotworu złośliwego układu limfatycznego.
Pierwsze objawy to zwykle powiększone, niebolesne węzły chłonne, gorączka, nocne poty i nieuzasadniona utrata masy ciała.
Morfologia może wykazać nieprawidłowości (np. podwyższone OB, niedokrwistość), ale do diagnozy konieczne są dokładniejsze badania.
Rokowania zależą od typu i stadium chłoniaka, ale np. w przypadku chłoniaka Hodgkina 5-letnie przeżycie przekracza 80–90%.
Chłoniak Hodgkina – podsumowanie
Chłoniak Hodgkina to nowotwór układu limfatycznego, który wcześnie wykryty daje bardzo dobre rokowania. Kluczowe jest zwracanie uwagi na objawy, takie jak powiększone węzły chłonne, gorączka czy nocne poty. Jeśli zauważasz u siebie niepokojące symptomy, nie zwlekaj – zgłoś się do lekarza, internisty w przypadku dorosłego i pediatry w przypadku dziecka. Im wcześniejsze rozpoznanie, tym lepsze rokowanie.
Źródła:
- Ansell SM. Hodgkin lymphoma: 2025 update on diagnosis, risk-stratification, and management. Am J Hematol. 2024 Dec;99(12):2367-2378. doi: 10.1002/ajh.27470. Epub 2024 Sep 6. PMID: 39239794., https://onlinelibrary.wiley.com/doi/10.1002/ajh.27470 (dostęp: 25.06.2025).
- Momotow J, Borchmann S, Eichenauer DA, Engert A, Sasse S. Hodgkin Lymphoma-Review on Pathogenesis, Diagnosis, Current and Future Treatment Approaches for Adult Patients. J Clin Med. 2021 Mar 8;10(5):1125. doi: 10.3390/jcm10051125. PMID: 33800409; PMCID: PMC7962816., https://pmc.ncbi.nlm.nih.gov/articles/PMC7962816 (dostęp: 25.06.2025).
- Shanbhag S, Ambinder RF. Hodgkin lymphoma: A review and update on recent progress. CA Cancer J Clin. 2018 Mar;68(2):116-132. doi: 10.3322/caac.21438. Epub 2017 Dec 1. PMID: 29194581; PMCID: PMC5842098., https://pmc.ncbi.nlm.nih.gov/articles/PMC5842098 (dostęp: 25.06.2025).
- Che Y, Ding X, Xu L, Zhao J, Zhang X, Li N, Sun X. Advances in the treatment of Hodgkin’s lymphoma (Review). Int J Oncol. 2023 May;62(5):61. doi: 10.3892/ijo.2023.5509. Epub 2023 Apr 7. PMID: 37026506; PMCID: PMC10147096., https://pmc.ncbi.nlm.nih.gov/articles/PMC10147096 (dostęp: 25.06.2025).
- Classic Hodgkin Lymphoma: The LYSA pragmatic guidelines Rossi, Cédric et al. European Journal of Cancer, Volume 213, 115073 https://www.ejcancer.com/article/S0959-8049(24)01204-8/fulltext (dostęp: 25.06.2025).