Osoby, które skarżą się na nawracające bóle brzucha i problemy z wypróżnianiem często przypisują swoje dolegliwości „drażliwym jelitom”. Czy słusznie? Dowiedz się, czym jest zespół jelita drażliwego i jakie badania są konieczne do postawienia diagnozy.
Spis treści:
- Co to jest zespół jelita drażliwego? Jak często występuje?
- Diagnostyka zespołu jelita drażliwego
- Badania laboratoryjne w diagnostyce zespołu jelita nadwrażliwego
- Zespół jelita nadwrażliwego – objawy
- Zespół jelita drażliwego – zmiany mikrobioty jelitowej (dysbioza)
- Kolonoskopia w zespole jelita nadwrażliwego
- Leczenie zespołu jelita nadwrażliwego
Co to jest zespół jelita drażliwego? Jak często występuje?
Zespół jelita nadwrażliwego (czasem zwany zespołem jelita drażliwego lub z ang. IBS – irritable bowel syndrome) jest zaburzeniem funkcji przewodu pokarmowego, w którym pacjent skarży się na nawrotowe bóle jelita grubego oraz problemy z wypróżnianiem.
IBS w przeszłości określany był jako zaburzenie czynnościowe i choroba psychosomatyczna. Obecnie wiemy, iż u jego podłoża leżą zaburzenia interakcji na osi jelito-mózg, a najważniejszą rolę w jego powstawaniu odgrywają bakterie jelitowe. Badania wskazują, iż nawet 50% pacjentów z zespołem jelita nadwrażliwego ma jakościowe i ilościowe zmiany w składzie mikrobioty jelitowej (dysbiozę).
Choroba występuje u ok. 11% populacji na świecie. Częściej u kobiet – 14%, wśród mężczyzn – 9%. Połowa pacjentów pierwsze objawy zgłasza przed 35. rokiem życia. Badania potwierdzają, iż udział w występowaniu choroby mają czynniki genetyczne, obserwuje się również częstsze występowanie zespołu jelita nadwrażliwego po przebyciu infekcji żołądkowo-jelitowej.
Diagnostyka zespołu jelita drażliwego
Zespół jelita drażliwego rozpoznaje się na podstawie wywiadu i objawów klinicznych pacjenta.
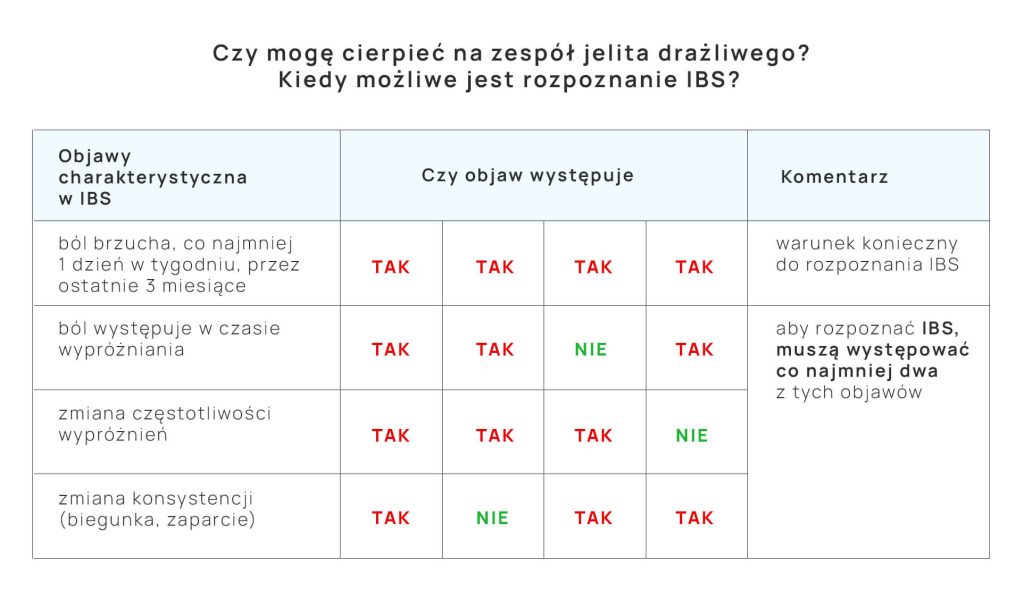
Aby można było postawić diagnozę, występujące symptomy muszą spełniać następujące kryteria:
- pacjent odczuwa nawracający ból brzucha, co najmniej jeden dzień w tygodniu, przez ostatnie 3 miesiące
- ból brzucha wiąże się z występowaniem co najmniej dwóch następujących czynników – występuje w czasie wypróżnienia, zmieniła się częstotliwość wypróżnień, zmieniła się konsystencja stolca.
W praktyce wyróżniamy kilka postaci (podtypów) IBS:
- IBS-D – z dominującą biegunką
- IBS-C – z dominującym zaparciem
- IBS-M – podtyp mieszany
- IBS-N – niesklasyfikowany.
Badania laboratoryjne w diagnostyce zespołu jelita nadwrażliwego
IBS jest chorobą, w której nie występują zmiany organiczne, dlatego nie ma badań laboratoryjnych potwierdzających tę chorobę. Ponieważ jednak objawy zespołu jelita nadwrażliwego przypominają objawy innych chorób przewodu pokarmowego, również tych, które mogą być groźne w skutkach dla pacjenta, zalecana jest diagnostyka laboratoryjna w celu wykluczenia tych chorób.
Jakie to badania i z jakiego powodu należy je zrobić?
- Morfologia – badanie krwi, w którym można stwierdzić występowanie niedokrwistości (anemii) z niedoboru żelaza, która może towarzyszyć nowotworom jelita grubego oraz celiakii. Dlatego stwierdzenie niedokrwistości (i leukocytozy) jest wskazaniem do pogłębienia diagnostyki.
- CRP – badanie wykonywane w celu stwierdzenia, czy w organizmie pacjenta nie toczy się stan zapalny. Badanie jest przydatne w różnicowaniu objawów IBS z nieswoistymi chorobami zapalnymi jelit, które mogą wywoływać podobne objawy (zwłaszcza niezaparciowe postacie IBS).
- Kalprotektyna w kale – marker stanu zapalnego jelit, który – podobnie jak CRP – pomaga w różnicowaniu z nieswoistymi chorobami zapalnymi jelit i pomaga w wykluczeniu np. choroby Leśniowskiego-Crohna. W wytycznych amerykańskich (American Collage of Gastroenteology) kalprotektyna może być zastąpiona laktoferyną w kale – ten parametr również pomaga ocenić, czy w jelitach nie występuje stan zapalny.
- TSH – podstawowe badanie funkcji tarczycy, które wykonuje się w celu wykluczenia nieprawidłowości funkcjonowania tego narządu. Zaburzenia pracy tarczycy mogą bowiem mieć związek z dolegliwościami brzusznymi, takimi jak zaparcia lub biegunki.
- Przeciwciała przeciwko transglutaminazie tkankowej w klasie IgA oraz badanie całkowitego IgA. Przeciwciała przeciwko transglutaminazie służą wykluczeniu choroby trzewnej (celiakii), która może objawiać się podobnymi symptomami jak IBS. Oznaczenie całkowitego IgA wykonuje się natomiast, ponieważ niedobór immunoglobulin klasy A jest najczęściej występującym niedoborem odporności i – jeśli mamy z nim do czynienia – badanie poziomu przeciwciał będzie fałszywie negatywne i utrudni prawidłowe rozpoznanie.
Jeśli przyczyną dolegliwości u badanego pacjenta jest zespół jelita drażliwego, wyniki wszystkich powyższych badań będą prawidłowe.

- Wodorowo-metanowy test oddechowy – SIBO – u pacjentów z IBS obserwuje się częste (30%) współwystępowanie SIBO, szczególnie jeśli zespół jelita nadwrażliwego ma postać biegunkową i przebiega ze wzdęciami. Dlatego u tych pacjentów należy wykonać badanie pomagające wykluczyć lub potwierdzić jego istnienie.
Uzupełnieniem diagnostyki IBS w uzasadnionych przypadkach może być wykonanie USG.

Zespół jelita nadwrażliwego – objawy
Zespół jelita nadwrażliwego jest chorobą przewlekłą, w której występują następujące objawy ze strony przewodu pokarmowego:
- nawracające bóle brzucha, mogą być związane z wypróżnieniem i odczuwane jako bolesne skurcze jelit;
- problemy z wypróżnieniem – biegunki lub zaparcia, lub zmienna konsystencja stolca. Należy podkreślić, iż u pacjentów z IBS zmienione stolce mogą występować na przemian ze stolcami prawidłowymi;
- wzdęcia brzucha, gazy, przelewania.
Obserwuje się, iż u 50-80% pacjentów istnieje zależność pomiędzy stresem a występowaniem i nasileniem tych objawów.
Inna grupa często występujących objawów to symptomy spoza układu pokarmowego:
- senność
- bóle głowy
- bóle pleców w odcinku lędźwiowym
- nocne oddawanie moczu
- częste i naglące oddawanie moczu
- zaburzenia miesiączkowania.
Objawy spoza przewodu pokarmowego nie mają znaczenia przy stawianiu rozpoznania, ale warto wiedzieć, że mogą towarzyszyć IBS, ponieważ mogą utrudniać i opóźniać diagnozę.
Zespół jelita drażliwego – zmiany mikrobioty jelitowej (dysbioza)
U ok. 50% pacjentów z IBS stwierdza się ilościowe oraz jakościowe zaburzenia w składzie mikrobioty (dysbiozę), u wielu z nich występuje SIBO – zespół przerostu bakteryjnego jelita cienkiego. Zmiany, które można obserwować u chorych z IBS to:
- zmniejszenie ilości bakterii z rodzaju Lactobacillus i Bifidobacterium
- zwiększenie ilości bakterii z rodzaju Streptococcus, E. coli, Clostridium spp
- zwiększenie ilości bakterii Firmicutes a zmniejszenie Bacteroidetes.
Kolonoskopia w zespole jelita nadwrażliwego
Zespół jelita nadwrażliwego jest chorobą, której objawy przypominają symptomy innych schorzeń układu pokarmowego, również tych, które mogą być dla pacjenta groźne w skutkach. W takich przypadkach – aby wykluczyć chorobę organiczną – wskazane byłoby wykonanie kolonoskopii. Jednak u pacjentów z IBS nie jest ona rekomendowana jako badania rutynowe.
Zalecenia mówią, aby w diagnostyce IBS kolonoskopia nie była wykonywana u osób w wieku poniżej 50 r.ż bez czynników ryzyka choroby organicznej (tabela poniżej).
Czynniki ryzyka choroby organicznej – sytuacje, w których powinna być wykonana kolonoskopia
| wiek | powyżej 50 lat |
| choroby w rodzinie | nowotwory jelita grubego, celiakia, nieswoiste choroby zapalne jelit |
| objawy | niezamierzona utrata masy ciała, występowanie objawów w nocy, wodobrzusze |
| badania laboratoryjne | niedokrwistość, zwiększona liczba białych krwinek |
Leczenie zespołu jelita nadwrażliwego
Leczenie IBS jest kilkuetapowe i obejmuje postępowanie niefarmakologiczne (wysiłek fizyczny oraz wsparcie psychologiczne, dietę, suplementację błonnika, stosowanie olejków z mięty pieprzowej oraz probiotyków) i stosowanie leków (eubiotyków, rozkurczowych, przeciwbiegunkowych lub zmniejszających zaparcie). Aby ustalić właściwe postępowanie, konieczne jest określenie objawu dominującego oraz rozpoznanie sytuacji, które nasilają objawy w celu modyfikacji stylu życia.
Postępowanie niefarmakologiczne:
- umiarkowany wysiłek fizyczny
- normalizacja masy ciała
- wsparcie psychologiczne w celu opracowania optymalnych sposobów radzenia sobie ze stresem
- dieta przy zespole jelita drażliwego – unikanie pokarmów, które szkodzą pacjentowi (modyfikacje indywidualne oparte na doświadczeniach pacjenta), dieta low-FOODMAP (z małą zawartością fermentujących cukrów prostych oraz polioli) – stosowana nie dłużej niż 6-8 tygodni, nie należy jej powtarzać, ponieważ pacjent nie odnosi korzyści z takiego postępowania, unikanie produktów wysoko przetworzonych
- stosowanie błonnika rozpuszczalnego w rekomendowanej dawce 10-25 g dobę, jego źródłem powinny być świeże warzywa i owoce, babka płesznik, babka lancetowata, babka jajowata, otręby owsiane. Pacjent z IBS powinien unikać błonnika nierozpuszczalnego (otręby pszenne, ziarna, orzechy, fasola, warzywa kapustne i korzeniowe) ponieważ może dodatkowo nasilać dolegliwości
- olejek z mięty pieprzowej – stosowanie preparatu w okresie od 2 do 12 tygodni
- probiotyki – powinny być stosowane z rozwagą, nie zaleca się stosowania probiotyków jako grupy, sugerowane jest stosowanie konkretnych szczepów probiotyków, które mają prawdopodobny korzystny wpływ na objawy IBS oraz modyfikują mikrobiotę jelitową.
Postępowanie farmakologiczne
Zgodnie z rekomendacjami Polskiego Towarzystwa Gastroenterologicznego oraz zaleceniami amerykańskimi w celu złagodzenia objawów stosuje się rifaksyminę. Lek jest podawany pacjentom z biegunką, bólami brzucha i wzdęciami, natomiast nie znajduje zastosowania u osób z zaparciami.
Pomocnicze znaczenie ma stosowanie leków rozkurczowych, jednak należy podkreślić, iż nie wszystkie leki z tej grupy są skuteczne u pacjentów z IBS, należy wybierać konkretne preparaty, których skuteczność została potwierdzona w zespole jelita nadwrażliwego.
Ważną grupą leków, która znajduje zastosowanie u pacjentów z IBS, są również leki przeciwdepresyjne (grupa trójpierścieniowych leków przeciwdepresyjnych) zmniejszające objawy bólowe.
Zespół jelita drażliwego to choroba przewlekła, która nie powoduje zmian organicznych w przewodzie pokarmowym. Ponieważ objawy choroby przypominają objawy innych chorób jelit, w postępowaniu diagnostycznym należy wykluczyć chorobę nowotworową, celiakię oraz nieswoiste choroby zapalne jelit. Leczenie drażliwości jelita jest wieloetapowe i obejmuje postępowanie zarówno farmakologiczne, jak i niefarmakologiczne. O poprawie i skuteczności leczenia świadczy zmniejszenie nasilenia objawów.
Przeczytaj też: Wpływ diety low-FODMAP na IBS