Martwica kości, znana również jako osteonekroza, to poważna choroba, która może prowadzić do trwałego uszkodzenia układu kostnego. W tym artykule wyjaśniamy, czym dokładnie jest martwica kości, jakie są jej przyczyny, objawy oraz jak wygląda proces leczenia. Dowiesz się także, czy martwica kości to rak i czy można ją całkowicie wyleczyć. Zadbaj o swoje zdrowie i dowiedz się, jak rozpoznać niepokojące objawy!
| Kluczowe informacje: >> Martwica kości (osteonekroza) to choroba polegająca na obumarciu tkanki kostnej wskutek niedokrwienia. >> Najczęściej dotyczy kości udowej, piszczelowej, piętowej oraz szczęki. >> Główne przyczyny to urazy, długotrwałe stosowanie kortykosteroidów, alkoholizm, choroby autoimmunologiczne i zaburzenia krzepnięcia. >> Objawy obejmują ból, ograniczoną ruchomość, obrzęk i deformacje stawów. >> W diagnostyce kluczową rolę odgrywają badania obrazowe (MRI, RTG) oraz badania laboratoryjne, takie jak morfologia krwi. >> Leczenie zależy od stadium – może być zachowawcze (odciążenie, farmakoterapia) lub chirurgiczne (np. endoprotezoplastyka). >> Wczesne rozpoznanie znacząco zwiększa szanse na zatrzymanie postępu choroby, a regularna kontrola zdrowia i unikanie czynników ryzyka to najlepsza forma profilaktyki. >> Martwicy kości można często zapobiec — nie ignoruj objawów i zgłoś się do lekarza przy pierwszych niepokojących dolegliwościach. |
Spis treści:
- Martwica kości: czym jest?
- Źródła martwicy kości: przyczyny rozwoju dolegliwości
- Objawy jałowej martwicy kości
- Diagnostyka martwicy kości: rozpoznanie
- Leczenie martwicy kości
- Czy można zapobiec rozwojowi martwicy kości?
- FAQ. Martwica kości – często zadawane pytania
Martwica kości: czym jest?
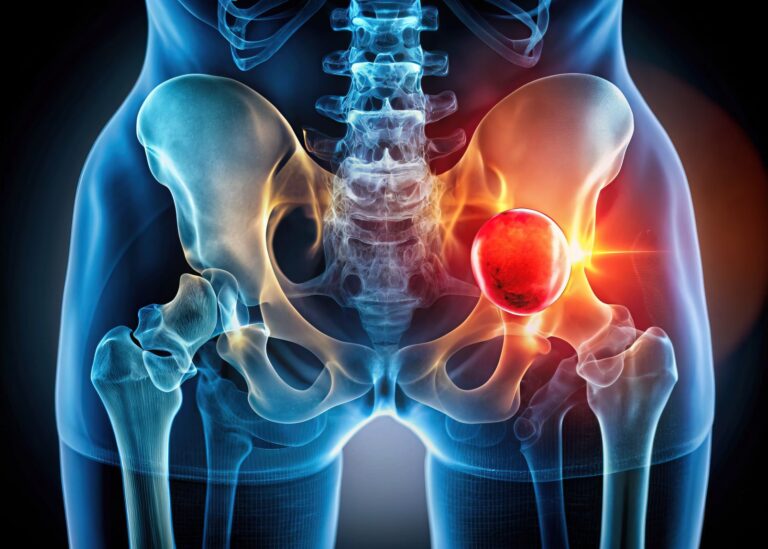
Martwica kości (osteonekroza) to stan, w którym dochodzi do obumarcia tkanki kostnej w wyniku zaburzenia ukrwienia. Brak dopływu krwi powoduje, że komórki kostne nie otrzymują tlenu ani substancji odżywczych, co prowadzi do ich śmierci. Wbrew częstym pytaniom — martwica kości to nie rak, choć nieleczona może prowadzić do poważnych komplikacji.
>> Zobacz: Nowotwór kości – objawy, przyczyny, badania i leczenie
Przebieg martwicy kości
Proces martwicy kości rozwija się stopniowo. Początkowo zmiany są niewidoczne w badaniach obrazowych, a objawy bywają niespecyficzne. W miarę postępu choroby dochodzi do osłabienia struktury kości, zapadnięcia się jej powierzchni i wtórnych uszkodzeń stawów. W zaawansowanych stadiach pacjent może utracić zdolność poruszania się i wymagać operacyjnego leczenia.
Źródła martwicy kości: przyczyny rozwoju dolegliwości
Do najczęstszych przyczyn martwicy kości należą:
- urazy mechaniczne (np. złamania),
- przewlekłe stosowanie glikokortykosteroidów,
- alkoholizm,
- choroby autoimmunologiczne,
- zaburzenia krzepnięcia,
- niedokrwistość sierpowatokrwinkowa,
- choroby zapalne i metaboliczne (np. toczeń rumieniowaty układowy).
>> Przeczytaj: Osteoporoza – cicha choroba kości
Objawy jałowej martwicy kości
Objawy martwicy mogą być różne w zależności od lokalizacji, ale najczęściej pojawiają się: ból w obrębie zajętej kości nasilający się podczas ruchu, ograniczona ruchomość w stawie, obrzęk i tkliwość, uczucie „chrupania” lub przeskakiwania w stawie.
Martwica kości udowej
Martwica głowy kości udowej to najczęstsza postać osteonekrozy. Choroba może dotyczyć jednej lub obu kończyn i prowadzi do zniszczenia stawu biodrowego. W zaawansowanym stadium konieczna bywa całkowita wymiana stawu.
Martwica kości piszczelowej
W tej postaci martwicy najczęściej dochodzi do uszkodzenia bliższej nasady kości piszczelowej, co prowadzi do bólu kolana, sztywności oraz trudności z poruszaniem się.
>> To może Cię zainteresować: Zapalenie okostnej: objawy, przyczyny, leczenie
Martwica kości piętowej
To rzadsza, ale bolesna forma choroby, która może znacznie utrudniać chodzenie. Najczęściej występuje po urazach lub przeciążeniach, np. u sportowców.
Martwica kości szczęki
Martwica szczęki często występuje jako powikłanie leczenia bisfosfonianami lub po zabiegach chirurgicznych w obrębie jamy ustnej. Objawia się bólem, obrzękiem i trudno gojącymi się ranami.
>> Zobacz: Choroba Pageta – objawy, przyczyny, diagnostyka i leczenie
Diagnostyka martwicy kości: rozpoznanie
Rozpoznanie martwicy kości opiera się na wywiadzie lekarskim, badaniu fizykalnym oraz badaniach obrazowych:
- RTG – przydatne w późniejszym stadium,
- rezonans magnetyczny (MRI) – najczulsza metoda diagnostyczna,
- tomografia komputerowa – pomocna w ocenie zaawansowania choroby.

Rola badań laboratoryjnych w rozpoznaniu martwicy kości
Chociaż badania laboratoryjne nie potwierdzają bezpośrednio martwicy kości, pomagają wykluczyć inne przyczyny objawów oraz wskazują na współistniejące choroby. Wśród zalecanych badań znajduje się:
- morfologia krwi – może wykazać objawy niedokrwistości lub stanu zapalnego,
- OB, CRP – markery stanu zapalnego,
- profil lipidowy – ocena ryzyka miażdżycy,
- badania układu krzepnięcia – przy podejrzeniu zakrzepicy.
>> To może Cię zainteresować: Zakrzepica żył głębokich – przyczyny, objawy, diagnostyka, leczenie
Leczenie martwicy kości
Leczenie zależy od stopnia zaawansowania choroby i obejmuje leczenie zachowawcze (ograniczenie obciążenia kończyny, leki przeciwbólowe i przeciwzapalne), farmakologiczne (np. leki poprawiające mikrokrążenie) i procedury chirurgiczne – od odciążenia (np. wiercenie odbarczające), po endoprotezoplastykę w zaawansowanym stadium.
Czy można zapobiec rozwojowi martwicy kości?
Tak. Zapobieganie polega na unikaniu nadużywania alkoholu, kontroli chorób przewlekłych, ograniczeniu stosowania steroidów, wczesnym leczeniu urazów i regularnym wykonywaniu badań profilaktycznych.
>> Przeczytaj: Zatrucie alkoholowe: objawy, przebieg, leczenie
FAQ. Martwica kości – często zadawane pytania
W tej części odpowiadamy na najczęściej zadawane pytania pacjentów dotyczące martwicy kości. Warto poznać odpowiedzi na wątpliwości, które pojawiają się najczęściej w gabinetach lekarskich i wyszukiwaniach internetowych.
Tak, w wielu przypadkach można zatrzymać rozwój choroby, zwłaszcza jeśli zostanie wcześnie wykryta. W zaawansowanych postaciach konieczne może być leczenie operacyjne.
Nie. Martwica kości to choroba zwyrodnieniowa, a nie proces nowotworowy.
Tak, nieleczona może prowadzić do trwałego kalectwa i zniszczenia stawów.
Zwiększone ryzyko złamań, deformacje kości, przewlekły ból i konieczność leczenia chirurgicznego.
Proces może rozwijać się miesiącami lub latami, w zależności od przyczyny i stopnia zaawansowania.
Zazwyczaj postępuje stopniowo, ale w niektórych przypadkach może mieć szybki przebieg – zwłaszcza przy dużym niedokrwieniu.
Bibliografia
- Lespasio MJ, Sodhi N, Mont MA. Osteonecrosis of the Hip: A Primer. Perm J. 2019
- Weinstein RS. Glucocorticoid-induced osteonecrosis. Endocrine. 2012
- Nogueira D, Caldas IM, Dinis-Oliveira RJ. Bisphosphonates and osteonecrosis of the jaws: Clinical and forensic aspects. Arch Oral Biol. 2023
- Zheng Y, Zheng Z, Zhang K, Zhu P. Osteonecrosis in systemic lupus erythematosus: Systematic insight from the epidemiology, pathogenesis, diagnosis and management. Autoimmun Rev. 2022