Artykuł powstał 24.10.2022 r., ostatnia aktualizacja: 21.04.2026 r.
Alergia na pyłki to najczęstsza postać alergii, która może pojawić się w każdym wieku. Objawy pyłkowicy, takie jak katar sienny, są dobrze znane. Jednak nie wszystkie symptomy alergii sezonowej kojarzą się z tym schorzeniem, trudności mogą pojawiać się zwłaszcza u dzieci. Jakie są objawy alergii na pyłki, jaki można ją zdiagnozować i jak się ją leczy?
| Z artykułu dowiesz się: >> jakie objawy mogą wskazywać na alergię sezonową, >> co powinno zwrócić uwagę w kierunku tej alergii u dzieci, >> dlaczego nowoczesna diagnostyka alergii jest ważna nie tylko dla jej prawidłowego rozpoznania, >> na czym polega odczulanie, >> jakie są warunki skutecznego odczulania. |
Spis treści:
- Czym jest alergia na pyłki?
- Jakie pyłki najbardziej uczulają?
- Objawy alergii na pyłki
- Objawy alergii na pyłki u dzieci i niemowląt
- Ile trwa alergia na pyłki i czy może się pojawić nagle?
- Diagnostyka alergii na pyłki
- Leczenie alergii na pyłki
- Odczulanie na pyłki – immunoterapia swoista
- Alergia na pyłki – czego nie jeść?
- Zakończenie
- FAQ: Alergia na pyłki – często zadawane pytania
Czym jest alergia na pyłki?
Alergia na pyłki to nadmierna reakcja układu immunologicznego na białka zawarte w pyłkach drzew, traw, chwastów. Dla większości ludzi pyłki roślin są nieszkodliwe, jednak układ odpornościowy pewnej grupy osób rozpoznaje je jako zagrożenie i zaczyna się przed nimi bronić, wytwarzając przeciwciała w klasie IgE. Efektem takiej aktywacji układu immunologicznego jest uwalnianie histaminy i mediatorów zapalenia, a co za tym idzie, występowanie alergicznego nieżytu nosa, alergicznego zapalenia spojówek, a u części pacjentów astmy alergicznej.
Symptomy alergii na pyłki występują w okresie pylenia drzew, traw i chwastów, czyli jest to schorzenie sezonowe. Badania wskazują, iż alergia sezonowa dotyczy – w zależności od źródeł – od 26 do 32% osób dorosłych i 20-27% dzieci, co czyni ją najczęstszym rodzajem alergii.
Objawy alergii na pyłki mogą się pojawiać w każdym momencie życia, częściej chorują kobiety (29%) niż mężczyźni (21%).
>> Sprawdź też: Nietolerancja histaminy czy alergia? Czym się różnią i dlaczego łatwo je pomylić?
Jakie pyłki najbardziej uczulają?
Przyczyną alergii na pyłki może być wiele roślin, ale najczęściej uczulają:
- drzewa – brzoza, olcha, leszczyna;
- trawy – żyto, tymotka;
- chwasty – bylica, ambrozja.
Pyłki drzew
Wśród pyłków drzew zdecydowanie najczęściej uczula pyłek brzozy, który w Polsce stanowi dominującą przyczynę alergicznego nieżytu nosa, zapalenia spojówek i astmy pyłkowej. Głównym alergenem brzozy jest komponenta Bet v 1.
Sezon pylenia brzozy rozpoczyna się z końcem marca i trwa do maja, a nawet do połowy czerwca. Niestety w wyniku reakcji krzyżowych, objawów możemy się spodziewać również w czasie pylenia leszczyny i olchy. Przy coraz cieplejszych zimach mogą one wystąpić już na początku stycznia.
Objawy alergii na pyłki brzozy pojawiają się nagle, co jest spowodowane bardzo wysokim stężeniem pyłków, szczególnie w pełni sezonu pylenia. Najczęstsze objawy to:
- wodnisty katar, kichanie, świąd w nosie,
- zapalenie spojówek – zaczerwienione oczy, łzawienie,
- duszność, napadowy kaszel, świszczący oddech.
Oprócz tych objawów brzoza jest istotną przyczyną występowania reakcji krzyżowych. U pacjentów z potwierdzoną alergią na pyłek brzozy – obecność Bet v 1 – może się rozwijać zespół alergii jamy ustnej (OAS), czyli krzyżowe uczulenie na:
- niektóre warzywa – marchew, seler,
- owoce – jabłka,
- orzechy ziemne,
- soję.
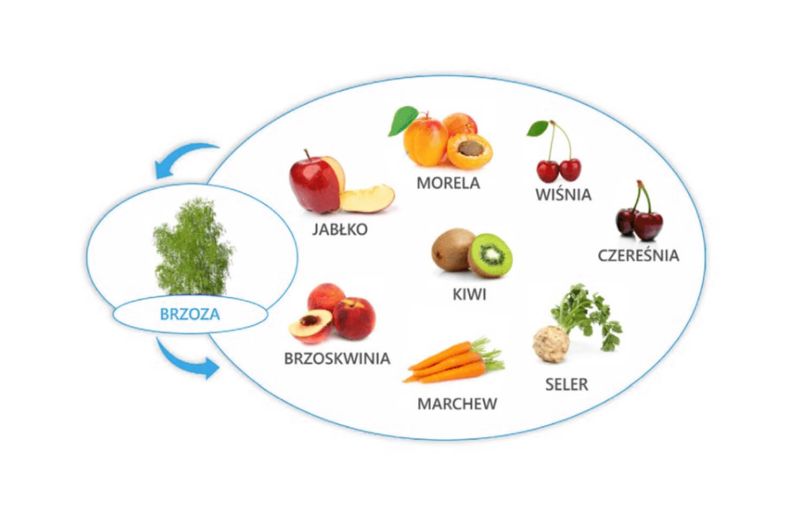
>> Zobacz: Alergia na pyłki drzew – co musisz wiedzieć i jak się chronić?

| To ważne: Lotne pyłki brzozy mogą przemierzać z wiatrem duże odległości. Badania wskazują, iż brzozy rosnące w pobliżu ruchliwych dróg wydzielają więcej alergenów, niż drzewa rosnące daleko od tras z dużym ruchem samochodów. |
Pyłki traw
Trawy są ważnym źródłem alergenów wziewnych. Sezon ich pylenia zaczyna się zazwyczaj z końcem maja i może trwać aż do września. Dominującą przyczyną pyłkowicy jest tymotka łąkowa, a jej główny alergen to rPhl p 1, występuje u ponad 95% osób z uczuleniem na trawy.
Jakie objawy towarzyszą alergii na pyłki traw? Otóż:
- wodnisty katar,
- zaczerwienione i łzawiące oczy,
- problemy z oddychaniem,
- zaostrzenia astmy.
Podobnie jak pyłek brzozy, tymotka również może być przyczyną reakcji krzyżowych i zespołu alergii jamy ustnej (OAS).
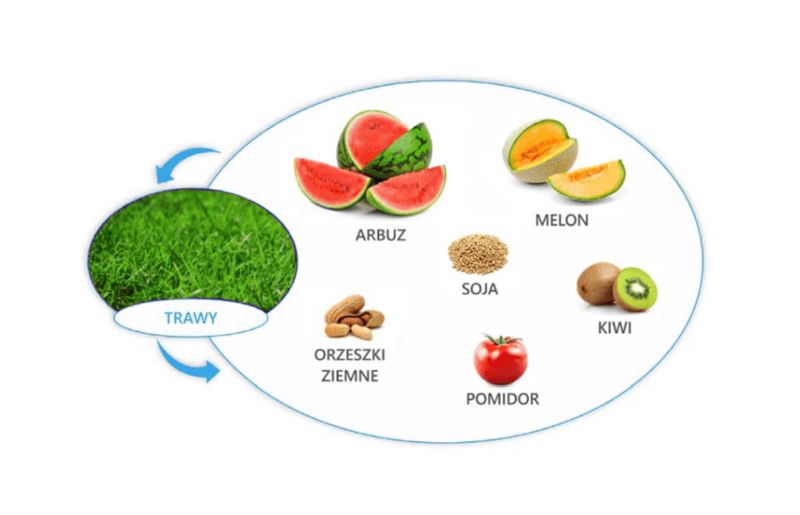
>> Zobacz: Alergia na pyłki traw. Objawy i leczenie alergii na trawy

Pyłki chwastów
Sezon pylenia chwastów w zależności od regionu zaczyna się z końcem czerwca i może trwać aż do początku października. Główną przyczyną objawów w tym okresie dla osób uczulonych są rośliny z rodziny astrowatych, do których należą:
- bylica,
- ambrozja,
- słonecznik,
- złocień maruna.
Dwa najpowszechniej występujące gatunki chwastów to bylica pospolita i ambrozja, które stanowią również najczęstszą przyczynę alergii sezonowej na chwasty. Głównym alergenem bylicy jest Art. V 1.
| Pamiętaj: Główną przyczyną pyłkowicy późnego lata w Polsce jest bylica pospolita. |
Jakie objawy mogą świadczyć o uczuleniu na pyłki chwastów? Można zaobserwować:
- katar sienny w postaci obfitej, wodnistej wydzieliny,
- ograniczona drożność nosa,
- utrudnione oddychanie,
- podrażnienia, zaczerwienienia i łzawienie oczu,
- zapalenie spojówek.
Zarówno bylica, jak i ambrozja mają również swój udział w objawach spowodowanych reaktywnością krzyżową. Najpoważniejsze reakcje krzyżowe mogą występować pomiędzy:
- bylica – rumianek;
- bylica – słonecznik;
- bylica – brzoskwinia, ale także jabłko, gruszka, melon, banan;
- bylica – koper włoski, ale także marchew, seler.
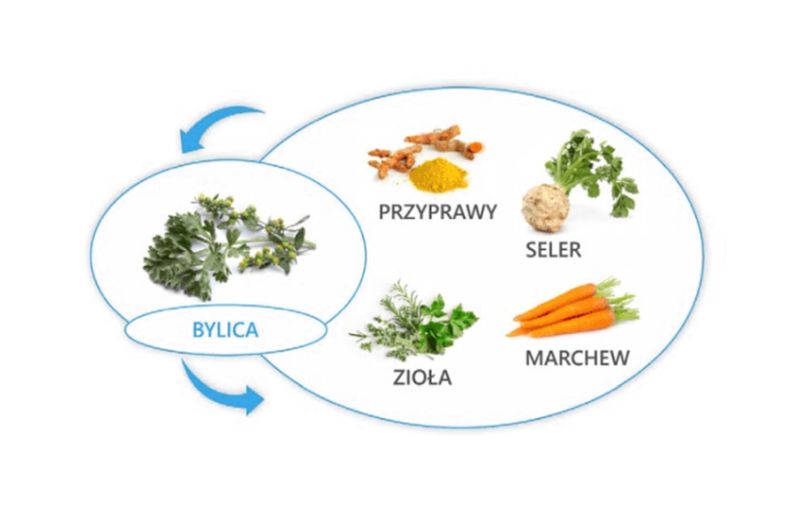
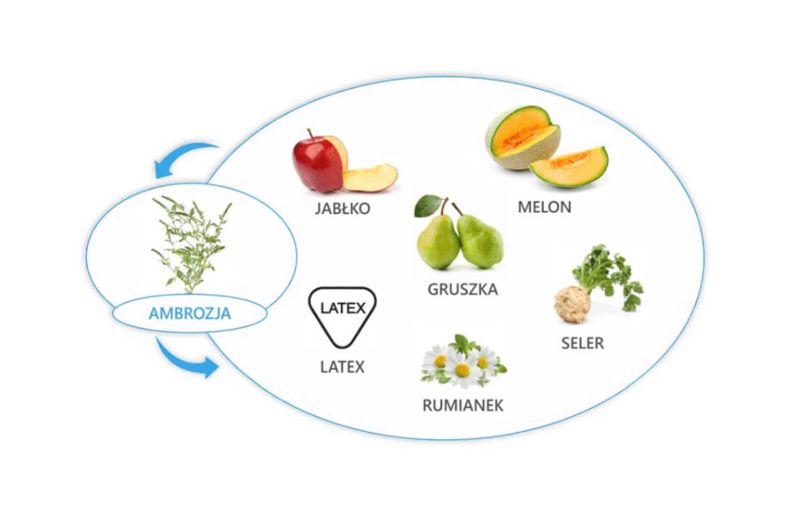

>> Dowiedz się więcej z artykułu: Alergia na pyłki chwastów – jak ją wykryć i na jakie rośliny uważać?
Objawy alergii na pyłki
Objawy alergii na pyłki to najczęściej dolegliwości ze strony nosa, oczu, skóry, a także dróg oddechowych. Ich nasilenie zwykle rośnie przy wysokim stężeniu pyłków (ciepło, sucho, wietrznie), a zmniejsza się po ograniczeniu ekspozycji (np. po powrocie do domu, umyciu twarzy, zmianie ubrania). Część z tych symptomów to dolegliwości rzadziej kojarzone z alergią, bywają mylone z przeziębieniem lub innymi schorzeniami.
>> Sprawdź: Jak sobie radzić z alergią na pyłki? Wywiad z dr. Dąbrowieckim
Alergia na pyłki – objawy ze strony nosa
Nos jest pierwszą linią kontaktu z pyłkami unoszącymi się w powietrzu. Błona śluzowa nosa nieustannie filtruje wdychane powietrze, co sprawia, że to właśnie w jamie nosowej gromadzi się najwięcej cząstek alergenowych, a najbardziej typowe objawy alergii sezonowej to symptomy kataru siennego. Należą do nich:
- wodnisty katar – wydzielina jest przejrzysta i płynna, w odróżnieniu od gęstej, żółtozielonej wydzieliny towarzyszącej infekcjom bakteryjnym,
- napadowe kichanie – często seryjne, powtarzające się wielokrotnie, szczególnie po wyjściu na zewnątrz w dni o wysokim stężeniu pyłków,
- uporczywe swędzenie nosa – pacjenci odruchowo pocierają nos, co u dzieci przyjmuje charakterystyczną postać tzw. „salutowania alergicznego”,
- uczucie zatkanego nosa i gorsza drożność – obrzęk błony śluzowej powoduje blokadę przepływu powietrza, zmuszając do oddychania przez usta,
- spływanie wydzieliny po tylnej ścianie gardła (co sprzyja chrząkaniu i kaszlowi).
W odróżnieniu od infekcji wirusowej objawy alergiczne zwykle nie wiążą się z gorączką i wyraźnym „rozbiciem”. Charakterystyczne bywa też to, że dolegliwości nasilają się po wyjściu na zewnątrz w czasie pylenia, a słabną po ograniczeniu kontaktu z alergenem.
Alergia na pyłki – objawy ze strony oczu
Oczy, podobnie jak nos, są bezpośrednio narażone na kontakt z pyłkami. Wilgotna powierzchnia spojówek łatwo absorbuje cząstki alergenów, wywołując miejscową reakcję zapalną. Typowe są:
- świąd i pieczenie oczu – uczucie bywa tak dokuczliwe, że pacjenci odruchowo pocierają oczy, co nasila objawy,
- intensywne łzawienie – szczególnie przy wietrznej i słonecznej pogodzie,
- zaczerwienienie spojówek – oczy wyglądają na przekrwione i podrażnione,
- uczucie piasku pod powiekami,
- światłowstręt i dyskomfort przy patrzeniu.
Częstym problemem w alergii na pyłki są także opuchnięte oczy, co jest szczególnie widoczne w godzinach porannych. Występujący zazwyczaj obrzęk powiek może jeszcze nasilać się po spacerze, wietrzeniu mieszkania w środku dnia czy po przebywaniu w miejscach o wysokim zapyleniu (łąki, parki). Jeśli obrzęk narasta gwałtownie lub towarzyszą mu duszność czy obrzęk warg/języka, wymaga pilnej oceny lekarskiej.
| Warto wiedzieć: Zapalenie spojówek o podłożu alergicznym dotyczy aż 90% pacjentów z alergią pyłkową. |
Objawy skórne alergii na pyłki
Alergia skórna na pyłki to zjawisko, które wielu pacjentów zaskakuje. Powszechnie panuje przekonanie, że pyłki podrażniają wyłącznie nos i oczy. Tymczasem skóra – jako narząd pokryty warstwą lipidową – również łatwo absorbuje pyłki. Zmiany zwykle dotyczą miejsc odsłoniętych: twarzy, szyi, dłoni, przedramion, czasem łydek.
Objawy skórne alergii pyłkowej obejmują:
- świąd skóry – szczególnie w miejscach nieosłoniętych odzieżą, narażonych na bezpośredni kontakt z pyłkami,
- zaczerwienienie i podrażnienie – skóra twarzy, szyi, dekoltu i rąk może reagować rumieniem i pieczeniem,
- drobne grudki lub wysypkę,
- zaostrzenie istniejących zmian skórnych – u pacjentów z atopowym zapaleniem skóry sezon pylenia często przynosi wyraźne pogorszenie. Szczególnie dotyczy to osób uczulonych na pyłek brzozy, u których przez większość roku zmiany skórne są pod kontrolą, a w kwietniu i na początku maja, gdy stężenie pyłków brzozy w powietrzu jest najwyższe, dochodzi do zaostrzenia zarówno ze strony dróg oddechowych, jak i skóry.
| To ważne: Swędzenie skóry może być objawem alergii wziewnej na pyłki. |
Inne objawy alergii na pyłki
Poza opisanymi wyżej symptomami, alergia pyłkowa może dawać objawy mniej oczywiste, które bywają pomijane lub błędnie interpretowane. Do częstych należą:
- kaszel – jest to jedno z najczęściej pomijanych powikłań alergii pyłkowej. Tymczasem alergeny, które drażnią oczy i nos, wpadają również do płuc. Kaszel pojawiający się po wyjściu z domu w piękną, wietrzną pogodę może być objawem alergicznym, a nie skutkiem przeziębienia,
- świszczący oddech, uczucie ucisku w klatce piersiowej, duszność – objawy sugerujące sezonową astmę lub podrażnienie oskrzeli,
- świąd gardła i podniebienia, drapanie w gardle, uczucie obrzęku gardła, ból gardła – należy pamiętać, że pyłki roślin gromadzą się również w jamie ustnej i gardle. Dolegliwości są czasami tak dokuczliwe, że bywają mylone z anginą, jednak w alergii przebiegają bez gorączki, a nasilają się po wyjściu na świeże powietrze,
- dyskomfort podczas przełykania,
- gorszy sen i zmęczenie wynikające z przewlekłych dolegliwości.
>> Może Cię zainteresować: Kaszel alergiczny – objawy. Jak odróżnić kaszel alergiczny od przeziębienia?
Alergia na pyłki – objawy po spożyciu niektórych pokarmów
U ok. 30% osób występuje także zespół pyłkowo‑pokarmowy (reakcje krzyżowe). Pacjent uczulony na pyłek brzozy może po spożyciu surowego jabłka, gruszki, brzoskwini, moreli, selera, marchewki, soi czy orzechów odczuwać świąd warg i języka, dyskomfort przy przełykaniu, a w cięższych przypadkach nawet objawy ze strony przewodu pokarmowego. Dzieje się tak, ponieważ główny alergen brzozy (Bet v 1) jest pod względem chemicznym niemal identyczny z białkami zawartymi w tych pokarmach. Co istotne, reakcje te dotyczą surowych, nieprzetworzonych produktów – upieczone jabłko czy kompot z gruszki zazwyczaj nie wywołują objawów, ponieważ obróbka termiczna niszczy strukturę uczulającego białka.
Objawy alergii na pyłki u dzieci i niemowląt
U dzieci alergia bywa mylona z „ciągłymi infekcjami”, zwłaszcza u maluchów chodzących do żłobka lub przedszkola. Warto rozważyć tło alergiczne, jeśli:
- dziecko bardzo często choruje,
- katar i objawy ze strony dróg oddechowych „nie reagują na antybiotyki” lub leki używane standardowo w leczeniu infekcji,
- katar i kichanie powracają sezonowo,
- objawy przebiegają bez gorączki i bez pogorszenia samopoczucia,
- dolegliwości nasilają się po spacerze i łagodnieją w domu,
- pojawia się przewlekły kaszel, szczególnie na zewnątrz,
- wcześniejsze leczenie „na infekcję” nie przynosi poprawy.
U małych dzieci pojawiają się objawy podobne jak u dorosłych, ale mogą również dominować nieco inne symptomy:
- oddychanie przez usta i chrapanie w nocy (z powodu obrzęku błony śluzowej nosa),
- ciemne cienie pod oczami (tzw. „alergiczne sińce”),
- drażliwość, problemy ze snem i trudności z koncentracją,
- pogorszenie apetytu.
| Pamiętaj: Objawy alergii na pyłki u dzieci i niemowląt są często mylone z infekcjami. |
Ile trwa alergia na pyłki i czy może się pojawić nagle?
Czas trwania objawów zależy przede wszystkim od tego, na jakie pyłki pacjent jest uczulony oraz od kalendarza pylenia w danym regionie. Osoba uczulona wyłącznie na pyłek brzozy będzie odczuwać dolegliwości głównie w kwietniu i na początku maja – czyli przez kilka tygodni. Natomiast pacjent uczulony jednocześnie na pyłki drzew, traw i chwastów może zmagać się z objawami nawet przez kilka miesięcy, od wczesnej wiosny aż do jesieni. U osób uczulonych na wiele alergenów jednocześnie, w tym roztocza kurzu domowego, objawy mogą utrzymywać się praktycznie przez cały rok z wyraźnym zaostrzeniem w sezonie pylenia.
Objawy alergii na pyłki mogą pojawić się nagle, a ich gwałtowny początek jest zazwyczaj związany z początkiem intensywnego pylenia. Może również wystąpić sytuacja, gdy po latach niewielkich dolegliwości organizm osiągnie większą wrażliwość na alergen. Wówczas chory może odczuwać początek okresu pylenia jako bardzo uciążliwy.
Warto również zdawać sobie sprawę, że alergia sezonowa może rozwinąć się w każdym wieku. Osoba, która przez 30 czy 40 lat nie miała żadnych problemów w sezonie pylenia, pewnego dnia może zacząć odczuwać typowe objawy alergiczne. Pierwszy kontakt z alergenem to faza wyprodukowania przeciwciał, dopiero przy kolejnych ekspozycjach dochodzi do pełnoobjawowej reakcji alergicznej. Jest to proces, który może przez lata zachodzić bezobjawowo, dlatego symptomy mogą się pojawiać również u osób dorosłych.
Diagnostyka alergii na pyłki
Rozpoznanie opiera się na połączeniu objawów (zwłaszcza ich sezonowości) i identyfikacji konkretnego alergenu w badaniach. W diagnostyce alergii sezonowej stosuje się:
- testy skórne punktowe (prick) z alergenami wziewnymi,
- oznaczanie swoistych IgE przeciwko konkretnym alergenom – zaletą tego badania jest możliwość wykonania go w każdym wieku – od niemowląt po osoby starsze. Nie wymaga odstawiania leków antyhistaminowych (co jest konieczne przed testami skórnymi) i może być wykonane nawet u pacjentów ze zmianami skórnymi uniemożliwiającymi testy prick.
- diagnostykę molekularną (komponentową), która pomaga ustalić, na jakie białka alergenowe organizm reaguje (szczególnie przy reakcjach krzyżowych i planowaniu immunoterapii).
- w wybranych sytuacjach testy prowokacyjne – najczęściej ma to miejsce gdy zarówno testy skórne, jak i badania z krwi dają wyniki ujemne, a objawy kliniczne jednoznacznie wskazują na alergię. Dotyczy to tak zwanego miejscowego alergicznego nieżytu nosa, w którym przeciwciała zlokalizowane są wyłącznie w błonie śluzowej narządu docelowego (np. nosa czy oka) i nie są wykrywalne standardowymi metodami. Testy prowokacyjne, np. naśluzówkowe, w połowie takich przypadków potwierdzają alergię.
>> Zobacz również: IgE całkowite – o czym świadczy wynik i w jakim celu przeprowadza się badanie?
Diagnostyka molekularna alergii na pyłki
Diagnostyka molekularna (komponentowa) stanowi najnowocześniejsze i najbardziej precyzyjne narzędzie diagnostyczne. W odróżnieniu od standardowych testów, które badają reakcję na cały ekstrakt alergenowy, diagnostyka molekularna pozwala zidentyfikować konkretne białko (komponent) odpowiedzialne za uczulenie. Pojedynczy alergen, na przykład pyłek brzozy, zawiera kilka różnych komponentów alergenowych – wiedza o tym, który z nich wywołuje reakcję, ma kluczowe znaczenie dla:
- planowania odczulania – pozwala ocenić, czy będzie ono skuteczne, ponieważ nie wszystkie komponenty równie dobrze poddają się immunoterapii,
- oceny ryzyka reakcji krzyżowych i identyfikacji komponentów anafilaktogennych – pozwala przewidzieć, na jakie pokarmy pacjent może reagować i jak poważna może być ta reakcja.
Od jakiego wieku można wykonywać badania z krwi w kierunku alergii?
Badania z krwi można wykonać już u bardzo małych dzieci. Jeśli są objawy i istnieje uzasadnione podejrzenie alergii nie ma „sztywnego” wieku, od którego diagnostyka jest możliwa.
Leczenie alergii na pyłki
Leczenie alergii pyłkowej opiera się na trzech filarach:
- unikaniu alergenu,
- farmakoterapii łagodzącej objawy,
- immunoterapii swoistej jako jedynej metody przyczynowej.
Ograniczanie kontaktu z pyłkami
Profilaktyka i unikanie alergenu stanowi ważny element leczenia, chociaż nie jest to łatwe. Praktyczne zalecenia obejmują:
- śledzenie kalendarza pylenia i komunikatów o stężeniu pyłków,
- rozpoczęcie przyjmowania leków antyhistaminowych dwa tygodnie przed spodziewanym początkiem sezonu pylenia,
- wietrzenie mieszkania wcześnie rano lub późno wieczorem, gdy emisja pyłków jest najniższa,
- po powrocie do domu: zmiana odzieży, prysznic, umycie włosów, wypłukanie nosa, oczu i gardła w celu usunięcia pyłków osadzonych na skórze i błonach śluzowych,
- w dni o wysokim stężeniu pyłków ograniczenie czasu spędzanego na zewnątrz, zamykanie okien,
- korzystanie z filtrów powietrza.
Leki łagodzące objawy alergii
Leczenie objawowe alergii polega na podawaniu:
- leków przeciwhistaminowych,
- preparatów donosowych oraz kropli do oczu – w zależności od występujących objawów,
- przy kaszlu i objawach oskrzelowych konieczna jest ocena pod kątem astmy i wdrożenie odpowiedniego leczenia wziewnego.
Odczulanie na pyłki – immunoterapia swoista
Odczulanie to metoda leczenia przyczynowego polegająca na stopniowym podawaniu alergenu w kontrolowanych dawkach w celu wywołania tolerancji. Terapia trwa zwykle 3-5 lat i może prowadzić do długotrwałego zmniejszenia objawów, a u części pacjentów do wieloletniej poprawy po zakończeniu leczenia. Immunoterapię kwalifikuje się indywidualnie po potwierdzeniu alergenu i ocenie wskazań oraz bezpieczeństwa. Najlepszym okresem na jej wdrożenie jest okres jesienno-zimowy.
| To ważne: Odczulanie to metoda leczenia alergii, polegająca na podawaniu kontrolowanych dawek alergenu. Efektem takiego postępowania jest „oduczenie” organizmu pacjenta nadwrażliwego i nadmiernego reagowania na pyłki. |
Immunoterapia to proces rozłożony na 3, a optymalnie na 5 lat; krótsze leczenie nie zapewnia trwałego efektu immunologicznego. U ok. 90% pacjentów poddanych odczulaniu uzyskuje się trwałe zmniejszenie objawów lub ich całkowite ustąpienie. Leki podaje się z formie iniekcji podskórnych, kropli podjęzykowych lub tabletek podjęzykowych. Terapię można rozpocząć u dzieci od ukończenia 5. roku życia, nie ma górnej granicy wieku pacjentów, u których można ją zastosować.
Odczulanie na pyłki – warunki skuteczności immunoterapii
Aby immunoterapia swoista (SIT) była skuteczna, ważne jest wykrycie, która molekuła, czyli białko wchodzące w skład alergenu, jest rzeczywiście odpowiedzialne za alergię. Poznanie uczulającego alergenu jest możliwe dzięki diagnostyce komponentowej, która – oprócz ustalenia źródła alergii – pozwala na przewidzenie, czy długoletni proces odczulania będzie skuteczny.
| Warto wiedzieć: Nie każdy alergen powodujący uczulenie, jest odpowiedni do procesu odczulania. Poznanie białka, które rzeczywiście powoduje alergię, jest kluczowe dla powodzenia terapii i jest to możliwe dzięki diagnostyce molekularnej. |
Immunoterapia swoista (SIT) na pyłki drzew
W przypadku alergii na pyłki brzozy, warunkiem skutecznej immunoterapii jest wykrycie cząsteczki Bet v1. Można to zrobić, wykonując pakiet badań SKUTECZNE ODCZULANIE NA PYŁKI DRZEW (metoda ImmunoCAP). W skład pakietu wchodzą badania:
- rBet v1 – wynik pozytywny wskazuje na obecność przeciwciał względem Bet v1 i prawdziwe uczulenie na pyłek brzozy. Stanowi wskazanie do immunoterapii swoistej na pyłki drzew
- rBet v2 + rBet v4 – wynik pozytywny wskazuje na obecność przeciwciał względem r Bet v2 + rBet v4 i wskazuje na fakt, iż prawdziwą przyczyną uczulenia nie jest brzoza, lecz inne pyłki – traw lub chwastów. Skuteczność odczulania na pyłki drzew w tym przypadku będzie niska.
Odczulanie na pyłki traw
W przypadku alergii na pyłki traw, warunkiem skutecznej immunoterapii jest wykrycie cząstek rPhlp 1 i Phl p5b. U około 11% pacjentów uczulonych na pyłek tymotki nie występuje żaden z tych alergenów, co wiąże się z niską skutecznością procesu odczulania.
Aby dowiedzieć się, czy u danego pacjenta immunoterapia będzie efektywna, należy zrobić badania z pakietu SKUTECZNE ODCZULANIE NA PYŁKI TRAW (metoda ImmunoCAP). W skład pakietu wchodzą:
- rPhl p1, rPhl p5b – wynik pozytywny świadczy o obecności przeciwciał przeciwko tym cząstkom białek i wskazuje na prawdziwe uczulenie na pyłek tymotki; jednocześnie jest informacją, iż odczulanie na pyłki traw będzie skuteczne.
- rPhl p7, rPhl p12 – wynik pozytywny tylko w tych dwóch klasach przeciwciał wskazuje, iż prawdziwą przyczyną uczulenia na pyłki nie są trawy, dlatego immunoterapia swoista na pyłki traw nie będzie skuteczna.
Odczulanie na pyłki chwastów
W przypadku alergii na pyłki chwastów, skuteczna immunoterapia jest możliwa, jeśli białkiem wywołującym uczulenie jest nArt v 1 w bylicy lub nAmb a 1 w ambrozji. Odpowiednie badania są zawarte w pakiecie SKUTECZNE ODCZULANIE NA PYŁKI CHWASTÓW (metoda ImmunoCAP):
- nAmb a 1 – dodatni wynik w tej grupie przeciwciał wskazuje na prawdziwe uczulenie na pyłek ambrozji i świadczy o tym, iż stanowi wskazanie do odczulania;
- nArt v 1 – obecność przeciwciał względem tej komponenty alergenowej świadczy o prawdziwym uczuleniu na pyłek bylicy i stanowi wskazanie do odczulania;
- nArt v 3 – obecność przeciwciał tylko przeciw Art v 3 wskazuje na niskie prawdopodobieństwo skuteczności odczulania na pyłek bylicy. Dodatkowo Art v 3 może wykazywać reakcję krzyżową z alergenami Pru p 3 brzoskwini lub Cor a 8 orzecha laskowego, dlatego wskazana jest dalsza diagnostyka w celu wykrycia prawdziwego źródła uczulenia;
- rPhl p7, rPhl p12 – dodatni wynik tylko tych przeciwciał przeciwko komponentom tymotki wskazuje na niskie prawdopodobieństwo skuteczności immunoterapii na pyłki traw lub chwastów, wskazana jest dalsza diagnostyka w celu poszukiwania źródła alergii.
Alergia na pyłki – czego nie jeść?
Niektóre pyłki drzew, traw czy chwastów wywołują reakcje krzyżowe z owocami, warzywami czy orzechami. Nie ma uniwersalnych rad jakich pokarmów unikać w przypadku np. uczulenia na pyłek brzozy czy traw, ponieważ różne ich komponenty reagują z różnymi pokarmami. Dlatego zawsze należy ustalić indywidualny profil uczuleniowy, który będzie wskazówką czego unikać w diecie.
Przykładowo osoby uczulone na:
- pyłek brzozy powinny unikać niektórych warzyw (marchew, seler), niektórych owoców (jabłka), orzechów ziemnych, soi, itp.,
- pyłek traw powinny unikać produktów mącznych (zwłaszcza pszenicy), ale także niektórych warzyw czy owoców,
- pyłek chwastów powinny unikać niektórych owoców (brzoskwinia, jabłko, gruszka, melon, banan), warzyw (koper włoski, marchew, seler), słonecznika, rumianku.
Dokładne wskazówki dietetyczne dla osoby uczulonej są możliwe do sformułowania po wykonaniu diagnostyki molekularnej.
Zakończenie
Alergia na pyłki to dokuczliwa dolegliwość, która może mieć duży wpływ na komfort życia pacjenta. W przypadku tej choroby bardzo ważna jest precyzyjna diagnostyka, która wskaże prawdziwe źródło alergii, pokaże potencjalne źródło alergii krzyżowych oraz odpowie na pytanie, czy odczulanie w danym przypadku będzie skuteczne.
FAQ: Alergia na pyłki – często zadawane pytania
W przypadku alergii objawy nasilają się po wyjściu z domu i ekspozycji na pyłki, natomiast po powrocie do domu, wzięciu kąpieli i wypłukaniu nosa odczuwamy wyraźną ulgę. Przy przeziębieniu takiej zależności nie ma – objawy utrzymują się niezależnie od miejsca przebywania, towarzyszą im gorączka, bóle mięśniowe i ogólne złe samopoczucie. Co więcej, w alergii szybką poprawę przynoszą leki antyhistaminowe, natomiast w infekcji wirusowej nie obserwujemy takiego efektu.
Samoistne ustąpienie alergii zdarza się dosyć rzadko. Znacznie skuteczniejszą drogą do uwolnienia się od objawów jest immunoterapia swoista (odczulanie), która pozwala uzyskać wieloletnią remisję. Po 3-5-letnim cyklu odczulania pacjent może być bezobjawowy przez kolejne 5, 8, a nawet 10 lat. Nie oznacza to jednak, że alergia zniknęła na zawsze – u części osób objawy mogą z czasem powrócić.
U osób uczulonych na pyłki bardzo częste jest współwystępowanie astmy. Badania szacują, że ponad 40% pacjentów uczulonych na pyłki choruje na astmę.
Piśmiennictwo
- Dąbrowiecki P., Jak sobie radzić z alergią na pyłki? Webinar dla ALAB laboratoria, 2023 https://www.alab.pl/centrum-wiedzy/alergia-na-pylki-wywiad-z-dr-dabrowieckim/ (dostęp: 12.03.2026).
- STANDARDY W ALERGOLOGII pod redakcją Jerzego Kruszewskiego, Marka L. Kowalskiego, Marka Kulusa, Polskie Towarzystwo Alergologiczne, Termedia Wydawnictwa Medyczne, Poznań 2019, Wydanie III uaktualnione
- Matricardi PM et al. EAACI Molecular Allergology User’s Guide. Pediatric allergy and immunology: official publication of the European Society of Pediatric Allergy and Immunology. 2016;27 Suppl 23:1-250. doi: 10.1111/pai.12563. PMID: 27288833
- Alina Gherasim, Thibaut Riff, Frank Dietsch, Florian Odul, Nathalie Domis, Hubert Mechin, Frederic de Blay, Relevance of an allergic patients database for determining pollen-induced asthma prevalence rates, Journal of Allergy and Hypersensitivity Diseases, Volume 6, 2025, 100043,ISSN 2950-3124, https://doi.org/10.1016/j.jahd.2025.100043. (dostęp: 12.03.2026).
- https://www.cdc.gov/nchs/pressroom/releases/20230126.html?CDC_AAref_Val=https://www-cdc-gov.translate.goog/nchs/pressroom/nchs_press_releases/2022/20220126.htm?_x_tr_sl=en&_x_tr_tl=pl&_x_tr_hl=pl&_x_tr_pto=sge (dostęp: 12.03.2026).
- https://www.aaaai.org/about/news/for-media/allergy-statistics (dostęp: 12.03.2026).