Anemia sierpowata to rzadka choroba w Polsce, jednak niebezpieczna i nieuleczalna. Dowiedz się, kogo może dotknąć, jak się objawia i jak przebiega leczenie.
Spis treści:
- Anemia (niedokrwistość) sierpowata – co to jest?
- Dziedziczenie niedokrwistości sierpowatokrwinkowej
- Anemia sierpowata – objawy
- Anemia sierpowata a malaria – jakie jest powiązanie?
- Anemia sierpowata – diagnostyka. Jakie badania wykonuje się w kierunku diagnozy?
- Anemia sierpowata – leczenie
- Anemia sierpowa – podsumowanie
Anemia (niedokrwistość) sierpowata – co to jest?
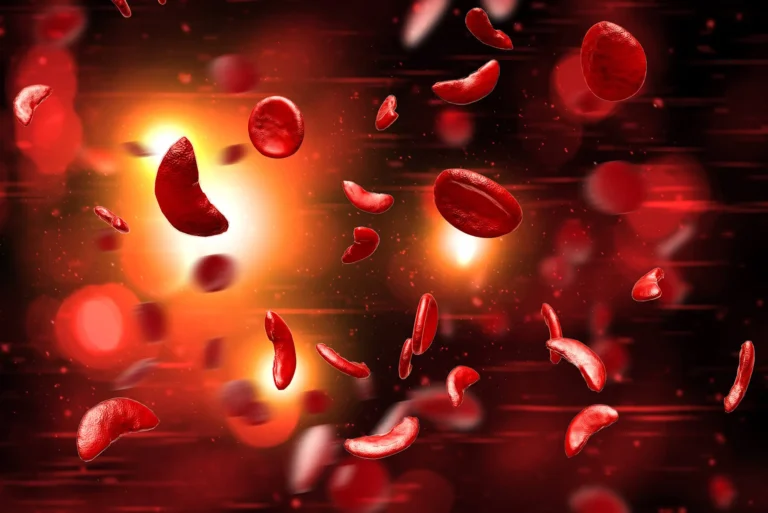
Niedokrwistość sierpowatokrwinkowa to choroba genetyczna, w której kluczowe białko zawarte w krwinkach czerwonych – hemoglobina – jest zbudowane nieprawidłowo, przez co jego funkcja ulega upośledzeniu. W warunkach niedotlenienia organizmu uszkodzona hemoglobina zaczyna tworzyć dłuższe łańcuchy, tworząc nieodwracalną charakterystyczną sierpowatą krwinkę czerwoną.
Dodatkowo polimeryzacja prowadzi do przewlekłego niszczenia erytrocytów i zatykania naczyń krwionośnych. W naszej szerokości geograficznej choroba występuje rzadko, jest natomiast dość częsta w krajach Afryki środkowej i zachodniej, a także wśród osób pochodzenia afrykańskiego.
>> Sprawdź też: Anemia – przyczyny, objawy i rodzaje niedokrwistości
Dziedziczenie niedokrwistości sierpowatokrwinkowej
Anemia sierpowata jest dziedziczona w sposób autosomalny recesywny, co oznacza, że do zachorowania dochodzi przy obecności mutacji w dwóch wariantach (allelach) genu. Taki sposób dziedziczenia oznacza, że obecność tylko jednego allelu z mutacją nie wywołuje pełnoobjawowej choroby – uszkodzonych krwinek jest tylko część, ale nie wszystkie.
Anemia sierpowatokrwinkowa może być leczona, nie jest jednak uleczalna. Nieprawidłowa hemoglobina w tym przypadku powstaje w wyniku pojedynczej mutacji zmiany sensu, prowadzącej do zastąpienia kwasu glutaminowego waliną w szóstej pozycji łańcucha β-globiny w hemoglobinie.
Anemia sierpowata – objawy
Czerwone krwinki, które zawierają HbS, pod wpływem środowiska ubogiego w tlen ulegają polimeryzacji i stają się sztywne. Powoduje to, że są podatne na hemolizę (rozpad), prowadzą do okluzji naczyń krwionośnych i niedokrwienia tkanek.
Z tego powodu anemia sierpowatokrwinkowa wywołuje szereg objawów:
- ostry ból: może dotyczyć dowolnej części ciała – najczęściej rąk i stóp, początek jest spontaniczny, może dotyczyć każdej części ciała, zwykle bez czynników wywołujących; może jednak być indukowany przez infekcje, gorączkę, odwodnienie, nagłą zmianę pogody, zimno i zanieczyszczenie powietrza;
- przewlekły ból: powtarzające się epizody bólowe prowadzą do przebudowy receptorów, co skutkuje ciągłym odczuwaniem dolegliwości;
- zmęczenie, osłabienie, słaba tolerancja wysiłku będące skutkiem niedokrwistości (w okresie bezobjawowym stężenie hemoglobiny zazwyczaj mieści się w zakresie 6 – 8 g/dl);
- zwiększona podatność na infekcje, zwłaszcza posocznicę bakteryjną i malarię u dzieci poniżej piątego roku życia;
- ostry zespół piersiowy charakteryzujący się wysokim ryzykiem zgonu: gorączka, ból i uczucie ucisku w klatce piersiowej, przyspieszony oddech, kaszel i duszność;
- powiększenie śledziony, niekiedy prowadzące do pęknięcia narządu i zgonu wskutek wstrząsu;
- deficyty poznawcze: niższa inteligencja, zaburzenia wzrokowo-ruchowe, dysfunkcje wykonawcze i zaburzenia pamięci;
- priapizm: długotrwały, bolesny wzwód prącia;
- zaburzenia lękowe i/lub depresyjne;
- uszkodzenie i/lub utrata wzroku;
- udary mózgu, w tym nieme klinicznie, z postępującym uszkodzeniem tego narządu;
- sinica, kołatanie serca, duszność, obrzęk, omdlenia, zmęczenie, ucisk i ból w klatce piersiowej jako skutek przewlekłego uszkodzenia płuc;
- wtórna niedokrwistość, krwiomocz, zaburzenia zagęszczenia moczu, albuminuria, uszkodzenie kłębuszków nerkowych jako skutek przewlekłej choroby nerek;
- owrzodzenia skóry, trudno gojące się rany przewlekłe, zakrzepica;
- podatność na złamania, zapalenia stawów, ograniczony zakres ruchu;
- przełom aplastyczny: zwykle wywoływany przez parwowirusa B-19 szybki spadek poziomu hemoglobiny o co najmniej 3 do 6 g/dl poniżej wartości wyjściowej; pojawia się silne zmęczenie, anemia, duszność, omdlenia.
Warto dodać, że objawy choroby pojawiają się już od wczesnego dzieciństwa.
Anemia sierpowata a malaria – jakie jest powiązanie?
W jednej sytuacji chorowanie na anemię sierpowatą jest “korzystne”. Mowa tu o malarii, tropikalnej chorobie wywołanej głównie przez zarodźca sierpowatego (Plasmodium falciparum), która w swoim przebiegu prowadzi do pękania krwinek czerwonych.
Dzieje się tak, gdyż zarodziec namnaża się w erytrocytach, ale tylko w tych o prawidłowej budowie hemoglobiny; zmienione chorobowo białko jest omijane przez pierwotniaka.
Stąd osoby będące nosicielami anemii sierpowatej, mające część krwinek prawidłowych, a część uszkodzonych, zdecydowanie łagodniej chorują na malarię.
Anemia sierpowata – diagnostyka. Jakie badania wykonuje się w kierunku diagnozy?
Podejrzenie anemii sierpowatej powinno skłaniać ku wykonaniu prostych badań:
- w morfologii krwi obwodowej pojawia się umiarkowanego stopnia niedokrwistość z towarzyszącym zwiększonym odsetkiem retikulocytów – młodych, niedojrzałych w pełni krwinek czerwonych,

- zwiększeniu może ulegać liczba płytek krwi i granulocytów,
- w rozmazie uwidocznione są krwinki o nieprawidłowym kształcie – sierpowate, tarczowate, a także owalne,
- zwiększeniu ulega stężenie bilirubiny całkowitej z przewagą frakcji wolnej (pośredniej, niezwiązanej z białkami krwi),
- elektroforeza (czyli rozdzielenie za pomocą pola elektrycznego) pozwala na określenie proporcji poszczególnych rodzajów hemoglobiny: obecność HbS, brak HbA (prawidłowej) i zwiększenie odsetka hemoglobiny płodowej,
- wysokosprawna chromatografia cieczowa (HPLC) może rozróżnić większość typów niedokrwistości sierpowatokrwinkowej, w tym heterozygotyczną,
- testy genetyczne oparte o metodę PCR: pozwalają na zidentyfikowanie mutacji wywołującej chorobę.

Diagnostyka niedokrwistości sierpowatej może być rozszerzona o ocenę ewentualnych powikłań. W tym przypadku zakres wykonywanych badań zależy od prezentowanych objawów, badania przedmiotowego oraz wywiadu chorobowego.
Anemia sierpowata – leczenie
Terapia anemii sierpowatej składa się trzech ważnych elementów: profilaktyki, zmniejszania odsetka nieprawidłowej hemoglobiny oraz leczenia powikłań.
Profilaktyka
Z uwagi na zwiększone ryzyko poważnych infekcji silnie zalecane są szczepienia przeciwko pneumokokom, a w wieku 2 i 5–7 lat uzupełnienie o preparat 23-walentny. Dodatkowe zalecane szczepienia obejmują H. influenzae typu b, szczepionkę przeciwko meningokokom (grupy B oraz A,C,Y i W135) i coroczne szczepienie przeciwko grypie.
Do 5. roku życia prowadzona jest także profilaktyka polegająca na podawaniu penicyliny – należy ją kontynuować do 5. roku życia, kiedy ryzyko inwazyjnej choroby bakteryjnej jest mniejsze.
Gorączka powyżej 38,5°C to stan nagły wymagający natychmiastowej oceny lekarskiej, obejmującej badanie fizykalne z uwzględnieniem parametrów życiowych i palpację śledziony, posiew krwi, pełną morfologię krwi, liczbę retikulocytów, badanie moczu i ewentualnie RTG klatki piersiowej.
Istotnym elementem jest edukacja pacjenta i jego otoczenia co do możliwych ostrych powikłań choroby.
Zmniejszanie odsetka nieprawidłowej hemoglobiny
Podstawowym lekiem od wielu lat pozostaje hydroksymocznik z hydroksykarbamidem, które indukują wytwarzanie hemoglobiny płodowej (HbF) i zmniejszają stan zapalny.
Stosowana jest także L-glutamina, która redukuje przewlekły ból i wydłuża czas do wystąpienia kolejnego bólu ostrego.
W ostatnich latach na rynku pojawił się lek biologiczny, kryzanlizumab, który jest wskazany u pacjentów w wieku 16 lat i starszych, a który zapobiega powikłaniom naczyniowym.
Obecnie coraz powszechniejszą metodą leczenia jest allogeniczny przeszczep szpiku kostnego (HSCT) polegający na zastąpieniu źródła wadliwych czerwonych krwinek szpikiem od zdrowego dawcy.
Odchodzi się od systematycznych przetoczeń koncentratu krwinek czerwonych.
Leczenie ostrych powikłań
Tu terapia jest wielodyscyplinarna, a spektrum możliwych kombinacji bardzo szerokie; interwencje obejmują zarówno farmakoterapię, jak i leczenie operacyjne.
Anemia sierpowa – podsumowanie
Niedokrwistość sierpowatokrwinkowa jest ciężką chorobą obarczoną ryzykiem wielu poważnych następstw. Nie jest chorobą uleczalną, można jednak zmniejszyć szereg dewastujących skutków. Leczenie jest wielokierunkowe, obejmuje profilaktykę, zapobieganie powikłaniom naczyniowym i leczenie ostrych powikłań.
Źródła
2019-2021 ASH Clinical Practice Guidelines on Sickle Cell Disease
https://www.hematology.org/education/clinicians/guidelines-and-quality-care/clinical-practice-guidelines/sickle-cell-disease-guidelines
McGann PT, Nero AC, Ware RE. Current management of sickle cell anemia. Cold Spring Harb Perspect Med. 2013 Aug 1;3(8):a011817. doi: 10.1101/cshperspect.a011817. PMID: 23709685; PMCID: PMC3721270.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3721270/
Sundd P, Gladwin MT, Novelli EM. Pathophysiology of Sickle Cell Disease. Annu Rev Pathol. 2019 Jan 24;14:263-292. doi: 10.1146/annurev-pathmechdis-012418-012838. Epub 2018 Oct 17. PMID: 30332562; PMCID: PMC7053558.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7053558/
Abdel-Hadi L, Ventura Carmenate Y, Castillo-Aleman YM, Sheikh S, Zakaria A, Phillips J. Treatment of sickle cell disease – options and perspective. Am J Blood Res. 2023 Apr 15;13(2):61-70. PMID: 37214647; PMCID: PMC10195315.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10195315/
Brandow AM, Liem RI. Advances in the diagnosis and treatment of sickle cell disease. J Hematol Oncol. 2022 Mar 3;15(1):20. doi: 10.1186/s13045-022-01237-z. PMID: 35241123; PMCID: PMC8895633.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8895633/
Inusa BPD, Hsu LL, Kohli N, Patel A, Ominu-Evbota K, Anie KA, Atoyebi W. Sickle Cell Disease-Genetics, Pathophysiology, Clinical Presentation and Treatment. Int J Neonatal Screen. 2019 May 7;5(2):20. doi: 10.3390/ijns5020020. PMID: 33072979; PMCID: PMC7510211.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7510211/
Arishi WA, Alhadrami HA, Zourob M. Techniques for the Detection of Sickle Cell Disease: A Review. Micromachines (Basel). 2021 May 5;12(5):519. doi: 10.3390/mi12050519. PMID: 34063111; PMCID: PMC8148117.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8148117/