Ornitoza (papuzica) to rzadka, ale potencjalnie groźna choroba zakaźna przenoszona przez ptaki – nie tylko papugi. Powoduje ją bakteria Chlamydia psittaci. Sprawdź objawy, drogi zakażenia oraz leczenie infekcji, potocznie nazywanej również chorobą hodowców gołębi.
| Z tego artykułu dowiesz się, że: >> ornitoza (papuzica) to choroba odzwierzęca przenoszona przez ptaki, >> w przebiegu choroby dominuje gorączka, kaszel i silny ból głowy, >> może prowadzić do poważnych powikłań, m.in. zapalenia płuc, a rzadziej także do zapalenia opon mózgowo-rdzeniowych, >> diagnoza opiera się na wywiadzie, badaniach obrazowych i testach serologicznych lub PCR, >> leczenie polega głównie na antybiotykoterapii, a profilaktyka obejmuje utrzymywanie odpowiednich zasad higieny i ostrożności w kontakcie z ptakami. |
Spis treści:
- Ornitoza: co to za choroba?
- Ornitoza u ludzi: przyczyny rozwoju choroby
- Jak często występuje papuzica?
- Ornitoza: objawy u człowieka
- Jak diagnozuje się ornitozę?
- Jak leczy się papuzicę?
- Profilaktyka ornitozy
- Papuzica: najczęstsze pytania o ornitozę (FAQ)
- Podsumowanie
Ornitoza: co to za choroba?
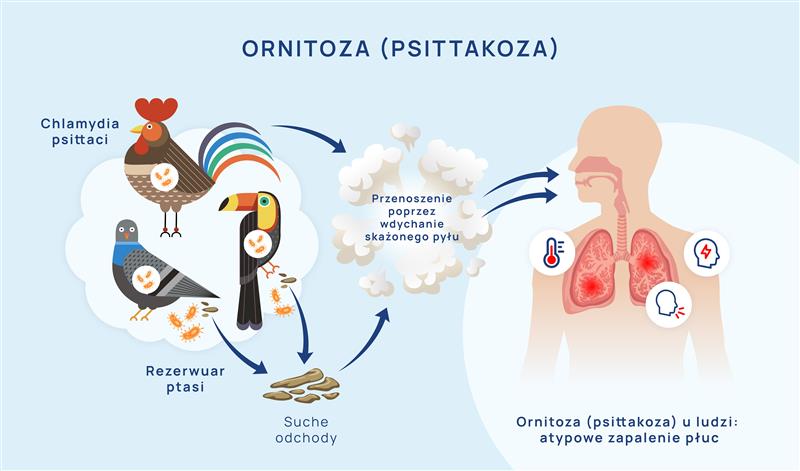
Ornitoza (w klasyfikacji ICD‑10 oznaczona kodem A70), nazywana także papuzicą lub chorobą ptasią, to choroba zakaźna wywoływana przez bakterię Chlamydia psittaci, której naturalnym rezerwuarem są ptaki – zarówno domowe (np. papugi, kanarki), jak i hodowlane czy dzikie. Papuzica należy do grupy zoonoz, czyli infekcji przenoszonych ze zwierząt na człowieka.
>> Zobacz: Najczęstsze choroby odzwierzęce i ich objawy
Ornitoza u ludzi: przyczyny rozwoju choroby
Do zakażenia bakterią dochodzi najczęściej poprzez wdychanie powietrza zanieczyszczonego cząstkami odchodów, wydzielin dróg oddechowych lub pyłu z piór zakażonych ptaków. Nie jest konieczny bezpośredni kontakt ze zwierzęciem – wystarczy przebywanie w pomieszczeniu, w którym były ptaki, zwłaszcza jeśli jest ono słabo wentylowane. Ryzyko zwiększa także czyszczenie klatek „na sucho” oraz nieprzestrzeganie zasad higieny. Źródłem zakażenia mogą być również inne elementy środowiska ptaków, takie jak ściółka, karmniki, miski z wodą czy kurz osadzony na sprzętach i ubraniach.
Szczególnie narażone na zakażenie są osoby mające regularny kontakt z ptakami:
- hodowcy ptaków,
- lekarze weterynarii, technicy weterynaryjni,
- pracownicy sklepów zoologicznych, zakładów przetwórstwa drobiowego,
- pracownicy służb granicznych, transportowych, inspekcji sanitarnych.
Transmisję między ludźmi opisywano bardzo rzadko (zwykle przy bliskim, długotrwałym kontakcie). W praktyce głównym źródłem zakażenia pozostają ptaki.
>> Przeczytaj: Ptasia grypa u ludzi – jak się objawia i czy stanowi zagrożenie dla człowieka
Jak często występuje papuzica?
Papuzica rozpoznawana jest rzadko, jednak jej rzeczywista częstość może być niedoszacowana. Przebieg choroby bywa niespecyficzny, a testy w kierunku Chlamydia psittaci nie są wykonywane rutynowo. Szacuje się, że ornitoza odpowiada za ok. 1% przypadków pozaszpitalnego zapalenia płuc, choć odsetek ten może być wyższy, zwłaszcza wśród osób zawodowo narażonych na kontakt z ptakami.
Zachorowania mają zwykle charakter sporadyczny, ale zdarzają się również ogniska epidemiczne, m.in. w rzeźniach, hodowlach czy placówkach ochrony zdrowia. W ostatnich latach zgłaszano okresowe wzrosty liczby przypadków w niektórych krajach Europy.

Ornitoza: objawy u człowieka
Objawy ornitozy pojawiają się zazwyczaj po 5-14 dniach od kontaktu z zakażonym ptakiem, choć w niektórych przypadkach okres wylęgania może być dłuższy. Przebieg choroby bywa różnorodny: od łagodnych objawów przypominających grypę, po ciężkie zapalenie płuc i powikłania wielonarządowe. U części pacjentów papuzica rozwija się dwufazowo.
Objawy papuzicy w I fazie
Pierwsza faza choroby zwykle rozpoczyna się nagle i może przypominać infekcję grypopodobną. Objawy ogólne są zwykle wyraźnie zaznaczone, pojawiają się na kilka dni przed rozwojem dolegliwości ze strony układu oddechowego. Należą do nich:
- nagła, wysoka gorączka (często powyżej 39°C),
- silny, pulsujący ból głowy (często dominujący objaw),
- dreszcze, bóle mięśni i stawów,
- znaczne osłabienie, uczucie rozbicia,
- ból gardła, suchość w jamie ustnej,
- brak apetytu, nudności.
Ze względu na niespecyficzny charakter dolegliwości, papuzicę można początkowo pomylić z grypą, anginą lub inną chorobą zakaźną.
Objawy papuzicy w II fazie
Po kilku dniach mogą pojawić się objawy ze strony układu oddechowego i inne symptomy:
- suchy, uporczywy kaszel,
- duszność, ból w klatce piersiowej,
- powiększenie wątroby i śledziony,
- zawroty głowy, zaburzenia świadomości,
- rzadziej: zapalenie spojówek, biegunka, wysypka skórna.
W ciężkich przypadkach ornitozy możliwe są powikłania, takie jak zapalenie opon mózgowo-rdzeniowych, mięśnia sercowego, wsierdzia czy ostre uszkodzenie wątroby. Szczególne ryzyko dotyczy osób starszych, z obniżoną odpornością i kobiet w ciąży.
Jak diagnozuje się ornitozę?
Rozpoznanie ornitozy opiera się na połączeniu obrazu klinicznego, dokładnego wywiadu epidemiologicznego (kontakt z ptakami) oraz badań serologicznych lub molekularnych. Do podstawowych narzędzi diagnostycznych należą:
- RTG klatki piersiowej: ujawnia zmiany śródmiąższowe lub płatowe nacieki zapalne (często w dolnych płatach). Czasem zmiany mogą być bardziej nasilone niż objawy kliniczne.
- Badania serologiczne:
- IgM, IgG, IgA metodą ELISA lub Western Blot: wykrywa przeciwciała przeciw Chlamydia psittaci; IgM może sugerować świeższe zakażenie, IgG częściej świadczy o przebytym kontakcie lub trwającym zakażeniu, a IgA bywa wiązane z aktywną odpowiedzią śluzówkową/przewlekłym zakażeniem; dostępne są panele obejmujące inne gatunki (np. C. pneumoniae, C. trachomatis), co wymaga interpretacji w kontekście objawów i wywiadu,
- MIF (microimmunofluorescencja): metoda referencyjna, w razie potrzeby może pomóc odróżnić zakażenie C. psittaci od innych gatunków Chlamydia; dostępna w wyspecjalizowanych laboratoriach.
- CF (test wiązania dopełniacza): szerzej dostępny, ale mniej swoisty; nie pozwala wiarygodnie odróżnić gatunków Chlamydia.
- PCR (reakcja łańcuchowa polimerazy): wykrywa DNA Chlamydia psittaci, preferencyjnie w materiale z dolnych dróg oddechowych (plwocina, aspirat/BAL). Wysoce swoisty, charakteryzuje się większą czułością niż serologia w ostrym stadium choroby. Częściej stosowany w diagnostyce zakażeń atypowych.
Do badań pomocniczych należą:
- morfologia krwi: ocena odpowiedzi zapalnej, ewentualnych zaburzeń hematologicznych,
- CRP, OB: markery stanu zapalnego,
- ALT, AST, LDH: wskaźniki zajęcia wątroby i uszkodzenia komórkowego,
- albumina: ocena stanu odżywienia i reakcji ostrej fazy (spadek w przebiegu zapalenia),
- jonogram (Na+, K+): monitorowanie zaburzeń wodno-elektrolitowych, zwłaszcza w cięższym przebiegu choroby,
- kreatynina, mocznik: ocena funkcji nerek, ewentualnych powikłań wielonarządowych,
- CK: wykrywanie uszkodzeń mięśni lub nasilenia procesu zapalnego.
W przypadku podejrzenia zajęcia ośrodkowego układu nerwowego wykonuje się również badanie płynu mózgowo-rdzeniowego, które może ujawniać pleocytozę i podwyższony poziom białka, choć zmiany te są nieswoiste.
Jak leczy się papuzicę?
Leczeniem z wyboru w ornitozie jest antybiotykoterapia, którą należy rozpocząć jak najszybciej po postawieniu rozpoznania. Nie trzeba czekać na wynik serologii czy PCR, jeśli obraz choroby i wywiad epidemiologiczny wskazują na ornitozę. Najczęściej stosuje się doksycyklinę (100 mg doustnie 2 razy dziennie przez co najmniej 10-14 dni; w cięższych przypadkach podawaną dożylnie w tej samej dawce).
W przypadku przeciwwskazań do tetracyklin (np. u dzieci, ciężarnych, przy nietolerancji tetracyklin) podaje się:
- azytromycynę: np. 500 mg pierwszego dnia, następnie 250 mg raz dziennie przez kolejne 4 dni,
- erytromycynę: 500 mg 4 razy dziennie przez 10-14 dni.
Większość pacjentów dobrze reaguje na leczenie. Poprawa ogólna i spadek gorączki obserwowane są zwykle w ciągu 48-72 godzin.

Profilaktyka ornitozy
Ponieważ nie istnieje szczepionka przeciwko Chlamydia psittaci, profilaktyka papuzicy opiera się na ograniczaniu ekspozycji i przestrzeganiu zasad higieny w kontakcie z ptakami.
Rekomendowane środki zapobiegawcze to:
- mycie rąk po kontakcie z ptakami lub ich wydzielinami, klatkami,
- czyszczenie klatek na mokro, w dobrze wentylowanych pomieszczeniach, przy użyciu maseczki, rękawic ochronnych,
- kwarantanna nowo nabytych ptaków przed kontaktem z innymi zwierzętami lub ludźmi,
- regularna kontrola zdrowia ptaków w hodowlach, sklepach zoologicznych i gospodarstwach drobiarskich,
- unikanie przebywania w zamkniętych pomieszczeniach z dużą liczbą ptaków, zwłaszcza bez odpowiednich środków ochrony.
Nie ma dowodów, aby do zakażenia dochodziło przez spożycie prawidłowo przygotowanego mięsa drobiowego – ryzyko dotyczy przede wszystkim wdychania zakaźnego pyłu/aerozolu w środowisku ptaków.
Papuzica: najczęstsze pytania o ornitozę (FAQ)
Odpowiedzi na najczęściej zadawane pytania dotyczące ornitozy.
Tak, zwłaszcza w przypadku opóźnionego rozpoznania lub braku leczenia. Choć większość zakażeń przebiega łagodnie, papuzica może prowadzić do powikłań, m.in. zapalenia płuc, mięśnia sercowego, wątroby czy układu nerwowego. Większe ryzyko dotyczy osób starszych, w ciąży i z obniżoną odpornością.
Nie, obecnie nie istnieje szczepionka na papuzicę. Trwają badania nad skuteczną immunoprofilaktyką, ale na dziś jedyną formą ochrony pozostaje higiena, nadzór nad zdrowiem ptaków i ograniczanie kontaktu z potencjalnym źródłem zakażenia.
Podsumowanie
Papuzica (ornitoza) to rzadka choroba odzwierzęca przenoszona przez ptaki, wywoływana przez bakterię Chlamydia psittaci. Objawia się gorączką, kaszlem i bólem głowy, a nieleczona może prowadzić do poważnych powikłań. Rozpoznanie opiera się na wywiadzie, badaniach obrazowych płuc, testach serologicznych i PCR. Leczenie polega na antybiotykoterapii doksycykliną lub makrolidami. Kluczowa pozostaje profilaktyka – higiena i zachowanie ostrożności przy kontakcie z ptakami.
Bibliografia
- Chandran L., Boykan R. Zakażenia wywołane przez chlamydie u dzieci i nastolatków. Pediatria po Dyplomie. 2011;15(2).
- Parfieniuk-Kowerda A. Chlamydiozy: Co to jest chlamydia i jakie objawy powoduje? Medycyna Praktyczna. Choroby zakaźne.
- Powiatowa Stacja Sanitarno-Epidemiologiczna w Wałbrzychu. Wzrost zachorowań na papuzicę w Europie.
- Richards M.J. Psittacosis. UpToDate.