Tyreotoksykoza to stan związany z nadmiernym działaniem hormonów tarczycy na organizm. Przeczytaj i dowiedz się, czym jest tyreotoksykoza, jakie są jej przyczyny, objawy, metody diagnostyczne oraz możliwości leczenia. Chcesz wiedzieć, jak tyreotoksykoza przebiega w ciąży i jakie niesie ryzyko? Wiele odpowiedzi znajdziesz właśnie tutaj.
| Z tego artykułu dowiesz się: >> czym jest tyreotoksykoza i jaka jest różnica między tyreotoksykozą a nadczynnością tarczycy, >> jak często występuje, >> jakie są jej najczęstsze przyczyny, >> jakie objawy mogą sugerować nadmiar hormonów tarczycy, >> czym jest tyreotoksykoza w ciąży i kiedy wymaga leczenia, >> jakie badania pozwalają postawić diagnozę, >> jakie są dostępne metody leczenia, >> jakie powikłania grożą w przypadku nieleczonej tyreotoksykozy. |
Spis treści:
- Tyreotoksykoza – co to jest?
- Epidemiologia tyreotoksykozy
- Przyczyny tyreotoksykozy
- Objawy tyreotoksykozy
- Czym jest tyreotoksykoza ciążowa?
- Diagnostyka tyreotoksykozy
- Leczenie tyreotoksykozy
- Powikłania nieleczonej tyreotoksykozy
- Podsumowanie
Tyreotoksykoza – co to jest?
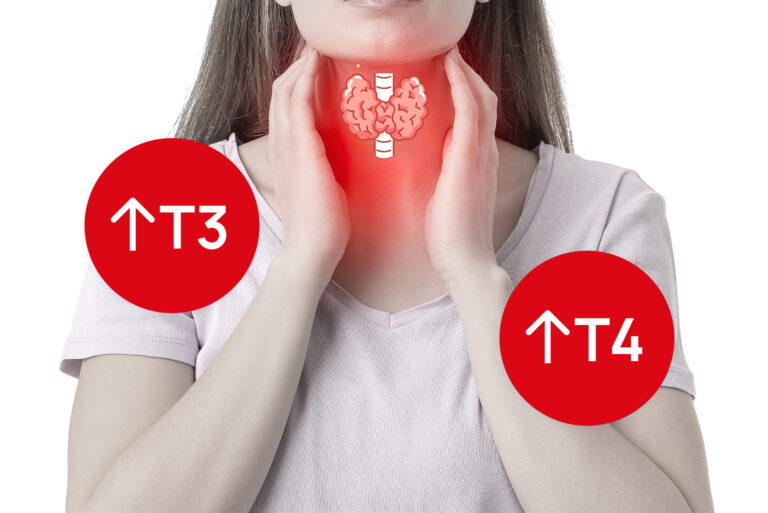
Tyreotoksykoza to stan, w którym w organizmie występuje nadmierne działanie hormonów tarczycy — trójjodotyroniny (T3) i tyroksyny (T4). Dochodzi do tego niezależnie od źródła nadmiaru hormonów.
Tyreotoksykoza a nadczynność tarczycy
Tyreotoksykoza jest stanem klinicznym wynikającym z nadmiaru hormonów, natomiast nadczynność tarczycy odnosi się do sytuacji, w której sama tarczyca produkuje zbyt dużo hormonów. Można więc mieć tyreotoksykozę bez nadczynności (np. w zapaleniu tarczycy), ale także nadczynność bez jawnych objawów tyreotoksykozy.
>> Przeczytaj również: Choroby tarczycy i ich diagnostyka
Epidemiologia tyreotoksykozy
Tyreotoksykoza występuje u około 0,2–1,3% dorosłych, częściej u kobiet niż u mężczyzn. W populacjach z niedoborem jodu częstość ta może być większa.
Przyczyny tyreotoksykozy
Tyreotoksykoza może mieć różne źródła — od nadprodukcji hormonów po ich uwalnianie na skutek uszkodzenia tarczycy lub nadmierną podaż z zewnątrz.
Choroba Gravesa-Basedova
Najczęstsza przyczyna tyreotoksykozy to choroba Gravesa-Basedova. Mechanizm opiera się na autoimmunologicznym pobudzeniu receptora TSH przez przeciwciała, co prowadzi do niekontrolowanej produkcji hormonów tarczycy. Charakterystyczne jest rozlane powiększenie tarczycy oraz możliwość wystąpienia objawów ocznych.

Sprawdź też:
>> Co to jest TSH i jaką rolę pełni w organizmie?
>> Nadczynność tarczycy – objawy, przyczyny, badania, leczenie
Guzki tarczycy i wole guzkowe
Autonomiczne guzki tarczycy lub wieloguzkowe wole toksyczne mogą samodzielnie wytwarzać hormony tarczycy, niezależnie od układu regulacji hormonalnej. To częsta przyczyna tyreotoksykozy u osób starszych.
Zapalenia tarczycy
W zapaleniach tarczycy dochodzi do uszkodzenia komórek pęcherzykowych i uwalniania wcześniej zmagazynowanych hormonów. Tyreotoksykoza ma wówczas zwykle charakter przejściowy. Dotyczy to m.in. bezbolesnego zapalenia tarczycy, poporodowego zapalenia tarczycy i podostrego zapalenia tarczycy.
Tyreotoksykoza indukowana lekami
Do omawianego stanu mogą prowadzić:
- nadmierna podaż leków hormonalnych,
- nadmiar jodu (np. z kontrastów lub suplementów),
- tyreotoksykoza wywołana amiodaronem (lekiem stosowanym głównie w zaburzeniach rytmu serca).
W mechanizmie tym tarczyca nie jest pierwotnie nadczynna – problem wynika ze zbyt wysokiej podaży hormonu lub jodu.
Objawy tyreotoksykozy
Objawy wynikają z przyspieszenia metabolizmu oraz nadmiernej stymulacji układu nerwowego i krążenia. Mogą być zróżnicowane i dotyczyć wielu układów.
Objawy ogólne i metaboliczne
Do najczęstszych należą:
- spadek masy ciała mimo wzmożonego apetytu,
- uczucie gorąca, nietolerancja ciepła,
- nadmierna potliwość,
- drżenie rąk, osłabienie mięśni,
- biegunki i zaburzenia miesiączkowania.
Objawy ze strony układu krążenia
Można zaobserwować:
- kołatania serca,
- szybkie bicie serca,
- zwiększone ciśnienie tętnicze,
- w skrajnych przypadkach objawy niewydolności serca.
Objawy neurologiczne i psychiczne
Nadmiar hormonów może powodować:
- pobudzenie, nerwowość, drażliwość,
- bezsenność, lęk, trudności z koncentracją,
- osłabienie mięśni, drżenia,
- w skrajnych przypadkach zaburzenia świadomości.
Objawy ze strony narządu wzroku
W przebiegu choroby mogą wystąpić:
- wytrzeszcz oczu,
- uczucie ciała obcego, suchość, łzawienie,
- światłowstręt,
- ograniczenia ruchomości gałek ocznych, podwójne widzenie.
Czym jest tyreotoksykoza ciążowa?
Niektóre zmiany hormonalne w ciąży mogą prowadzić do okresowego obniżenia TSH i wzrostu T4. W większości przypadków jest to fizjologiczne, ale czasami rozwija się tyreotoksykoza wymagająca diagnozy i obserwacji.
To również może Cię zainteresować:
>> Tarczyca przed ciążą – pod specjalnym nadzorem
>> Tarczyca w ciąży – pod specjalnym nadzorem
Tyreotoksykoza ciężarnych a choroba Gravesa-Basedowa
U kobiet z aktywną chorobą autoimmunologiczną tarczycy przeciwciała mogą przenikać przez łożysko i oddziaływać na tarczycę matki, a w rzadkich przypadkach — także płodu.
Kiedy tyreotoksykoza w ciąży może wymagać leczenia?
Leczenie jest wskazane, gdy objawy są nasilone, zagrażają zdrowiu matki, powodują powikłania sercowe lub mogą negatywnie wpływać na płód. W ciąży stosuje się tylko wybrane leki przeciwtarczycowe, a radiojodu się nie używa.
Diagnostyka tyreotoksykozy
Rozpoznanie opiera się na badaniach laboratoryjnych, obrazowych oraz ocenie klinicznej.
Badania laboratoryjne
Podstawą jest pomiar:
- TSH — zwykle niskie lub niewykrywalne,
- fT4 i fT3 — podwyższone.
Badanie przeciwciał
Umożliwia rozpoznanie tyreotoksykozy autoimmunologicznej poprzez ocenę przeciwciał przeciw receptorowi TSH.
Badania obrazowe
W diagnostyce stosuje się:
- USG tarczycy — szczególnie przy guzkach i zapaleniach,
- scyntygrafię tarczycy — oceniającą aktywność hormonalną gruczołu.
Leczenie tyreotoksykozy
Leczenie zależy od przyczyny, nasilenia objawów i ogólnego stanu pacjenta.
Farmakoterapia – leki przeciwtarczycowe
Najczęściej stosuje się tiamazol lub propylotiouracyl, które hamują wytwarzanie hormonów tarczycy. W celu złagodzenia objawów sercowych podaje się beta-blokery (leki spowalniające częstość pracy serca).
Leczenie tyreotoksykozy jodem promieniotwórczym
Radiojod niszczy nadczynne tkanki tarczycy i jest stosowany w utrwalonej nadczynności, zwłaszcza w chorobie guzkowej.
Leczenie chirurgiczne
Zabieg usunięcia tarczycy rozważa się, gdy leczenie farmakologiczne jest nieskuteczne, występują duże guzki, ucisk na inne struktury lub pacjent preferuje metodę definitywną.
Zasady leczenia tyreotoksykozy u kobiet w ciąży
Terapia musi być bezpieczna dla płodu. Stosuje się wybrane leki przeciwtarczycowe, a operacje przeprowadza się jedynie w uzasadnionych przypadkach. Leczenie radiojodem jest przeciwwskazane!
Powikłania nieleczonej tyreotoksykozy
Brak leczenia może prowadzić do szeregu poważnych skutków, takich jak:
- nadciśnienie tętnicze,
- zaburzenia rytmu serca (zwłaszcza migotanie przedsionków),
- niewydolność serca,
- osteoporoza,
- osłabienie mięśni,
- ryzyko zakrzepicy,
- przełom tarczycowy — stan zagrożenia życia.
Podsumowanie
Tyreotoksykoza jest poważnym stanem związanym z nadmiarem hormonów tarczycy. Może wynikać z autoimmunologicznej choroby Gravesa-Basedowa, obecności guzków tarczycy, zapaleń czy nadmiernej podaży hormonów i jodu. Objawy mogą obejmować wiele układów, od metabolicznych po neurologiczne i sercowe. Wczesna diagnostyka i odpowiednie leczenie pozwalają uniknąć groźnych powikłań.
Źródła
- Lee SY, Pearce EN. Hyperthyroidism: A Review. JAMA. 2023 Oct 17;330(15):1472-1483. doi: 10.1001/jama.2023.19052. PMID: 37847271; PMCID: PMC10873132.
https://pmc.ncbi.nlm.nih.gov/articles/PMC10873132/ (dostęp: 30.12.2025) - Sharma A, Stan MN. Thyrotoxicosis: Diagnosis and Management. Mayo Clin Proc. 2019 Jun;94(6):1048-1064. doi: 10.1016/j.mayocp.2018.10.011. Epub 2019 Mar 25. PMID: 30922695.
https://www.mayoclinicproceedings.org/article/S0025-6196(18)30799-7/fulltext (dostęp: 30.12.2025) - Ross DS, Burch HB, Cooper DS, Greenlee MC, Laurberg P, Maia AL, Rivkees SA, Samuels M, Sosa JA, Stan MN, Walter MA. 2016 American Thyroid Association Guidelines for Diagnosis and Management of Hyperthyroidism and Other Causes of Thyrotoxicosis. Thyroid. 2016 Oct;26(10):1343-1421. doi: 10.1089/thy.2016.0229. Erratum in: Thyroid. 2017 Nov;27(11):1462. doi: 10.1089/thy.2016.0229.correx. Erratum in: Thyroid. 2025 Sep;35(9):1097. doi: 10.1089/thy.2016.0229.correx2. PMID: 27521067.
https://www.liebertpub.com/doi/10.1089/thy.2016.0229?url_ver=Z39.88-2003&rfr_id=ori%3Arid%3Acrossref.org&rfr_dat=cr_pub++0pubmed (dostęp: 30.12.2025) - Kahaly GJ, Bartalena L, Hegedüs L, Leenhardt L, Poppe K, Pearce SH. 2018 European Thyroid Association Guideline for the Management of Graves’ Hyperthyroidism. Eur Thyroid J. 2018 Aug;7(4):167-186. doi: 10.1159/000490384. Epub 2018 Jul 25. PMID: 30283735; PMCID: PMC6140607.
https://pmc.ncbi.nlm.nih.gov/articles/PMC6140607/ (dostęp: 30.12.2025)