Krwiak podkosmówkowy to stan kliniczny będący dość częstą przyczyną konsultacji ginekologiczno-położniczych. Przypadłość ta może być przyczyną krwawienia z dróg rodnych i wymaga podjęcia diagnostyki różnicowej oraz wykonania odpowiednich badań laboratoryjnych i obrazowych.
| Z tego artykułu dowiesz się: >> Co to jest krwiak podkosmówkowy i jak powstaje? >> Jak objawia się krwiak podkosmówkowy i czy zawsze jest to stan objawowy? >> Z jakimi zagrożeniami dla płodu wiąże się obecność krwiaka podkosmówkowego? >> Jakie badania są niezbędne do rozpoznania krwiaka podkosmówkowego? >> Z jakim rokowaniem wiąże się zdiagnozowanie krwiaka podkosmówkowego? |
Spis treści:
- Czym jest krwiak podkosmówkowy?
- Jak często występują krwiaki w ciąży?
- Przyczyny wystąpienia krwiaka podkosmówkowego
- Jakie objawy towarzyszą krwiakom podkosmówkowym w ciąży?
- Dlaczego krwiak podkosmówkowy może być niebezpieczny?
- Pęknięcie krwiaka w ciąży: objawy
- Diagnostyka krwiaka podkosmówkowego w ciąży
- Rokowania pacjentek z krwiakiem podkosmówkowym
- Krwiak podkosmówkowy: najczęstsze pytania (FAQ)
Czym jest krwiak podkosmówkowy?
Krwiak podkosmówkowy (subchorionic hematoma – SCH) to obecność wynaczynionej krwi pomiędzy endometrium, czyli błoną śluzową wyścielającą jamę macicy, a błoną kosmówkową, a więc zewnętrzną błoną płodową, która otacza zarodek. Istotą problemu jest częściowe oddzielenie się kosmówki, związane z uszkodzeniem naczyń krwionośnych. Prowadzi to do krwawienia i zebrania się krwi między tymi dwiema błonami.
Kosmówka to błona, która powstaje w czasie 2-3 tygodnia ciąży, a w kolejnych tygodniach ciąży przekształca się w płodową część łożyska. Można więc powiedzieć, że jest to pierwotna forma tej struktury. Kosmówka zapewnia wymianę substancji między matką, a płodem (wymiana tlenu, substancji odżywczych czy też produktów przemiany materii). Co więcej, produkuje ważne hormony wpływające na prawidłowy przebieg ciąży – mowa tutaj o beta-hCG (a więc gonadotropinie kosmówkowej). Rola kosmówki jest więc kluczowa w rozwoju płodu i utrzymaniu ciąży.
Jak często występują krwiaki w ciąży?
Odnosząc się do populacji ogólnej, krwiak podkosmówkowy może wikłać nawet 3-20% ciąż. W niektórych dostępnych opracowaniach krwiak podkosmówkowy diagnozowany był nawet w 1 przypadku na 5 pięć ciąż. Należy jednak podkreślić, że dane dotyczące częstości tego zjawiska cechują się dość dużą rozbieżnością. U pacjentek borykających się z problemem niepłodności, krwiak ten odnotowywany był w 12,5% przypadków. Kosmówka jest obecna w pierwszym trymestrze, a więc patologia opisywana w tym artykule pojawia się typowo we wczesnym okresie ciąży.

Przyczyny wystąpienia krwiaka podkosmówkowego
Nie ma jednej, konkretnej przyczyny powstawania krwiaków podkosmówkowych. Czynniki ryzyka i stany kliniczne, które sprzyjają pojawieniu się tego zaburzenia to między innymi:
- nieprawidłowości dotyczące krążenia matczyno-płodowego – niedostateczne dostosowanie się układu naczyniowego w sytuacji pojawienia się rozwijającego się płodu,
- zaburzenia krzepnięcia, w tym trombofilia,
- schorzenia autoimmunologiczne – takie jak zespół antyfosfolipidowy,
- zaburzenia anatomiczne dotyczące układu rozrodczego, w tym macicy,
- urazy miednicy,
- zaburzenia hormonalne,
- nadmierny wysiłek fizyczny,
- przewlekły stan zapalny w obrębie endometrium,
- choroby układu sercowo-naczyniowego występujące u ciężarnej – w tym nieprawidłowo leczone lub nieleczone nadciśnienie tętnicze, a także zaburzenia naczyniowo-ruchowe.
>> Sprawdź: Ciśnienie w ciąży – jakie jest prawidłowe? Czy nadciśnienie w ciąży jest groźne?
Jakie objawy towarzyszą krwiakom podkosmówkowym w ciąży?
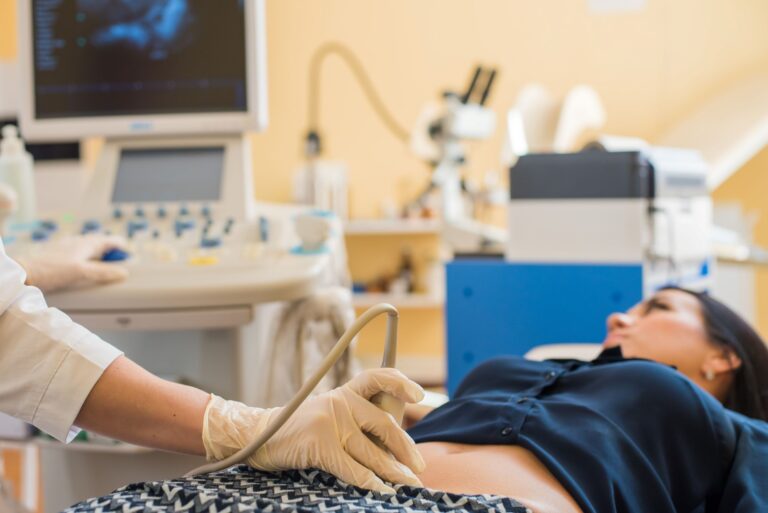
Na wstępie tego akapitu należy zaznaczyć, że niewielkie krwiaki podkosmówkowe mogą nie dawać żadnych objawów. Są wówczas zauważane podczas rutynowych badań ultrasonograficznych (badanie USG). Większe krwiaki podkosmówkowe mogą jednak wiązać się z obecnością symptomów klinicznych. Najczęstsze objawy krwiaka podkosmówkowego to:
- plamienie z dróg rodnych,
- krwawienie z dróg rodnych,
- rzadziej: ból zlokalizowany w podbrzuszu i uczucie napięcia w okolicy macicy.
Warto podkreślić, że krwiak podkosmówkowy jest jedną z najczęstszych przyczyn krwawienia w pierwszym trymestrze ciąży.
>> Zobacz:
- Plamienie lub krwawienie w ciąży – co może oznaczać i kiedy udać się do szpitala?
- Okres w ciąży – czy to możliwe? Co oznacza krwawienie w ciąży?
Dlaczego krwiak podkosmówkowy może być niebezpieczny?
Krwiak podkosmówkowy stanowi zagrożenie, ponieważ prowadzi do odwarstwienia kosmówki, co może w niektórych sytuacjach skutkować zaburzeniami w dostarczaniu tlenu i substancji odżywczych do rozwijającego się płodu. Stwarza to zagrożenie poronieniem. Ponadto, badania dowodzą, że pojawienie się krwiaka podkosmówkowego we wczesnej ciąży zwiększa ryzyko wystąpienia takich powikłań jak:
- PIH – nadciśnienie indukowane ciążą,
- IUGR – wewnątrzmaciczne zahamowanie wzrostu płodu,
- poród przedwczesny – czyli poród przed ukończeniem 37. tygodnia ciąży,
- mała masa urodzeniowa dziecka – a więc masa poniżej 2500 g,
- przedwczesne oddzielenie się łożyska.
Pęknięcie krwiaka w ciąży: objawy
Mówiąc o pęknięciu krwiaka mamy na myśli zjawisko przedostawania się krwi do jamy macicy. Proces ten będzie się objawiał klasycznie krwawieniem, które może być jednorazowym epizodem, ale może utrzymywać się przez kilka dni. W krwistej wydzielinie z dróg rodnych mogą pojawić się skrzepy. Niekiedy pojawiają się dolegliwości bólowe zlokalizowane w podbrzuszu.
>> To ważne: Ból brzucha w ciąży. Jakie objawy powinny niepokoić?
Diagnostyka krwiaka podkosmówkowego w ciąży
Pierwszym krokiem w diagnostyce krwiaka podkosmówkowego jest wywiad chorobowy i dokładne badanie przedmiotowe. Podstawą diagnostyki jest badanie ultrasonograficzne, które pozwala nie tylko na potwierdzenie obecności krwiaka, ale również na określenie jego lokalizacji oraz wielkości. W niektórych przypadkach konieczna może być hospitalizacja na Oddziale Ginekologiczno-Położniczym.
Jakie badania laboratoryjne wykonać przy krwiaku podkosmówkowym?
Badania laboratoryjne, które wykonuje się w trakcie diagnostyk i terapii krwiaka podtwardówkowego to przede wszystkim:
- morfologia krwi obwodowej – pozwala na ocenę stężenia hemoglobiny, a tym samym określenia stopnia utraty krwi, jeżeli doszło do krwawienia,
- stężenie beta-hCG (a więc gonadotropin kosmówkowej), stężenie progesteronu – pozwala na ocenę rozwoju ciąży,
- stężenie białka CRP – przy podejrzeniu infekcji,
- oznaczenie parametrów krzepnięcia – w tym stężenie fibrynogenu, a także oznaczenie APTT, PT, INR.
W przypadku podejrzenia trombofilii wykonuje się takie badania laboratoryjne jak:
- badanie na obecność mutacji czynnika V Leiden i protrombiny G20210A,
- oznaczenie białka C i białka S,
- oznaczenie poziomu antytrombiny.
Niekiedy konieczne bywa wykluczenie zespołu antyfosfolipidowego, który zwiększa ryzyko wystąpienia krwiaka podkosmówkowego. W tym celu oznacza się:
- przeciwciała antykardiolipinowe,
- antykoagulant toczniowy,
- przeciwciała anty-β2-glikoproteinie I.
Są to badania wykonywane z próbki krwi żylnej.
Rokowania pacjentek z krwiakiem podkosmówkowym
Niewielkie krwiaki podkosmówkowe w ogromnej większości przypadków nie mają znaczenia klinicznego i nie wiążą się z występowaniem powikłań. W wielu sytuacjach zmiany te mają tendencję do samoistnego wchłaniania się, a więc zmniejszania swoich rozmiarów. Gorsze rokowanie jest związane z wczesnym pojawienie się krwiaka, szczególnie przed ukończeniem 9. tygodnia ciąży. Należy mieć jednak świadomość, że większe krwiaki wiążą się z ryzykiem poważnych powikłań, w tym ryzykiem poronienia. Z tego powodu konieczne jest monitorowanie sytuacji klinicznej i stosowanie się do zaleceń prowadzącego ginekologa.
Krwiak podkosmówkowy: najczęstsze pytania (FAQ)
Krwiak podkosmówkowy wiąże się z licznymi obawami ciężarnych i ich rodzin. Poniżej odpowiedzi na najczęściej zadawane pytania.
To zależy. Nie da się określić dokładnie czasu wchłaniania krwiaka podkosmówkowego, ponieważ zależy to od wielu czynników, w tym jego wielkości i lokalizacji. Konieczne jest jednak monitorowanie tego procesu z wykorzystaniem ultrasonografii.
Nie zawsze, ponieważ zależy to od konkretnej sytuacji klinicznej. Jeżeli reżim łóżkowy został zalecony przez lekarza ginekologa, to należy stosować się wówczas do jego zaleceń.
Szczególnie niepokojące są duże krwiaki podkosmówkowe i krwiaki objawowe, w tym objawiające się krwawieniem z dróg rodnych. Każdy niepokojący objaw należy skonsultować z lekarzem prowadzącym ciążę.
Nie da się jednoznacznie odpowiedzieć na to pytanie. Ryzyko powikłań zależy bowiem od wielu składowych, w tym rozmiaru i lokalizacji krwiaka, a także stanu klinicznego ciężarnej.
Krwiak podkosmówkowy może wiązać się z wystąpieniem takich powikłań jak poronienie, nadciśnienie indukowane ciążą, wewnątrzmaciczne zahamowanie wzrostu płodu, poród przedwczesny, mała masa urodzeniowa dziecka czy też przedwczesne oddzielenie się łożyska.
Krwiaki podkosmówkowe mogą być przypadkowym znaleziskiem ultrasonograficznym i w przypadku małych rozmiarów – mogą nie mieć znaczenia klinicznego. Jednak w każdym przypadku konieczna jest ocena ginekologiczna i przeprowadzenie odpowiedniej diagnostyki.
Bibliografia
- B. Waksmański i inni, Ocena czynników prognostycznych przebiegu ciąży powikłanej krwiakiem pozałożyskowym rozpoznanym w pierwszej połowie ciąży, Klin Perinatol Ginek. 2004, 40, 15-19,
- L. Biesiada i inni, Krwiak podkosmówkowy jako czynnik ryzyka ciąży i porodu kobiet z zagrażającym poronieniem, Ginekol Pol, 2010, 81, 902-906,
- S. Nagy i inni, Clinical significance of subchorionic and retroplacental hematomas detected in the first trimester of pregnancy, Orv Hetil, 2005, 146, 2157-2161.