Artykuł powstał: 02.01.2023 r. ostatnia aktualizacja: 12.05.2026 r.
Stres jest stałym zjawiskiem w naszym życiu i nie jesteśmy w stanie go uniknąć, chociaż często marzy nam się „życie bez stresu”. Biorąc jednak pod uwagę fakt, iż stres jest również procesem, który mobilizuje nas do wysiłku, bezstresowe życie nie jest stanem pożądanym. To, czego musimy się nauczyć, to jak radzić sobie ze stresem i jak można poznać, że stres przestał być naszym przyjacielem.
| Z tego artykułu dowiesz się, że: >> stres jest nie tylko zjawiskiem negatywnym, ale do pewnego stopnia odgrywa rolę pozytywną, >> niekorzystne skutki zdrowotne może mieć bardzo nasilony lub długotrwały stres, >> poziom stresu można oszacować korzystając ze skali Holmesa i Rahe’a, >> w ocenie skutków stresu pomocne są badania laboratoryjne, np. długość telomerów, >> radzenie sobie ze stresem powinno być jedną z kompetencji współczesnego człowieka, >> pomocne w rozładowywaniu stresu są techniki oddechowe. |
Spis treści:
- Czym jest stres?
- Co się dzieje w organizmie pod wpływem stresu?
- Krzywa stresu – dystres i eustres
- Skutki stresu
- Objawy stresu
- Stres – jakie badania laboratoryjne należy zrobić?
- Radzenie sobie ze stresem na co dzień
- Sposoby na stres – co robić, gdy zaczniesz się stresować?
- Zakończenie
Czym jest stres?
Słowo „stres” w języku polskim zostało zapożyczone z języka angielskiego, gdzie wyraz „stress” dosłownie oznacza „naprężenie”. Pojęcie stresu pojawiło się w literaturze naukowej w 1956 roku, doczekało się bardzo wielu naukowych wyjaśnień w dziedzinie medycyny i psychologii. W każdej z nich stres ma swoją definicję, która ewoluowała przez lata pod wpływem badań.
Czym jest stres? Najprościej mówiąc, jest to odpowiedź organizmu (reakcja) na bodźce, które zakłócają jego homeostazę (równowagę).
Co się dzieje w organizmie pod wpływem stresu?
W reakcji na bodziec, będący również stresorem, w organizmie człowieka zachodzi szereg zmian. Ciało mobilizuje się do walki z zagrożeniem lub do ucieczki (reakcja walcz lub uciekaj), aktywuje układ współczulny, wydzielając adrenalinę i noradrenalinę. Dzięki temu:
- rośnie ciśnienie krwi,
- przyspiesza akcja serca,
- przyspiesza oddech,
- ciało się poci,
- hamowane są procesy trawienia,
- krew napływa do mięśni, serca i mózgu.
Powyższe reakcje występują już kilka chwil po zadziałaniu stresora, dzięki nim organizm jest gotowy do natychmiastowego działania.
Kilka minut do kilku godzin po zadziałaniu stresora aktywowany jest inny mechanizm odpowiedzi na stres – oś podwzgórze-przysadka-nadnercza.
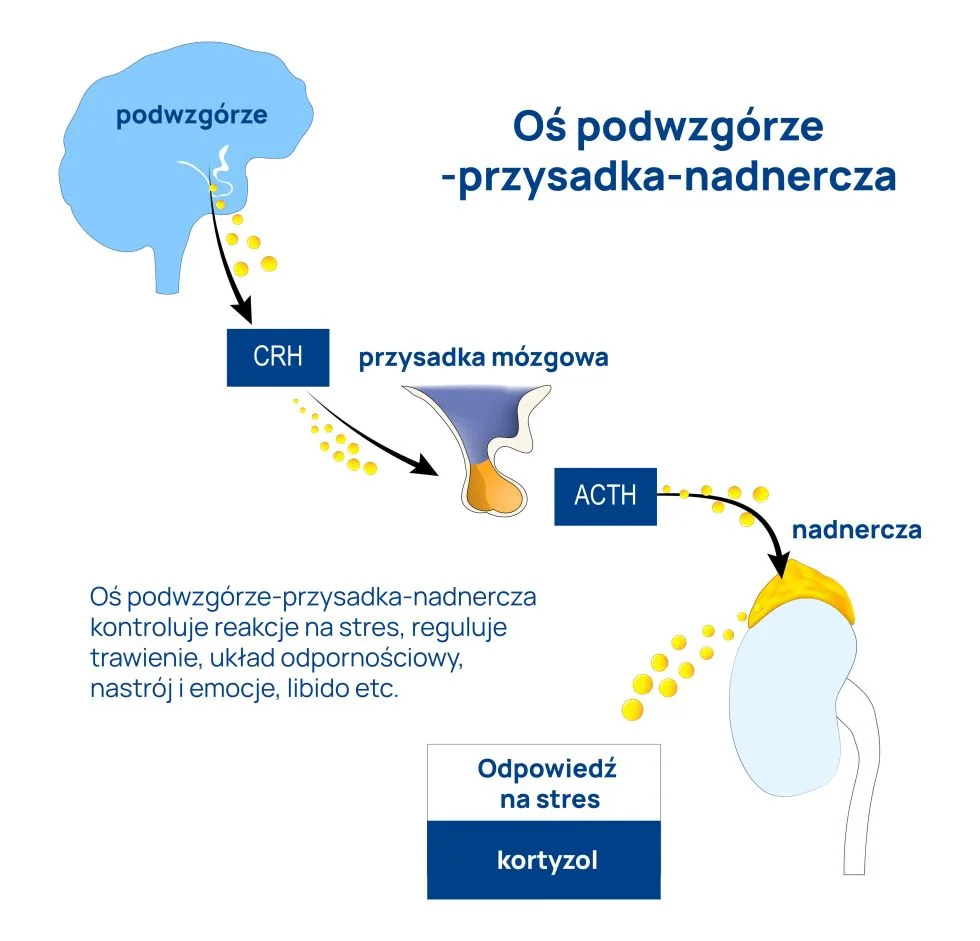
Podwzgórze wydziela hormon CRH (kortykoliberynę), który pobudza przysadkę do wydzielania ACTH. Ten ostatni działając na korę nadnerczy pobudza ją do wydzielania glikokortykosteroidów, głównie kortyzolu.
Kortyzol – jak działa hormon stresu?
Jaką rolę pełni kortyzol w sytuacji stresowej i dlaczego jest wówczas potrzebny w większych ilościach?
Kortyzol to hormon, który odpowiada za utrzymanie odpowiedniego poziomu glukozy we krwi. Robi to na trzy sposoby:
- pobudza organizm do wytwarzania większej ilości glukozy,
- ogranicza jej magazynowanie,
- hamuje produkcję insuliny.
W efekcie poziom glukozy (która jest głównym źródłem energii dla komórek nerwowych i mózgu) we krwi rośnie. Dzięki temu organizm może skutecznie działać w warunkach zwiększonej mobilizacji.
Ze względu na tę kluczową rolę w reakcji organizmu na stres, kortyzol jest wykorzystywany w badaniach laboratoryjnych jako wskaźnik poziomu stresu.
>> Dowiedz się więcej: Kortyzol – hormon stresu

Krzywa stresu – dystres i eustres
Stres i jego skutki są zazwyczaj kojarzone z konsekwencjami negatywnymi. Jednak należy podkreślić, iż stres – jako mechanizm mobilizujący organizm do działania – jest zjawiskiem korzystnym. Szkodliwe skutki stresu są widoczne, jeśli przeradza się on w zjawisko przewlekłe lub jest bardzo silny.
Można to prześledzić na wykresie krzywej stresu, która pokazuje dwie jego odsłony – dystres i eustres.
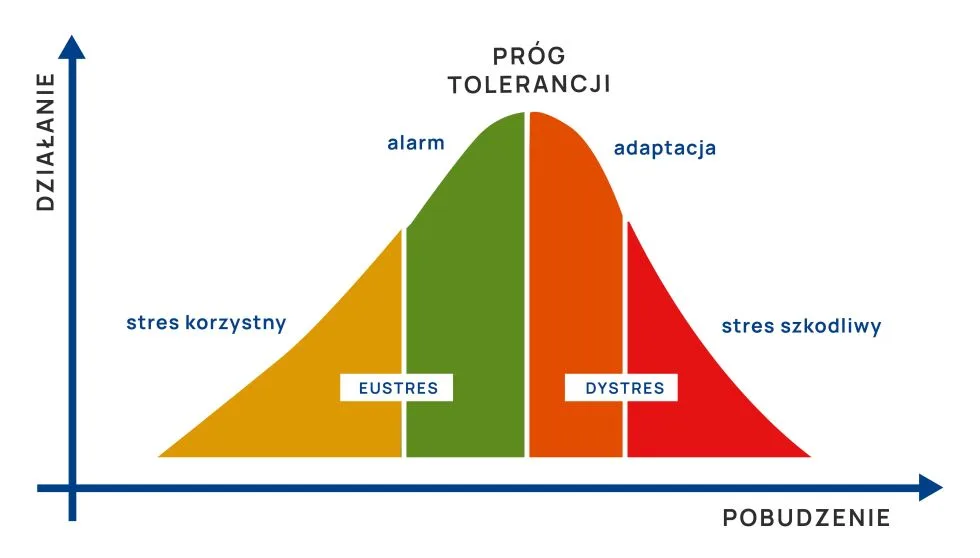
Eustres
Pierwszym etapem działania czynników stresogennych jest tzw. eustres (stres korzystny), który mobilizuje do działania. Obserwujemy lekkie pobudzenie, organizm uczy się, jak działać w nowych warunkach i bez większych problemów radzi sobie z powstającą presją. Jeśli na tym etapie stres nie jest bardzo silny lub długotrwały, organizm wraca do stanu wyjściowego i stres nie powoduje negatywnych skutków.
Jeśli natomiast stresor działa nadal, zasoby naszego organizmu zaczynają być na granicy wydolności, włącza się alarm. Jest to czas, kiedy powinniśmy pozwolić sobie na odpoczynek lub inną reakcję, która pomaga rozładować stres.
Dystres
Jeśli nie zareagujemy na stres na etapie alarmu, organizm przekracza swój próg tolerancji i zaczyna adaptować się do działania w stanie ciągłej mobilizacji, czyli w tzw. dystresie.
Adaptacja polega m.in. na ciągłym wydzielaniu substancji, które pomagają działać w warunkach stresu – adrenaliny i kortyzolu. Niestety, o ile krótkotrwałe ich działanie jest korzystne i mobilizuje nas do działania (np. poprzez pobudzenie, wzrost ciśnienia, wzrost poziomu glukozy jako substancji dostarczającej energii dla mózgu), to długotrwałe ich wydzielanie zaczyna niekorzystnie oddziaływać na nasze zdrowie:
- rozwija się nadciśnienie tętnicze, nietolerancja glukozy i cukrzyca,
- osłabia się działanie układu immunologicznego,
- spada odporność.
Dodatkowym efektem działania kortyzolu jest zwiększenie apetytu, gromadzenie tkanki tłuszczowej i rozwój otyłości brzusznej, co nakłada się na wcześniej opisane efekty długotrwałego stresu. To jest moment, kiedy zwykły relaks może już nie wystarczyć, a organizm nie jest w stanie sam sobie poradzić z efektem powstającej kuli śnieżnej. Jest to czas, kiedy powinniśmy poszukać porady specjalisty – psychologa lub psychiatry oraz zrobić badania laboratoryjne krwi, które pomogą w diagnozie i leczeniu towarzyszących chorób somatycznych.
Skutki stresu
Wpływ stresu na organizm człowieka jest sprawą indywidualną. To, co jest dużym stresem dla jednej osoby, wcale nie musi nim być dla kogoś innego. Dlatego, aby ułatwić specjalistom i pacjentom ocenę stresorów w życiu człowieka, w 1967 roku stworzono Social Readjustment Rating Scale (SRRS) – skala Holmesa i Rahe’a – proste narzędzie służące do oceny stresorów (sytuacji stresowych) i ich potencjalnego wpływu na zdrowie.
Skala uwzględnia 43 ważne wydarzenia życiowe przypisując im określoną liczbę punktów. Badania wskazują, iż kumulacja dużej liczby jednostek stresowych w ciągu roku lub dwóch lat, wiąże się z większym ryzykiem wystąpienia chorób somatycznych oraz problemów ze zdrowiem psychicznym.
Tabela – niektóre stresory w skali stresu Holmesa
| Życiowe wydarzenie | Jednostki stresowe |
| Śmierć współmałżonka | 100 |
| Rozwód | 73 |
| Separacja | 65 |
| Śmierć bliskiego członka rodziny | 63 |
| Poważny uraz lub choroba | 53 |
| Ślub | 50 |
| Utrata pracy | 47 |
| Emerytura | 45 |
| Choroba członka rodziny | 44 |
| Powikłania ciąży, komplikacje okołoporodowe | 40 |
| Poważne problemy małżeńskie | 39 |
| Zmiana kondycji finansowej | 38 |
| Zmiana pracy | 36 |
| Rozstanie z partnerem/partnerką | 35 |
| Znaczący kredyt | 31 |
| Wyprowadzka dorosłych dzieci z domu | 29 |
| Konflikty z teściami | 29 |
| Wybitne osobiste osiągnięcie | 28 |
| Ślub córki/syna | 26 |
| Rozpoczęcie lub zakończenie nauki w szkole | 26 |
| Zmiana warunków życia | 25 |
| Zmiana godzin lub warunków pracy | 20 |
| Zmiana miejsca zamieszkania | 20 |
| Zmiana szkoły | 20 |
| Zmiana w nawykach życia towarzyskiego | 18 |
| Zmiana nawyków snu | 16 |
| Zmiana nawyków żywieniowych | 15 |
| Wakacje/urlop | 13 |
| Święta – przygotowania, wydatki, spotkania | 12 |
| Nieznaczne naruszenie prawa | 11 |
Jak obliczyć poziom stresu?
Poziom stresu w skali Holmesa i Rahe’a oblicza się, sumując jednostki stresowe poszczególnych wydarzeń z życia w ciągu ostatnich dwunastu miesięcy. Ważne jest to, iż jeśli jakieś zdarzenie wystąpiło więcej niż jeden raz, np. zmiana pracy czy zmiana miejsca zamieszkania, każde z nich otrzymuje swoją osobną punktację.
Interpretacja wyników poziomu stresu:
- jeśli suma punktów jest niższa niż 150, oznacza to, iż stres u danej osoby jest na poziomie nieprzekraczającym możliwości adaptacji organizmu. Ryzyko rozwinięcia się chorób związanych ze stresem w ciągu najbliższych dwóch lat jest niskie.
- suma punktów pomiędzy 150-299 oznacza podwyższone ryzyko pojawienia się chorób związanych ze stresem w ciągu najbliższych dwóch lat. Stres jest istotnym czynnikiem wpływającym na stan zdrowia danej osoby.
- jeśli suma punktów wynosi 300 i więcej oznacza to wysokie ryzyko pojawienia się poważnych problemów zdrowotnych i sygnał do wprowadzenia zmian w stylu życia. Może to również oznaczać konieczność poszukania wsparcia psychologa i/lub psychiatry.
Długofalowe skutki stresu
Długofalowe skutki wysokiego poziomu stresu mogą mieć wpływ na cały organizm i stanowić poważny czynnik ryzyka wielu chorób.
Należą do nich:
- choroby układu sercowo-naczyniowego – nadciśnienie tętnicze, choroba niedokrwienna serca, zwiększone ryzyko zawału i udaru;
- choroby psychiczne – depresja, zaburzenia lękowe, zespół stresu pourazowego, zespół przewlekłego zmęczenia;
- zaburzenia metaboliczne – insulinooporność, cukrzyca t.2, otyłość brzuszna;
- osłabienie układu odpornościowego (obniżenie poziomu limfocytów) – częste i nawracające infekcje, choroby autoimmunologiczne (choroba Hashimoto, Graves-Basedowa);
- choroby przewodu pokarmowego – zespół jelita drażliwego, nasilenie nieswoistych chorób zapalnych jelit;
- zaburzenia cyklu menstruacyjnego u kobiet i zwiększenie ryzyka poronienia;
- zaburzenia ruchliwości i budowy plemników u mężczyzn – jedno z badań pokazało, że mężczyźni, którzy doświadczyli dwóch lub więcej stresujących wydarzeń życiowych w ciągu ostatniego roku w porównaniu z mężczyznami, u których nie wystąpiły żadne stresujące wydarzenia, mieli niższy odsetek ruchliwych plemników i niższy odsetek plemników o prawidłowej budowie morfologicznej;
- problemy skórne – nasilenie łuszczycy, AZS,
- przyspieszenie starzenia się organizmu i zwiększenie wieku biologicznego.
>> Warto przeczytać: Stres a poziom limfocytów. Jak długotrwały stres wpływa na odporność?

Objawy stresu
Objawy stresu, czyli reakcja organizmu na stres, obejmuje trzy grupy symptomów: fizyczne, emocjonalne i behawioralne.
Fizyczne objawy stresu
Fizyczne, czyli somatyczne symptomy stresu to:
- przyspieszona akcja serca, podwyższone ciśnienie tętnicze,
- przyspieszony i spłycony oddech,
- problemy żołądkowo-jelitowe – ból brzucha, biegunka, nudności, obniżony apetyt, zaburzenia połykania („gula” w gardle), suchość w ustach,
- zwiększone napięcie mięśni – karku, ramion, zaciskanie szczęki i żuchwy
- ból głowy,
- zwiększona potliwość.
Emocjonalne objawy stresu
Objawy emocjonalne to: trudności z pamięcią i koncentracją, nadmierna drażliwość, obniżony nastrój, odczuwanie niepokoju i lęku, gonitwa myśli.
>> Warto przeczytać: Stany lękowe – czym są i jakie są ich objawy? Przyczyny i leczenie
Behawioralne objawy stresu
W stanie stresu obserwuje się również zmiany w zachowaniu, nawykach i stylu życia. Mogą to być:
- problemy ze snem – trudności z zasypianiem, budzenie się w nocy, bezsenność
- spadek libido,
- skłonność do zwiększonej konsumpcji używek (alkohol, papierowy, kofeina), leków, substancji narkotycznych,
- problemy z odżywianiem – kompulsywne objadanie się, podjadanie w nocy, brak apetytu,
- unikanie kontaktów z ludźmi.
>> Sprawdź: Problemy z koncentracją, z czego mogą wynikać i jak znaleźć przyczynę?

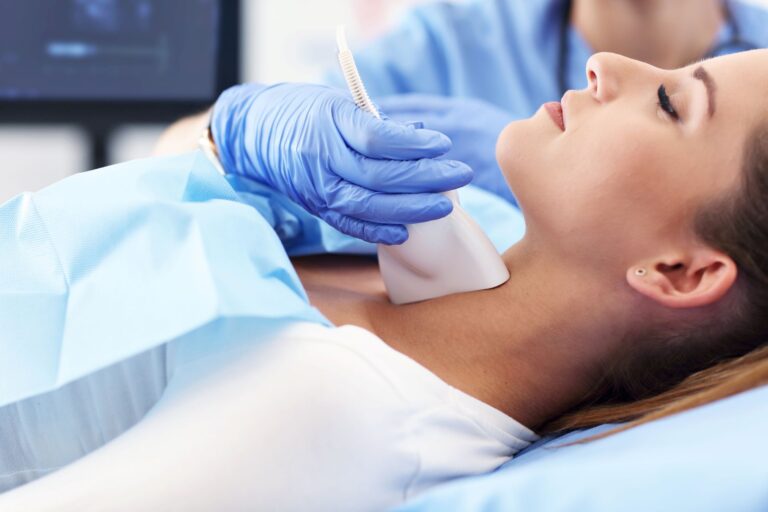
Stres – jakie badania laboratoryjne należy zrobić?
Badanie hormonu stresu
Jak napisaliśmy wyżej, markerem stresu jest kortyzol (hormon stresu) i to jest jedno z rekomendowanych badań. Oznaczanie poziomu kortyzolu we krwi nie zawsze wiąże się z znacznym podwyższeniem jego poziomu powyżej normy, czasem pozostaje on tuż powyżej górnej granicy wartości referencyjnych, utrzymując się na stale podwyższonym poziomie. Ponieważ kortyzol charakteryzuje się dobowym rytmem wydzielania, lepszy obraz profilu kortyzolu otrzymuje się badając jego profil dzienny w ślinie – wówczas widać jak kształtuje się stężenie hormonu stresu w ciągu całego dnia.
Badanie długości telomerów
Badaniem pomocnym w diagnostyce przewlekłego stresu jest badanie długości telomerów, czyli naszego wieku biologicznego. Jedną z przyczyn skracania się telomerów – a co za tym idzie wieku biologicznego – jest właśnie przewlekły stres.
Poziom stresu a ryzyko wystąpienia chorób
Biorąc pod uwagę fakt niekorzystnego działania stresu na układ sercowo-naczyniowy, odporność i wiele innych, należałoby wykonać panel testów, który wskaże, w jakiej kondycji są te parametry zdrowotne, które:
- mogą ulegać pogorszeniu pod wpływem przewlekłego stresu,
- wpływają na to, iż organizm ze stresem radzi sobie gorzej.
W ALAB laboratoria przygotowaliśmy trzy pakiety badań STRES, które można wykonać, gdy jesteśmy poddawani działaniu przewlekłego stresu.
- Pakiet STRES PODSTAWOWY STAN ZDROWIA przeznaczony jest dla pacjentów, którzy chcą skontrolować poziom tych parametrów krwi, które w stanie przewlekłego stresu mogą być zaburzone.
- Pakiet STRES oprócz ww. parametrów zawiera badanie poziomu kortyzolu oraz glutationu – najsilniejszego antyoksydantu naszego organizmu.
- Pakiet STRES KOMPLEKSOWY to szeroki wachlarz badań, w tym specjalistycznych, które głęboko wchodzą w diagnostykę stresu i jego skutków dla organizmu. Pakiet badań STRES KOMPLEKSOWY zawiera badania niestabilne, dlatego jest dostępny w wybranych punktach ALAB laboratoria.

Radzenie sobie ze stresem na co dzień
Ponieważ nie jesteśmy w stanie uniknąć stresu, umiejętność radzenia sobie w takich sytuacjach powinna być jedną z ważniejszych kompetencji współczesnego człowieka. Długofalowe sposoby na stres są pod ręką na co dzień, ważne jest aby mieć świadomość co może zadziałać i jak to zastosować.
Długofalowe sposoby na stres
Jeśli jesteśmy pod wpływem przewlekłego stresu należy postawić na wprowadzenie nawyków charakterystycznych dla zdrowego stylu życia. Na co zwracać uwagę?
- Zbilansowana dieta – jeśli długość telomerów jest pośrednim markerem działania przewlekłego stresu, to sposobem żywienia, który wpływa na wydłużenie się telomerów jest dieta śródziemnomorska. Badania wskazują, iż jest korzystna w radzeniu sobie ze skutkami skracania telomerów. Jest to dieta, która sprzyja również poprawie ogólnego stanu zdrowia, poprawia parametry metaboliczne, sprzyja zdrowiu przewodu pokarmowego i odbudowie prawidłowej mikrobioty.
- Aktywność fizyczna – umiarkowana aktywność fizyczna jest udowodnionym sposobem na wydłużenie telomerów i zapobieganie skutkom przewlekłego stresu. Rekomendacje mówią, iż aktywność powinna trwać co najmniej 150 minut tygodniowo, przy czym nie musi to być specjalny trening lub siłownia. Polecane są również spacery i robienie co najmniej 8 tys. kroków dziennie.
- Medytacja – liczne badania naukowe wspierają tezę, iż medytacja jest bardzo pomocną praktyką w radzeniu sobie z przewlekłym stresem. Medytacja pomaga m.in. obniżyć poziom kortyzolu, dzięki czemu uspokaja emocje oraz umysł. Medytacja ma wiele form, jedną z nich jest medytacja mindfulness, inną medytacja w jodze. Formą medytacji może być również modlitwa. Ważne jest, aby medytacja była regularnym rytuałem, w miarę możliwości praktykowanym codziennie.
Więcej o medytacji i o tym jak zacząć medytować w artykule: Medytacja – jak działa na stres? Czym jest medytacja, jak zacząć medytować?
- Prawidłowy oddech – współczesny człowiek często ma spłycony oddech oraz tzw. paradodkaslny tor oddychania. Powrót do prawidłowego toru oddechowego i oddychania przeponą jest również dobrą praktyką, wspomagającą niwelowanie skutków przewlekłego stresu.
Sposoby na stres – co robić, gdy zaczniesz się stresować?
Oddech na stres
Niezwykle pomocnym sposobem na bieżący stres jest oddech. Wydłużenie fazy wdechu i wydechu uspokaja umysł, spowalnia pracę serca i obniża ciśnienie tętnicze (zarówno skurczowe, jak i rozkurczowe).
Szczególnie polecaną techniką oddechową jest oddychanie lewą dziurką nosa, dzięki czemu zmniejsza się aktywność układu współczulnego i uspokaja reakcja „uciekaj lub walcz”.
W sytuacji stresowej należy:
- usiąść z prostym kręgosłupem – można siedzieć na krześle,
- zatkać kciukiem prawej dłoni prawe nozdrze,
- zacząć spokojnie i głęboko oddychać przez lewe nozdrze,
- skoncentrować uwagę na oddechu, powtarzając w myślach wdech-wydech,
- kontynuować oddech przez kilka minut.
>> Warto sprawdzić również: Jak prawidłowo oddychać? Jak oddychać przeponą?
Akupresura – punkty na stres
Innym polecanym sposobem jest uciskanie lub delikatny masaż punktów akupresurowych zlokalizowanych w różnych miejscach naszego ciała, które w tradycji medycyny chińskiej „uspokajają ducha”. Punktów, które wg przekazów mają takie działanie jest wiele, skoncentrujemy się na tych, które w sytuacji stresowej są łatwo dla nas dostępne – na głowie i rękach.
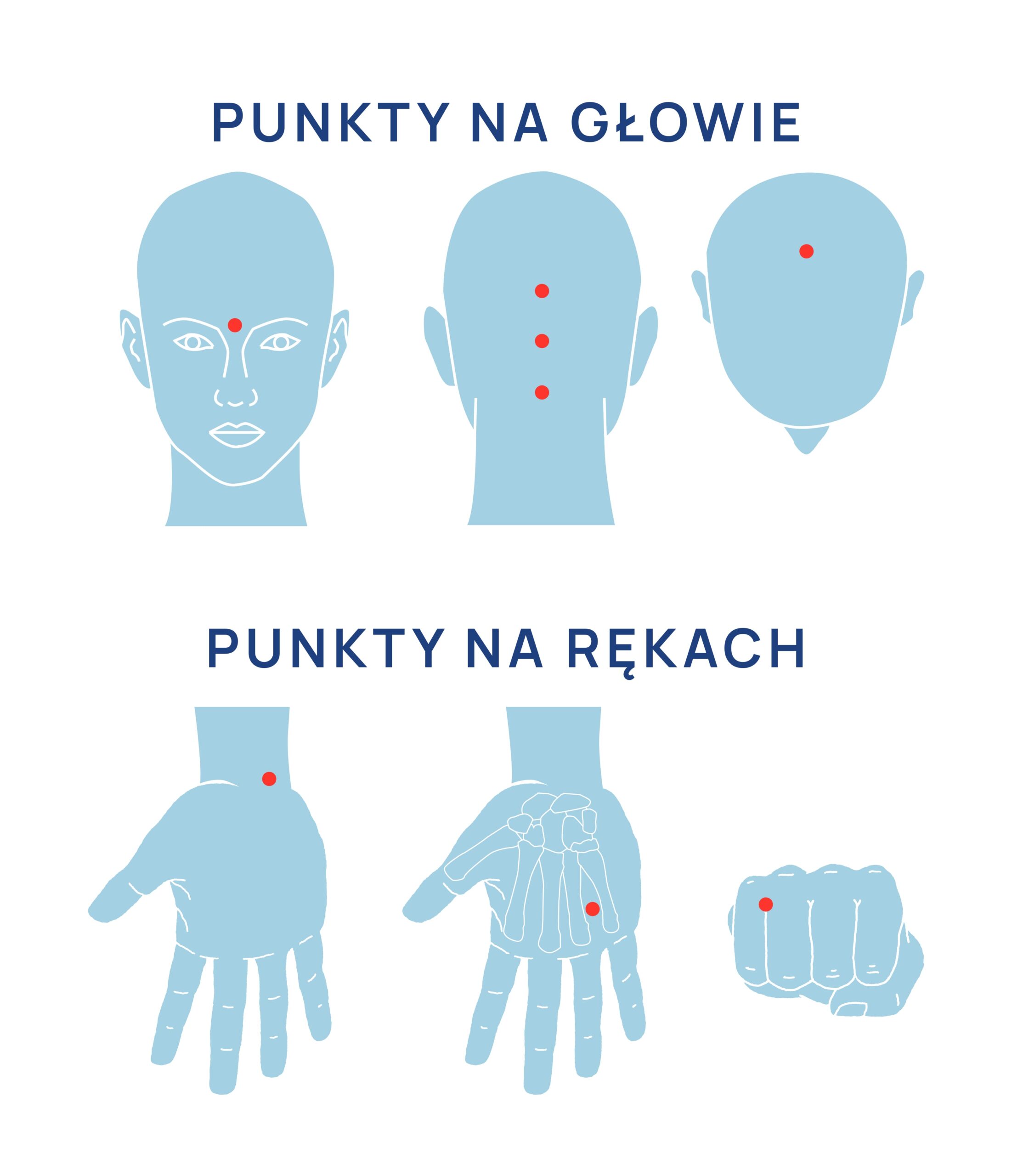
Punkty położone na głowie, które warto delikatnie stymulować – masować lub uciskać:
- punkt na czubku głowy – w tradycji chińskiej akupunktury nazywany punktem 100 tysięcy spotkań – jego stymulowanie pomaga zmniejszyć niepokój i oczyszcza umysł, pomaga skoncentrować uwagę na tu i teraz,
- trzy punkty położone z tyłu głowy – w linii środkowej. Pierwszy położony jest na tuż pod wypukłością kości potylicznej – guzkiem, który na ogół łatwo wyczuć. Pozostałe dwa punkty znajdziemy przesuwając się w kierunku czubka głowy ok. 3 cm powyżej punktu pierwszego (szerokość dwóch palców) – jest to meridian o nazwie „drzwi mózgu”, a ostatni powyżej 6 cm (szerokość czterech palców u dłoni);
- punkt między brwiami – punkt yintang – delikatny masaż uspokaja i relaksuje, pomaga również łagodzić ból głowy.
Punkty położone na kończynach górnych to:
- miejsce zlokalizowane na wewnętrznej krawędzi nadgarstka, po stronie łokciowej, w przedłużeniu małego palca, tuż pod wgłębieniem jednej z kości nadgarstka. Punkt nazywany „bramą ducha” jest najważniejszym punktem akupunkturowym, który wpływa na uspokojenie i regulację emocji,
- punkt położony pomiędzy podstawą 4 i 5 palca, powyżej krawędzi fałdu skóry, który je łączy,
- punkt na wewnętrznej stronie dłoni, w zagłębieniu pomiędzy czwartą i piątą kością śródręcza. W praktyce znajduje się w miejscu gdzie sięga czubek małego palca przy zaciśniętej pięści.
Zakończenie
Stres jest nieodłącznym towarzyszem życia współczesnego człowieka. Nie możemy go uniknąć, ale jesteśmy w stanie przeciwdziałać jego skutkom. Każdy z nas dysponuje narzędziami, które pomagają rozładować stres. Wiedza jakie to narzędzia i jak je stosować na co dzień, jest ważnym aspektem profilaktyki zdrowia.
Bibliografia
- McGonagle KA, Kessler RC. Chronic stress, acute stress, and depressive symptoms. Am J Community Psychol. 1990 Oct;18(5):681-706. doi: 10.1007/BF00931237. PMID: 2075897.
- Janevic T, Kahn LG, Landsbergis P, Cirillo PM, Cohn BA, Liu X, Factor-Litvak P. Effects of work and life stress on semen quality. Fertil Steril. 2014 Aug;102(2):530-8. doi: 10.1016/j.fertnstert.2014.04.021. Epub 2014 May 23. PMID: 24856463; PMCID: PMC4382866.
- Santos J., Maran P.L., Rodriguez-Urrutia A. Stress, microbiota, and the gut-brain axis in mental and digestive health. Medicina Clinica. 2025;164:295-304.
- Holmes TH, Rahe RH, The social readjustment rating scale, Journal of Psychosomatic Research, Volume 11, Issue 2,1967, Pages 213-218, ISSN 0022-3999, https://doi.org/10.1016/0022-3999(67)90010-4.
- Sosnowski T., Zadania umysłowe a aktywność sercowo-naczyniowa, Gdańskie Wydawnictwo Psychologiczne, Sopot 2002.
- Deadman P, Al-Khafaji M, Baker K, Podręcznik Akupunktury, Wydawnictwo Galaktyka, Łódź 2023.
- Vanutelli ME, Grigis C, Lucchiari C. Breathing Right… or Left! The Effects of Unilateral Nostril Breathing on Psychological and Cognitive Wellbeing: A Pilot Study. Brain Sci. 2024 Mar 23;14(4):302. doi: 10.3390/brainsci14040302. PMID: 38671954; PMCID: PMC11048276.