Artykuł powstał 02.09.2020 r., ostatnia aktualizacja: 24.04.2026 r.
Jeśli zaczynamy przybierać na wadze lub nadmiernie chudnąć, przyjaciółki mówią nam „zbadaj tarczycę”. Gdy ciągle chce nam się spać, jesteśmy zmęczeni, wypadają nam włosy, doktor Google podpowiada „zbadaj tarczycę”. Czy mają rację? Czym jest tarczyca? Jakie mogą być choroby tarczycy? Jakie badania tarczycy możemy zrobić, żeby sprawdzić czy funkcjonuje prawidłowo? Na te i inne pytania postaramy się odpowiedzieć w poniższym artykule.
| Z tego artykułu dowiesz się: >> jakie badania tarczycy wykonuje się w diagnostyce tego narządu, >> czym jest badanie TSH, >> dlaczego oznaczenie wolnych hormonów tarczycy (fT4 i fT3) lepiej odzwierciedla funkcje tarczycy niż hormony T3 i T4, >> jakie pakiety tarczycowe można wykonać w ALAB laboratoria i który pakiet wybrać. |
Spis treści:
- Co to jest tarczyca? Jakie funkcje pełnią hormony tarczycy?
- Tarczyca – jakie hormony produkuje?
- Badania tarczycy – jakie parametry mają znaczenie w diagnostyce?
- TSH – hormon przysadki mózgowej, będący podstawowym badaniem tarczycy
- fT3 i fT4 – podstawowe hormony w diagnostyce tarczycy
- Badanie poziomu jodu a diagnostyka chorób tarczycy
- Badania tarczycy – jakie choroby można wykryć?
- Jakie inne badania wykonuje się w diagnostyce chorób tarczycy?
- Pakiet tarczycowy ALAB – jakie badania obejmuje?
- Zakończenie
Co to jest tarczyca? Jakie funkcje pełnią hormony tarczycy?
Zdrowa tarczyca to niewielki gruczoł, który ma objętość do 20 ml u kobiet i do 25 ml u mężczyzn. Położona jest w obrębie szyi, tuż za naszą tchawicą, a jej kształt często porównuje się do kształtu motyla. Tarczyca produkuje kilka hormonów, a pomiar ich poziomu to podstawowe badania laboratoryjne tarczycy.

Tarczyca – jakie hormony produkuje?
Głównym hormonem wytwarzanym przez tarczycę jest tyroksyna T4. Stanowi 85% objętości wszystkich hormonów, które są przez ten narząd produkowane. Druga w kolejności jest trójodotyronina T3, poza tym tarczyca produkuje śladowe ilości tzw. odwrotnej trójodotyroniny rT3 oraz kalcytoniny. W diagnostyce chorób tarczycy znaczenie mają dwa pierwsze hormony.
T4, czyli tyroksyna, jest pulą magazynową tarczycy. Organizm wykorzystuje tę pulę w momencie, gdy jest to potrzebne do prawidłowego funkcjonowania i przetwarza ją na postać aktywną, czyli T3 – trójodotyroninę.
>> Warto przeczytać również: Choroby tarczycy i badanie rT3 – co warto wiedzieć?
Badania tarczycy – jakie parametry mają znaczenie w diagnostyce?
Jakie badania można zrobić, aby zbadać tarczycę? Należą do nich hormony, zarówno te produkowane w samej tarczycy, jak i TSH – hormon produkowany przez przysadkę mózgową. Ważnym elementem diagnostyki tego gruczołu bywa również oznaczanie poziomu jodu.
TSH – hormon przysadki mózgowej, będący podstawowym badaniem tarczycy
TSH jest hormonem stosowanym do diagnostyki tarczycy, chociaż nie jest przez nią produkowane. Jak to zatem możliwe, że hormon powstający poza tarczycą może świadczyć o jej funkcjonowaniu? Otóż TSH powstaje w przysadce mózgowej, która bywa nazywana „centrum dowodzenia” gruczołami dokrewnymi, ponieważ jest odpowiedzialna za wydzielanie i magazynowanie kilkunastu hormonów. Jednym z nich jest TSH, od którego zależy praca tarczycy.
Wydzielanie TSH pobudza tarczycę do produkcji i wydzielania hormonów T4 oraz T3. Jeśli stężenie tych hormonów we krwi zaspokaja potrzeby organizmu, przysadka dostaje informację zwrotną, iż może przestać produkować TSH. Jeśli zaś zaczyna ich być za mało, jest to dla przysadki sygnał, że musi się zabrać do pracy i produkować więcej TSH. Jest to mechanizm tzw. sprzężenia zwrotnego.
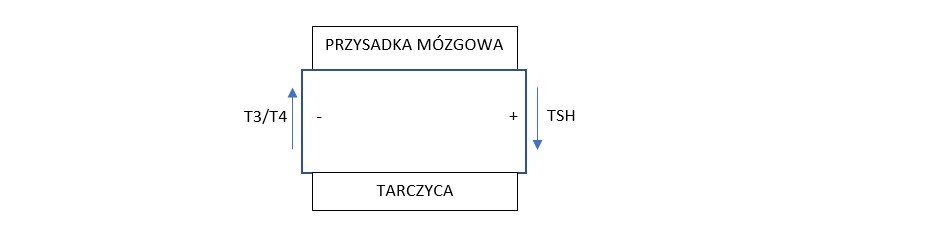
W sytuacji, gdy chora tarczyca zaczyna się buntować i wydziela za mało lub za dużo T4 i T3 jest to sygnałem dla przysadki, aby zmniejszyła lub zwiększyła produkcję TSH. Ma to swoje odzwierciedlenie w poziomie tego hormonu we krwi, dlatego jest on stosowany jako jeden z markerów diagnostyki tarczycy. Na dodatek jest to marker bardzo czuły, bo nawet niewielkie spadki czy wzrosty poziomu hormonów tarczycy mają odzwierciedlenie w produkcji TSH.
>> Dowiedz się więcej: Co to jest TSH i jaką rolę pełni w organizmie?
fT3 i fT4 – podstawowe hormony w diagnostyce tarczycy
Hormony tarczycy we krwi mogą mieć dwie postaci:
W ofertach laboratorium można zbadać obydwa rodzaje tych parametrów, jednak należy mieć świadomość, iż hormony związane z białkami są nieaktywne i stanowią odzwierciedlenie całkowitej ich puli dostępnej w organizmie. Jednak w celu sprawdzenia rzeczywistego obrazu aktywności tarczycy należy oznaczać poziom hormonów w postaci wolnej, czyli fT4 i fT3.
>> Może Cię zainteresować: Układ hormonalny człowieka. Budowa, funkcje, hormony
Badanie poziomu jodu a diagnostyka chorób tarczycy
Jod jest niezbędny do produkcji hormonów tarczycy. Punktem wyjścia do ich wytworzenia, czyli substratem, jest aminokwas tyrozyna, hormony tarczycy powstają poprzez przyłączanie jodu do tyrozyny.
Dlatego niedobór jodu jest czynnikiem, który w sposób kluczowy wpływa na pracę tarczycy.
Większość jodu w naszym organizmie gromadzona jest właśnie w tarczycy, natomiast wydalana jest głownie przez nerki. Dlatego, jeśli chcemy ocenić poziom jodu i sprawdzić, czy mamy jego niedobory, należy zrobić badanie stężenia jodu w moczu. Jest to najlepsza metoda, aby zdiagnozować niedobory tego pierwiastka i ocenić w jakim stopniu mogą one wpływać na pracę tarczycy.
Badania tarczycy – jakie choroby można wykryć?
Badania tarczycy pomagają w diagnostyce chorób, w których zaburzona jest ilość produkowanych hormonów. Jest to przede wszystkim nadczynność lub niedoczynność tarczycy, również jej subkliniczne postacie. Pomagają także w ocenie funkcji tarczycy w chorobie Hashimoto czy u kobiet w ciąży. Uproszczona interpretacja widoczna jest w tabeli.
| Poziom TSH | Poziom fT4 | Co może oznaczać? |
| obniżony | podwyższony | nadczynność tarczycy/ początek choroby Hashimoto |
| obniżony | norma | subkliniczna nadczynność tarczycy / ciążą |
| obniżony | obniżony | dysfunkcja przysadki lub podwzgórza |
| norma | obniżony | niedobór jodu, zwłaszcza przy podwyższonym fT3 |
| podwyższony | obniżony | niedoczynność tarczycy / choroba Hashimoto |
| podwyższony | norma | subkliniczna niedoczynność tarczycy / otyłość |
| podwyższony | podwyższony | guz przysadki |

Jakie inne badania wykonuje się w diagnostyce chorób tarczycy?
Choroby tarczycy wiążą się nie tylko z nieprawidłowym wydzielaniem hormonów, ale również zmianami zapalnymi, zmianami w wielkości narządu, zmianami jego struktury czy guzkami tarczycy.
Dlatego w badaniach na tarczycę zastosowanie mają również oznaczenia poziomów przeciwciał, a także badania obrazowe, np. USG tarczycy.
Pakiet tarczycowy ALAB – jakie badania obejmuje?
Badania laboratoryjne tarczycy wykonuje się najczęściej w panelu. Wybór odpowiednich badań zależy od celu diagnostycznego. W ofercie ALAB jest cały szereg pakietów tarczycowych, obejmujących różne badania. Przewodnik jaki pakiet tarczycowy wybrać prezentujemy poniżej.
| DLA KOGO? | JAKI PAKIET WYBRAĆ? | BADANIA W PAKIECIE? |
| Jestem w ciąży, monitoruję funkcję tarczycy | PAKIET TARCZYCOWY PRZESIEWOWY I DLA KOBIET W CIĄŻY | TSH, fT4 |
| Chcę zbadać tarczycę profilaktycznie, nie mam żadnych objawów, w rodzinie nie występują choroby tarczycy | ||
| Chcę zbadać tarczycę profilaktycznie, nie mam żadnych objawów, w rodzinie występują choroby tarczycy | PAKIET TARCZYCOWY | TSH, fT4, fT3 |
| Chcę zbadać tarczycę, ponieważ odczuwam objawy mogące świadczyć o chorobie tarczycy | ||
| Badanie funkcji tarczycy zasugerował mi lekarz/dietetyk | ||
| Monitoruję leczenie niedoczynności/nadczynności tarczycy | ||
| Chcę zbadać funkcję tarczycy oraz sprawdzić poziom przeciwciał | PAKIET TARCZYCOWY ROZSZERZONY | TSH, fT4, fT3, przeciwciała anty-TPO i anty- Tg, TRAb |
| Chcę wykonać kompleksowe badanie tarczycy, ponieważ u mnie w rodzinie występuje ch. Hashimoto i/lub Graves-Basedowa | ||
| Chcę rozpocząć lub już prowadzę suplementację witamin i/lub pierwiastków wspierających funkcje tarczycy | PAKIET SUPLEMENTACJA W CHOROBACH TARCZYCY | cynk, selen, ferrytyna, wit. D, wit. B12. |
| Mam podejrzenie choroby Hashimoto | PAKIET HASHIMOTO | TSH, fT4, fT3, przeciwciała anty-TPO i anty- Tg |
| Mam podejrzenie niedoczynności tarczycy z powodu Hashimoto | ||
| Mam problemy z zajściem w ciążę i/lub donoszeniem ciąży | ||
| Mam podejrzenie choroby Hashimoto, chcę również zbadać czy nie mam niedoborów selenu i wit. D3 | PAKIET HASHIMOTO ROSZERZONY | TSH, fT4, fT3, przeciwciała anty-TPO i anty- Tg, selen, wit.D3 |
| Monitoruję suplementację selenu i wit. D3 w chorobie Hashimoto | ||
| Mam podejrzenie choroby Graves-Basedowa | PAKIET GRAVES-BASEDOWA | TSH, fT4, fT3, przeciwciała TRAb |
| Mam podejrzenie nadczynności tarczycy z powodu choroby Graves-Basedowa | ||
| Mam podejrzenie choroby Graves-Basedowa, chcę również zbadać czy nie mam niedoborów selenu i wit. D3 | PAKIET GRAVES-BASEDOWA ROZSZERZONY | TSH, fT4, fT3. przeciwciała TRAb, selen, wit. D3 |
| Monitoruję suplementację selenu i wit. D3 w chorobie Graves-Basedowa | ||
| Chcę wykonać kompleksowy zestaw badań laboratoryjnych funkcji tarczycy, komplet przeciwciał oraz diagnostykę istotnych niedoborów w diecie | PAKIET TARCZYCOWY KOMPLEKSOWY | TSH, fT4, fT3, przeciwciała anty-TPO, anty- Tg, TRAb selen, wit.D3, jod w moczu |
Zakończenie
Badania laboratoryjne tarczycy to bardzo ważny element diagnostyki chorób tego narządu, a także monitorowania leczenia. Odpowiednio dobrane badania wspomagają precyzyjną diagnozę. W badaniach tarczycy często trzeba oznaczyć kilka parametrów, dlatego warto skorzystać z gotowych pakietów badań.
Bibliografia
- https://podyplomie.pl/wiedza/wielka-interna/1289,diagnostyka-laboratoryjna-chorob-tarczycy (dostęp 23.04.2026)