Artykuł powstał 18.08.2022 r., ostatnia aktualizacja: 20.04.2026 r.
Bakterie z gatunku Helicobacter pylori są powszechną przyczyną zakażeń przewodu pokarmowego. W Polsce problem ten dotyczy większości populacji dorosłych.Chociaż zakażenie przebiega zazwyczaj bezobjawowo, u 20-30% zainfekowanych pojawiają się symptomy choroby. Nieleczona infekcja Helicobacter pylori może prowadzić do powstania wrzodów żołądka i dwunastnicy oraz do rozwoju raka żołądka i chłoniaka MELT.
| Z tego artykułu dowiesz się: >> czym jest Helicobacter pylori, >> jak dochodzi do zakażenia Helicobacter pylori, >> jakie objawy chorobowe mogą świadczyć o infekcji Helicobacter pylori, >> na czym polega diagnostyka w kierunku Helicobacter pylori, >> czy zakażenie Helicobacter pylori jest uleczalne, >> jak zabezpieczyć się przed zakażeniem Helicobacter pylori. |
Spis treści
- Epidemiologia zakażenia bakterią Helicobacter pylori
- Helicobacter pylori – co to za bakteria i gdzie występuje?
- Skąd się bierze Helicobacter pylori? Drogi zakażenia
- Helicobacter pylori – objawy zakażenia
- Diagnostyka Helicobacter pylori – jakie badania na Helicobacter należy wykonać?
- Helicobacter pylori – leczenie zakażenia
- Profilaktyka zakażenia Helicobacter pylori
- Zakończenie
- Helicobacter – sekcja FAQ
Epidemiologia zakażenia bakterią Helicobacter pylori
Helicobacter pylori jest powszechną przyczyną zakażeń przewodu pokarmowego u ludzi. Szacuje się, że ok. 50% populacji świata jest nosicielami tej baterii. W Polsce problem nosicielstwa dotyczy 70-80% populacji osób dorosłych i 30% dzieci. Chociaż zakażenie przebiega zwykle bezobjawowo, u 20-30% zainfekowanych pojawiają się symptomy choroby. U ok. 1% osób poddanych skutecznej terapii dochodzi do powtórnego zakażenia.
>> Może Cię zainteresować: Budowa, funkcje i najczęstsze choroby układu pokarmowego człowieka
Helicobacter pylori – co to za bakteria i gdzie występuje?
Helicobacter pylori jest spiralną bakterią, która ma zdolność przenikania w głąb błony śluzowej układu pokarmowego. Bakteria wykrywana jest przede wszystkim w dalszej części żołądka, ale wykazano, że może zakażać również inne tkanki. Obecność Helicobacter pylori w żołądku wynika ze specyficznych cech drobnoustroju, zdolnego do bytowania i rozwoju w nieprzyjaznym środowisku o niskim pH.
Zakażenie Helicobacter pylori związane jest z chorobą wrzodową żołądka i dwunastnicy, ponieważ bakterie wykrywa się u ok. 70-80% osób z tymi schorzeniami. Nieleczona infekcja może prowadzić do rozwoju raka żołądka, czemu sprzyja przewlekły stan zapalny błony śluzowej. W przypadku osób z wrzodem żołądka o etiologii Helicobacter pylori, ryzyko transformacji nowotworowej jest dwukrotnie większe. Rak jelita cienkiego, w tym dwunastnicy jest rzadkością.
Skąd się bierze Helicobacter pylori? Drogi zakażenia
Jedynym rezerwuarem Helicobacter pylori jest człowiek. Do zakażenia dochodzi zazwyczaj w dzieciństwie wraz z wiekiem wzrasta odsetek osób zainfekowanych. Do przenoszenia bakterii dochodzi głównie drogą pokarmową na skutek używania wspólnych naczyń, picia z tych samych butelek, pocałunków z osobą zakażoną. Możliwa jest również droga fekalno-oralna.
Główne przyczyny zakażenia Helicobacter pylori:
- zaniedbywanie higieny osobistej,
- złe warunki sanitarne,
- niski status socjalno-ekonomiczny,
- spożywanie zanieczyszczonych pokarmów,
- skażona woda,
- wiek (do zakażenia dochodzi głównie w dzieciństwie),
- uwarunkowania genetyczne.
| Czy wiesz, że…? Rozprzestrzenianie się zakażenia Helicobacter pylori jest parokrotnie większe w krajach rozwijających się niż w krajach rozwiniętych. |
>> Sprawdź też nasz artykuł: Choroba wrzodowa, dyspepsja, infekcja Helicobacter pylori – diagnostyka i postępowanie
Helicobacter pylori – objawy zakażenia
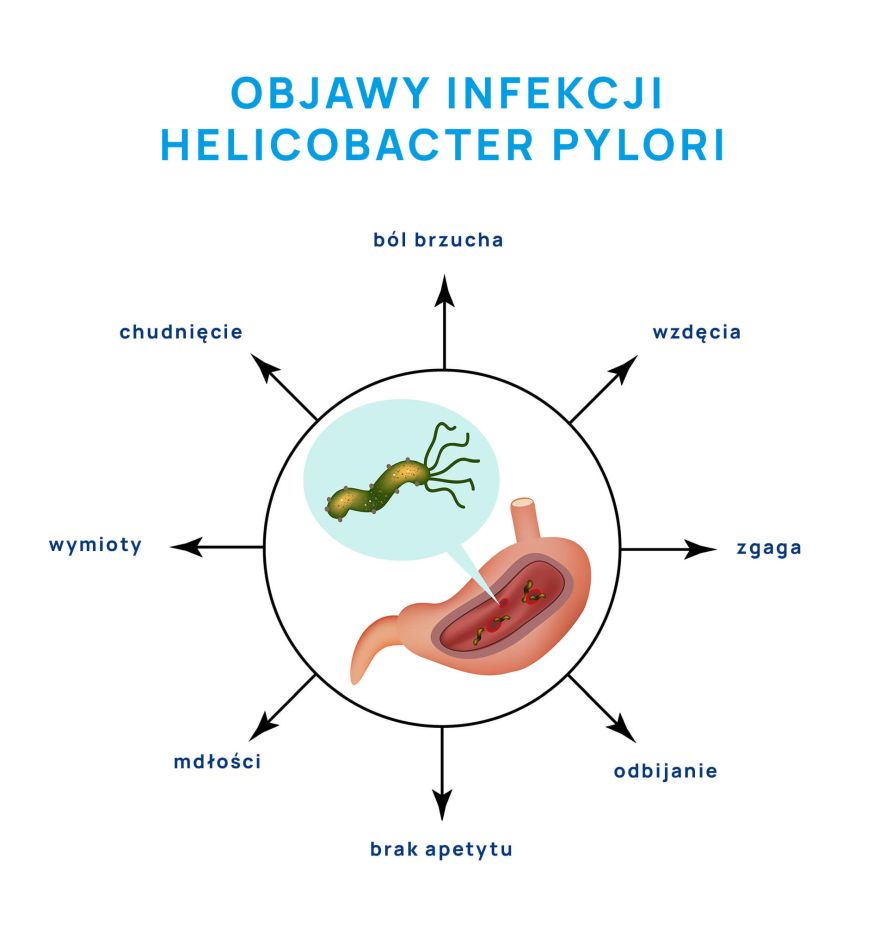
W większości przypadków zakażenie Helicobacter pylori przebiega bezobjawowo, ale u niektórych osób mogą pojawić się symptomy choroby. W przebiegu infekcji mogą pojawić się:
- ból brzucha,
- wzdęcia,
- zgaga,
- odbijanie,
- brak apetytu,
- mdłości,
- niestrawność,
- nudności,
- wymioty,
- spadek wagi.
Początkowo łagodne symptomy choroby mogą szybko mijać, jednak bez leczenia odpowiednimi antybiotykami bakterie nie są eliminowane. Nawroty objawów infekcji z czasem stają się coraz bardziej dotkliwe. Wrzody dwunastnicy i wrzody żołądka mogą dawać silne bóle brzucha po jedzeniu, wzdęcia i uczucie pełności.
Diagnostyka Helicobacter pylori – jakie badania na Helicobacter należy wykonać?
Wskazaniami do wykonania badań w kierunku zakażenia Helicobacter pylori są:
- aktywna lub przebyta choroba wrzodowa,
- wczesny rak żołądka,
- rak żołądka u bliskich krewnych,
- chłoniak MALT,
- dyspepsja,
- planowane długotrwałe leczenie niesteroidowymi lekami przeciwzapalnymi,
- niedokrwistość z powodu niedoboru żelaza o nieznanej etiologii,
- niedobór witaminy B12.
W wykrywaniu zakażenia Helicobacter pylori stosowane są zarówno inwazyjne, jak i nieinwazyjne metody diagnostyczne.
>> Może Cię zainteresować: Witamina B12 a nowotwory
Badanie na Helicobacter – metody nieinwazyjne
Metody nieinwazyjne zalecane są osobom bez objawów alarmowych i bez wywiadu rodzinnego w kierunku nowotworów przewodu pokarmowego. Badania powinny być wykonywane w laboratorium, gdzie interpretowane są przez diagnostę laboratoryjnego.
Testy na obecność antygenów H.pylori w kale
Testy wykonywane z kału służą do diagnozowania aktywnego zakażenia H.pylori oraz do oceny skuteczności leczenia.
- Helicobacter pylori w kale – antygen – metoda automatyczna
Test wykonywany jest metodą chemiluminescencji (CLIA) z zastosowaniem specyficznych przeciwciał monoklonalnych. Wynik przedstawiany jako ujemny, dodatni lub niejednoznaczny w oparciu o stężenia antygenów w badanej próbce kału.

- Helicobacter pylori w kale – antygen – metoda manualna
Test wykonywany jest szybką metodą immunochromatograficzną (kasetkową), wykorzystującą powinowactwo specyficznych przeciwciał do antygenów H.pylori. Powstające w przypadku zakażenia kompleksy antygen-przeciwciało uwidaczniają się na membranie testowej w postaci barwnej linii.
>> Warto przeczytać również: Badanie kału w kierunku pasożytów. Jak się przygotować, ile trwa, co wykrywa? Fakty i mity
Test serologiczny na obecność przeciwciał w klasie IgG
Test wykonywany jest z surowicy krwi i ma zastosowanie u chorych, którzy są w w trakcie leczenia lub po niedawnym leczeniu IPP (inhibitorami pompy protonowej) i antybiotykami. Może być wykorzystany również u pacjentów z aktywnym lub niedawno przebytym krwawieniem z wrzodu żołądka, zanikowym zapaleniem błony śluzowej żołądka lub nowotworem. Badanie nie nadaje się do potwierdzenia eradykacji bakterii – przeciwciała mogą być wykrywane po roku od wyleczenia, a nawet dłużej.
Testy oddechowe z mocznikiem znakowanym 13C lub 14C
Test oddechowy oparty jest na reakcji chemicznej rozkładu mocznika przez ureazę H.pylori do NH3i CO2. Pacjent przed wykonaniem badania spożywa mocznik znakowany nieradioaktywnym izotopem 13C lub radioaktywnym izotopem 14C. Wzrost stężenia 13CO2 lub dodatni wynik oznaczenia 14CO2 wwydychanym powietrzu świadczy o obecności H. pylori. Metoda stosowana jest do zarówno potwierdzenia zakażenia, jak i do kontroli eradykacji bakterii.
>> Zobacz też nasz artykuł: Najczęstsze nowotwory u kobiet i mężczyzn
Badanie na Helicobacter – metody inwazyjne
Metody inwazyjne, wymagające endoskopowego pobrania wycinka, powinny być wykonywane u osób z alarmowymi objawami i u pacjentów z wywiadem rodzinnym w kierunku nowotworów przewodu pokarmowego.
Test urazowy
Badanie wymaga pobrania wycinków błony śluzowej żołądka w trakcie gastroskopii. Wycinki umieszczane są na specjalnej płytce zawierającej mocznik z dodatkiem chromogenu. Test urazowy wykorzystuje zdolność H. pylori do rozkładania mocznika. W przypadku obecności bakterii bibułka wskaźnikowa zmienia zabarwienie.
>> Warto przeczytać też: Przygotowanie do gastroskopii – przygotowanie i zalecenia oraz dieta
Hodowla
Metoda polega na przeniesieniu wycinków pobranych w trakcie gastroskopii na specjalne podłoże do hodowli bakterii. Badanie może być przydatne w przypadku niepowodzeń terapeutycznych dla oceny wrażliwości szczepów H.pylori na antybiotyki. Metoda jest rzadko stosowana ze względu na czasochłonność, koszty i ograniczony dostęp do pracowni mikrobiologicznych wykonujących tego typu diagnostykę.
| UWAGA: Nie należy przyjmować IPP przez 7-14 dni przed testami: oddechowym, antygenowym i urazowym. |
Helicobacter pylori – leczenie zakażenia
Leczenie ma na celu eradykację (eliminację) bakterii z organizmu i jest zalecane w każdym przypadku stwierdzenia zakażenia Helicobacter pylori. Terapia obejmuje podawanie kilku leków przeciwdrobnoustrojowych oraz leków z grupy inhibitorów pompy protonowej (IPP), które hamują wydzielanie kwasu solnego w żołądku. Skuteczność leczenia, przy przestrzeganiu zaleceń, wynosi ponad 90%. U ok. 1% po eradykacji bakterii dochodzi do ponownego zakażenia.
Schemat pierwszego wyboru leczenia zakażenia Helicobacter pylori (terapia14-dniowa):
- terapia poczwórna z bizmutem (zalecana w Polsce)
- lek z grupy inhibitorów pompy protonowej (IPP),
- cytrynian bizmutu,
- dwa antybiotyki (metronidazol, tetracyklina).
- terapia poczwórna bez bizmutu (przy braku dostępu do bizmutu)
- lek z grupy inhibitorów pompy protonowej (IPP),
- trzy antybiotyki (amoksycylina, metronidazol, klarytromycyna).
- terapia potrójna (możliwe niepowodzenia ze względu na narastającą oporność H.pylori na klarytromycynę)
- lek z grupy inhibitorów pompy protonowej (IPP),
- dwa antybiotyki (amoksycylina lub metronidazol, klarytromycyna).
Przy nieskuteczności leczenia zakażenia Helicobacter pylori podaje się leki drugiego wyboru, a przy dwukrotnym niepowodzeniu terapii należy ocenić wrażliwość bakterii na antybiotyki i leczyć zgodnie z wynikiem antybiogramu.
| Warto wiedzieć: W większości przypadków nie ma konieczności kontroli skuteczności terapii, jeżeli jednak wykonuje się takie badanie, test należy przeprowadzić po miesiącu od zakończenia leczenia. |
Profilaktyka zakażenia Helicobacter pylori
Nie istnieje swoista profilaktyka zakażeń Helicobacter pylori. Mimo że nie ma ustalonych zasad zapobiegania zakażeniom, dla uniknięcia infekcji H.pylori zaleca się:
- przestrzegania podstawowych zasad higieny,
- dbałość o standard sanitarny otoczenia, szczególnie w dużych skupiskach ludzi,
- unikanie współużywania naczyń, sztućców, picia z tych samych butelek,
- dietę bogatą w witaminy C i E, beta-karoten,
- karmienie dziecka piersią.
>> Sprawdź: Witamina C – niewielka cząsteczka o wielkim znaczeniu
Zakończenie
Zakażenia układu pokarmowego Helicobacter pylori są bardzo powszechne. Mimo że u większości osób zakażenie przebiega bezobjawowo, u niektórych osób może dojść do rozwoju choroby. Konsekwencją przewlekłego stanu zapalnego żołądka wywołanego przez H.pylori mogą być wrzody żołądka i dwunastnicy, rak żołądka, chłoniak MALT.
Osoby z potwierdzonym zakażeniem wymagają podjęcia terapii, która przy przestrzeganiu zaleceń lekarskich ma ponad 90% skuteczność. Do wykrycia infekcji stosowane są inwazyjne i nieinwazyjne metody diagnostyczne.
Helicobacter– sekcja FAQ
Nieleczona choroba wywołana przez Helicobacter pylori prowadzi do przewlekłego stanu zapalnego żołądka, choroby wrzodowej żołądka i dwunastnicy. Zwiększa też ryzyko rozwoju nowotworów – raka żołądka i chłoniaka MALT.
Tak, przy zakażeniu Helicobacter pylori mogą wystąpić zaparcia. Jest to spowodowane zmianami składu mikrobioty jelitowej oraz zaburzeniami trawienia wynikającymi z przewlekłej infekcji.
Do zakażenia Helicobacter pylori może dojść na skutek bliskich kontaktów z osobą zakażoną – współużywania naczyń, sztućców, picia z tej samej butelki, pocałunków, oblizywania smoczków. Do szerzenie bakterii dochodzi również drogą fekalno-oralną poprzez brudne ręce, spożywanie niemytych owoców i warzyw.
Refluks żołądkowy i infekcja Helicobacter pylori mają różne przyczyny i wymagają odmiennego leczenia. W zakażeniu H.pylori dochodzi do uszkodzenia ściany żołądka na skutek miejscowej reakcji zapalnej, w refluksie kwas żołądkowy wielokrotnie cofa się do przełyku podrażniając jego błonę śluzową. Infekcja Helicobacter pylori może nasilać refluks.
Bibliografia
- lek. Magdalena Wiercińska „Helicobacter pylori (H. pylori) – objawy zakażenia bakterią, testy i leczenie” https://www.mp.pl/pacjent/gastrologia/choroby/zoladek/134806,helicobacter-pylori (dostęp 17.04.2026 r.)
- Krystian Adrych, Bogdan Solnica, Elżbieta Rożynek, Gajane Martirosian „Diagnostyka zakażenia Helicobacter pylori” https://www.mp.pl/interna/chapter/B16.V.28.1.3. (dostęp 18.04.2026 r.)
- Prof. dr hab. med. Witold Bartnik „Leczenie zakażenia (eradykacja) Helicobacter pylori” https://www.mp.pl/pacjent/gastrologia/choroby/zoladek/80640,leczenie-zakazenia-eradykacja-helicobacter-pylori (dostęp 18.04.2026 r.)
- Waldemar Rastawicki, Klaudia Wiechetek-Płaza „SEROPREVALENCE OF HELICOBACTER PYLORI INFECTIONS IN CHILDREN AND ADULTS IN POLAND IN THE YEARS 2020-2023” PRZEGL EPIDEMIOL 2023;77(3): 317-326