Dla wielu pacjentów informacja o konieczności wyłonienia stomii wiąże się z dużym stresem, obawami o codzienne funkcjonowanie oraz jakość życia. W praktyce jednak jest to rozwiązanie, które często ratuje zdrowie, a nawet życie, a odpowiednia edukacja i wsparcie pozwalają pacjentom wrócić do normalnej aktywności zawodowej i społecznej. Sprawdź, co to jest stomia, na czym polega jej działanie, jak wygląda i kiedy jest konieczna.
| Z tego artykułu dowiesz się, że: >> stomia to chirurgicznie wytworzone połączenie układu lub narządu wewnętrznego z powierzchnią skóry. >> stomie dzieli się na odżywcze lub wydalnicze. >> główne rodzaje to: kolostomia (jelito grube), ileostomia (jelito cienkie) i urostomia (moczowa). >> wyłonienie stomii bywa konieczne w leczeniu nowotworów i innych poważnych schorzeń. >> stomia może być czasowa lub stała. |
Spis treści:
- Stomia: co to jest?
- Kiedy stomia jest konieczna: przyczyny wyłonienia stomii
- Jak często wyłania się stomię?
- Jak wygląda stomia?
- Czy stomia jest na zawsze?
- Jak żyć ze stomią?
- Najczęstsze pytania o stomię (FAQ)
Stomia: co to jest?
Stomia to celowo wytworzone połączenie pomiędzy światłem narządu wewnętrznego a powierzchnią ciała, umożliwia podawanie pokarmu do przewodu pokarmowego (stomie odżywcze) lub odprowadzanie treści fizjologicznych, najczęściej kału albo moczu (stomie wydalnicze), z pominięciem naturalnej drogi. Najczęściej dotyczy jelita grubego, jelita cienkiego i dróg moczowych. Stomie wydalnicze nie mają zwieracza, dlatego oddawanie treści jest niezależne od woli pacjenta i zwykle wymaga stosowania sprzętu stomijnego (worka).
Rodzaje stomii
Podstawowy podział stomii obejmuje rozróżnienie na stomie:
- odżywcze – umożliwiające podawanie pokarmu bezpośrednio do przewodu pokarmowego,
- wydalnicze – umożliwiające odprowadzanie treści fizjologicznych.
Do stomii odżywczych zaliczane są gastrostomia, czyli połączenie żołądka ze skórą, oraz jejunostomia – połączenie ze skórą jelita czczego. Natomiast rodzaje stomii wydalniczych to:
- ezofagostomia – wyprowadzenie przełyku na ścianę klatki piersiowej lub szyję w celu odprowadzania śliny i wydzielin górnego odcinka przewodu pokarmowego;
- kolostomia – wyprowadzenie światła jelita grubego. Stolec wydalany przez kolostomię jest zwykle uformowany lub półpłynny. Kolostomie są często wyłaniane po lewej stronie brzucha;
- ileostomia – wyprowadzenie światła jelita cienkiego. Wydzielina jest płynna, bogata w enzymy trawienne, które mogą silnie drażnić skórę, stąd wymaga szczególnie starannej pielęgnacji. Ileostomię wyłania się zwykle po prawej stronie brzucha;
- urostomia – wyprowadzenie dróg moczowych w celu odprowadzenia moczu z pominięciem poszczególnych elementów układu moczowego. Najczęstszym typem jest metoda Brickera, gdzie wykorzystuje się fragment jelita cienkiego, do którego implantuje się moczowody, a jego koniec wyprowadza na skórę.
Ponadto stomia wydalnicza może być czasowa (zakładana na krótki czas) lub stała (gdy nie ma możliwości przywrócenia naturalnej drogi wydalania).
| Warto wiedzieć: Urostomia może być wyłoniona na poziomie nerek, moczowodów, pęcherza moczowego, cewki moczowej. |
Kiedy stomia jest konieczna: przyczyny wyłonienia stomii
Do najczęstszych przyczyn wyłonienia stomii jelitowej należą m.in.:
- rak jelita grubego,
- niedrożność jelit,
- choroby zapalne jelit (np. choroba Leśniowskiego-Crohna, wrzodziejące zapalenie jelita grubego),
- perforacja jelita,
- wady wrodzone układu pokarmowego,
- urazy jamy brzusznej,
- powikłana choroba uchyłkowa jelita grubego,
- rozległa endometrioza jelita grubego,
- nieszczelność lub rozejście się zespolenia po operacji.
Wskazania do wyłonienia urostomii to m.in. rak pęcherza moczowego, nowotwór moczowodów, wady wrodzone dróg moczowych i pęcherza moczowego, pęcherz neurogenny, urazy nerek.
Jak często wyłania się stomię?
Według dostępnych danych w Polsce żyje ponad 35 tysięcy osób z wyłonioną stomią. Każdego roku wykonuje się nawet 7 tysięcy takich zabiegów. Największą grupę pacjentów stanowią osoby po operacjach onkologicznych jelita grubego.
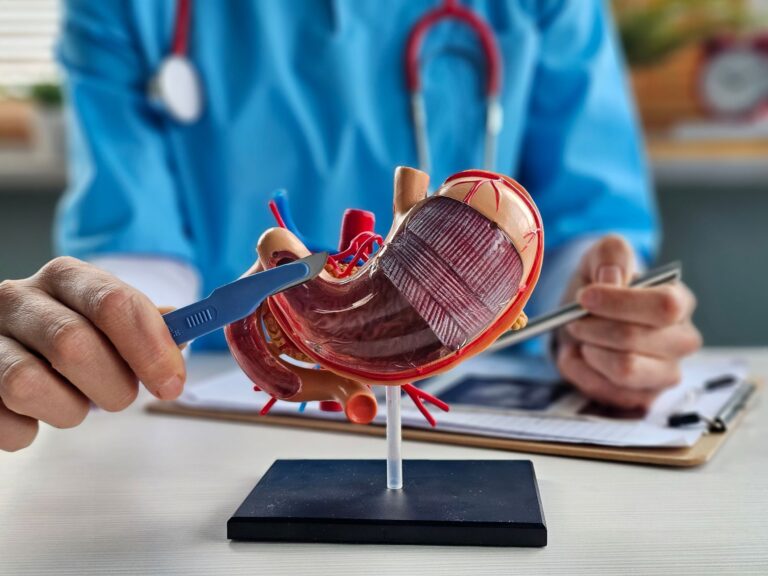
Jak wygląda stomia?
Zdrowa stomia ma kolor różowy lub czerwony (podobny do wewnętrznej strony policzka), jest wilgotna i nie jest unerwiona czuciowo (czyli jej dotykanie nie boli). Może nieznacznie wystawać ponad powierzchnię skóry lub być z nią zrównana. Jej kształt jest okrągły lub owalny.
Bezpośrednio po operacji stomia bywa obrzęknięta. Jednak z czasem jej rozmiar ulega zmniejszeniu.
Czy stomia jest na zawsze?
Stomia może mieć charakter czasowy lub stały. Stomia czasowa wyłaniana jest na krótki czas – np. w celu ochrony zespolenia jelitowego lub odbarczenia układu moczowego. Warunkiem jej wyłonienia jest istnienie możliwości przywrócenia fizjologicznej drogi wydalania. Stomia stała pozostaje na całe życie pacjenta i dotyczy sytuacji, w których nie ma możliwości odtworzenia ciągłości przewodu pokarmowego lub dróg moczowych.
Jak żyć ze stomią?
Życie ze stomią wymaga adaptacji, jednak przy odpowiednim wsparciu pacjenci mogą prowadzić aktywne i satysfakcjonujące życie. Istotne znaczenie mają: edukacja stomijna, nauka obsługi sprzętu oraz regularne kontrole medyczne. Osoby ze stomią mogą pracować, uprawiać sport, podróżować i utrzymywać życie towarzyskie.
Zasady dotyczące pielęgnacji skóry wokół stomii oraz używania sprzętu stomijnego są przekazywane pacjentowi i jego rodzinie przez pielęgniarkę jeszcze w szpitalu, po operacji.
Pielęgnacja skóry wokół stomii
Prawidłowa pielęgnacja skóry okołostomijnej zapobiega podrażnieniom i powikłaniom. Skóra wokół stomii powinna być czysta, sucha i odpowiednio chroniona przed kontaktem z treścią jelitową lub moczem.
Skóra wokół stomii powinna być oczyszczana podczas każdej zmiany sprzętu stomijnego. Należy umyć ją letnią wodą z delikatnym środkiem myjącym o neutralnym pH oraz dokładnie osuszyć (gazikiem, chusteczką, miękkim ręcznikiem). Nie powinno się używać preparatów zawierających alkohol oraz substancji natłuszczających. Dopuszczalne jest stosowanie dedykowanych preparatów ochronnych (np. past uszczelniających). Pacjent powinien regularnie obserwować skórę wokół stomii pod kątem nieprawidłowości.
Czego unikać przy stomii?
Pacjenci ze stomią powinni unikać działań, które mogą prowadzić do uszkodzenia skóry lub powikłań stomijnych m.in.:
- używania do pielęgnacji środków drażniących i natłuszczających,
- golenia skóry wokół stomii (np. maszynką „na gładko”); jeśli trzeba usunąć owłosienie, lepiej zrobić to delikatnie (trymerem/nożyczkami), by nie podrażnić skóry,
- pośpiechu podczas wymiany worka stomijnego,
- aktywności obciążających brzuch,
- stosowania nieprawidłowej diety mogącej prowadzić do biegunek i zaparć.
Wszelkie niepokojące zmiany wokół stomii należy niezwłocznie skonsultować z lekarzem lub pielęgniarką stomijną.
Najczęstsze pytania o stomię (FAQ)
Odpowiedzi na najczęściej zadawane pytania dotyczące stomii.
Stomia polega na chirurgicznym wyłonieniu fragmentu jelita lub dróg moczowych na powierzchnię skóry w celu odprowadzania treści fizjologicznych. Zastępuje czasowo lub trwale naturalną drogę wydalania.
Długość życia zależy od choroby podstawowej i skuteczności jej leczenia, a nie od samego posiadania stomii.
Przy stomii czasowej odbyt pozostaje zachowany, ale nie bierze udziału w wydalaniu. W przypadku stomii stałej odbyt może zostać chirurgicznie usunięty lub pozostaje nieczynny.
Sama stomia nie zawsze oznacza niepełnosprawność, jednak niektórych przypadkach może stanowić podstawę do orzeczenia, w zależności od stanu funkcjonalnego pacjenta. Decyzja podejmowana jest indywidualnie przez komisję orzekającą.
Należy unikać aktywności obciążających brzuch i spożywania ciężkostrawnych posiłków. Przy pielęgnacji niewskazane jest stosowanie środków drażniących i natłuszczających.
Do możliwych powikłań należą podrażnienia skóry, przepuklina okołostomijna czy zwężenie stomii.
Opieka merytoryczna: lek. Katarzyna Ciepłucha
Bibliografia
- https://www.mp.pl/pacjent/badania_zabiegi/132730,stomia (dostęp 09.02.2026)
- B. Dębowska, Aspekty opieki pielęgniarskiej nad pacjentem ze stomią, w tym zapobieganie powikłaniom, Skrypt dla uczestniczek/uczestników kursu dokształcającego
- T. Banasiewicz i in., Stomia prawidłowe postępowanie chirurgiczne i pielęgnacja, Wskazania do wyłonienia stomii Michał Drews, Tomasz Kościński Poznań 2014
- https://gastroenterologia-praktyczna.pl/a1614/Chorzy-ze-stomia.html/ (dostęp 09.02.2026)
- M. Ćwiek, K. Kowalczuk, Zmiany w funkcjonowaniu osób z wyłonioną stomią jelitową [w:] Jakość życia w naukach medycznych i społecznych t. I