Spis treści
- Jakie są wczesne objawy nowotworu jelita grubego?
- Jestem „za młody” na raka jelita grubego – czy aby na pewno?
- Czy warto zwlekać z diagnostyką?
- Czym grozi lekceważenie objawów nowotworu jelita grubego?
- Czy istnieje program badań przesiewowych raka jelita grubego?
- Nie jestem objęty/a programem – co mam zrobić?
Choroby nowotworowe można śmiało nazwać „epidemią współczesności”. Jednym z najczęstszych w polskiej populacji jest rak jelita grubego, a rozpoznanie – według danych Ministerstwa Zdrowia – każdego roku słyszy aż 18 tysięcy Polaków. Choroba jest bardzo podstępna, często rozwija się niepostrzeżenie przez wiele lat – w tym u osób młodych, o czym poniżej, stąd tak ważna jest znajomość wczesnych objawów, których obecność powinna skłaniać ku przeprowadzeniu diagnostyki.
Jakie są wczesne objawy nowotworu jelita grubego?
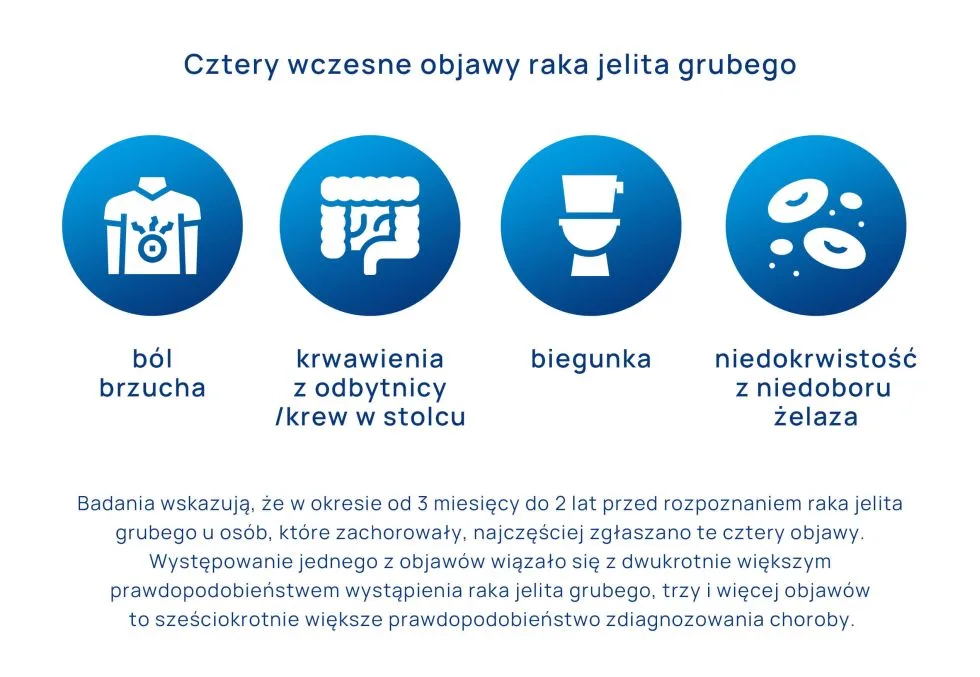
Jak wspomniano na wstępie, objawy mogą być przez długi czas nieobecne, a gdy występują jakiekolwiek, to często nie są wiązane z rakiem. Bardzo ważnych i jednocześnie niepokojących danych dostarczyli w lipcu br. amerykańscy naukowcy działający pod egidą National Cancer Institute, którzy dokonali analizy danych 113 milionów osób między 18. a 64. rokiem życia; w dalszym etapie prac zidentyfikowano osoby z co najmniej 2-letnim ciągłym zapisem danych medycznych, w ten sposób pozyskano materiał obejmujący informacje o 5075 osobach w wieku 18-49 lat ze zdiagnozowanym nowotworem jelita grubego i 22 378 osób nieobciążonych tą chorobą. W celu wiarygodnego porównania obie grupy dobrano pod względem wieku i innych czynników, takich jak płeć i miejsce zamieszkania. W kolejnym kroku sprawdzono, czy co najmniej jeden z kilkunastu znanych objawów raka jelita grubego występował częściej w grupie chorych na nowotwór w okresie od 3 miesięcy do 2 lat przed postawieniem diagnozy. W ten sposób odkryto, że cztery objawy – ból brzucha, krwawienie z odbytu, przewlekła biegunka i niedokrwistość z niedoboru żelaza – występowały istotnie częściej u osób, u których ostatecznie zdiagnozowano raka jelita grubego. Odkrytą zależność sprawdzono następnie w populacji w wieku 50-64 lat i zauważono, że występowały one tylko nieznacznie częściej w porównaniu do osób zdrowych.
Jestem „za młody” na raka jelita grubego – czy aby na pewno?
By w pełni uświadomić sobie powagę powyższych odkryć, warto przedstawić bardziej szczegółowe wyniki badania. Wykazano, że w omawianym okresie (3 miesiące do 2 lat) prawie 20% młodszych dorosłych chorych na nowotwór jelita grubego zgłaszało co najmniej jeden z czterech wymienionych objawów. Najczęstszym okazał się ból brzucha, który dotykał 11,6% osób. Nie ten objaw był jednak najbardziej specyficzny – według naukowców najsilniejsze powiązanie z rakiem wykazywało krwawienie z odbytu, a następnie niedokrwistość z niedoboru żelaza.
Czy warto zwlekać z diagnostyką?
Na to pytanie także uzyskano odpowiedź w postaci twardych danych naukowych, zbadano bowiem zależność czasową między pojawianiem się objawów a postawieniem rozpoznania. W ten sposób wykazano, że wśród osób z jednym objawem wynosił on około 10 miesięcy; pojawianie się każdego dodatkowego skracało ten czas, jednak nawet u osób z trzema lub czterema średnie opóźnienie wynosiło około 5 miesięcy. W tym miejscu nie można pominąć istotnego faktu – jak podają autorzy, nie dysponowali oni informacjami co do stadium choroby, w której została ona zdiagnozowana, co tym bardziej powinno skłaniać do czujności i niezwlekania z udaniem się na przeprowadzenie odpowiedniej diagnostyki.
Czym grozi lekceważenie objawów nowotworu jelita grubego?
Jak pokazuje literatura naukowa i praktyka kliniczna młodsi dorośli częściej ignorują wczesne objawy choroby; wiele przypadków zostaje zdiagnozowanych dopiero w zaawansowanym stadium, co w przypadku osób z rozsianym nowotworem jelita grubego oznacza, że tylko 14% z nich będzie żyło 5 lat lub dłużej. W przypadku wykrycia choroby na wczesnym etapie 5-letnie przeżycie wynosi aż 90%, a dodatkową korzyścią jest mniej obciążające leczenie.
Czy istnieje program badań przesiewowych raka jelita grubego?
Na szczęście Polska jest krajem realizującym taki program (Ministerstwo Zdrowia szacuje, że populacja wymagająca przebadania wynosi aż 8 milionów ludzi!). Polega on na przeprowadzeniu kolonoskopii z pobraniem i oceną wycinków jelita grubego, a także – gdy są obecne – usunięciu polipów wielkości do 15 mm. Kryteriami uprawniającymi do bezpłatnego skorzystania jest wiek między 50. a 69. rokiem życia lub między 40. a 49. rokiem życia w przypadku osób posiadających krewnych I stopnia z rozpoznaniem raka jelita grubego. Lista placówek realizujących jest dostępna pod linkiem.
Nie jestem objęty/a programem – co mam zrobić?
Jeżeli jesteś osobą w wieku 18-49 lat i zauważasz u siebie jeden lub więcej z wymienionych wcześniej objawów, to nie zwlekaj; udaj się do lekarza pierwszego kontaktu i powiedz o swoich dolegliwościach i obawach. Zapamiętaj, że według danych naukowych połowa nowotworów jelita grubego o wczesnym początku jest wykrywana u osób poniżej 45. roku życia, u których nie zaleca się rutynowych badań przesiewowych. Pamiętaj również, że po pierwsze sam proces diagnostyki nie jest równoznaczny z obecnością choroby, a po drugie postawienie rozpoznania daje ci szansę na podjęcie leczenia; tym skuteczniejszego i mniej obciążającego, im wcześniej zostanie rozpoczęte.
Piśmiennictwo