Mgła mózgowa to potoczne określenie na szereg dolegliwości związanych z funkcjami poznawczymi – od problemów z koncentracją po spowolnienie myślenia. W tym artykule znajdziesz wyjaśnienie, czym charakteryzuje się mgła mózgowa: co to za dolegliwość, jakie są jej przyczyny i jak leczyć mgłę mózgową, by wrócić do pełni sprawności.
| Z tego artykułu dowiesz się: >> czym jest mgła mózgowa i na czym polega brain fog, >> jakie są najczęstsze przyczyny mgły mózgowej, w tym: COVID-19, Hashimoto, niedoczynność tarczycy, depresja, zmiany hormonalne, >> jak objawia się mgła mózgowa, >> jakie badania wykonać przy jej występowaniu, >> jak radzić sobie z dolegliwościami na co dzień, a także poznasz odpowiedzi na najpopularniejsze pytania odnośnie mgły mózgowej. |
Spis treści:
- Mgła mózgowa – co to jest tzw. brain fog?
- Mgła mózgowa – przyczyny
- Jak objawia się mgła mózgowa?
- Mgła mózgowa – jakie badania wykonać?
- Mgła mózgowa – jak leczyć brain fog?
- Najczęstsze pytania o mgłę mózgową (FAQ)
Mgła mózgowa – co to jest tzw. brain fog?
„Mgła mózgowa” nie jest medycznym terminem diagnostycznym. Tą nazwą określa się zespół dolegliwości obejmujących zaburzenia funkcji poznawczych. Pod tym pojęciem kryją się trudności takie jak spowolnienie myślenia, problemy z koncentracją, gorsza pamięć, mniejsza wydajność intelektualna.
Na czym polega mgła mózgowa? Osoby dotknięte tą dolegliwością mają poczucie, że ich zdolności umysłowe (pamięć, koncentracja, szybkość myślenia) są obniżone, a umysł „zamglony” – stąd nazwa „mgła mózgowa”. Choć może być chwilowa, u części osób utrzymuje się tygodniami lub nawet miesiącami, znacząco utrudniając codzienne funkcjonowanie.

Mgła mózgowa – przyczyny
Przyczyny pojawienia się mgły mózgowej są bardzo zróżnicowane. U części osób opisuje się związek z procesami zapalnymi, stresem oksydacyjnym lub zaburzeniami regulacji neuroprzekaźników, jednak mechanizm nie zawsze jest jednoznaczny i zależy od przyczyny. W wielu przypadkach mgła mózgowa wynika z przeciążenia, braku snu czy przewlekłego stresu. Do częstych czynników sprzyjających zalicza się również zaburzenia hormonalne, infekcje, problemy psychiczne, działania niepożądane niektórych leków oraz niedobory (np. witaminy B12, żelaza, a także witaminy D).
Mgła mózgowa po COVID-19
Jedną z najczęściej wymienianych obecnie przyczyn mgły mózgowej jest przebycie infekcji COVID-19. Mgła mózgowa po COVID-19 może utrzymywać się przez wiele tygodni, a nawet miesięcy po infekcji. W takim wypadku mówimy o tzw. long COVID.
Warto przy tym wspomnieć, że mgła mózgowa może wystąpić także u osób, które przeszły zakażenie bezobjawowo. Wirus Sars-Cov-2 atakuje nie tylko układ oddechowy, ale również inne układy, w tym nerwowy. Zgodnie z najnowszą wiedzą medyczną, mgła mózgowa po COVID-19 jest wynikiem trwającego podczas zakażenia stanu zapalnego oraz nieprawidłowej reakcji układu odpornościowego, czyli tzw. burzy cytokinowej.
Oprócz przewlekłego zmęczenia po infekcji mogą pojawić się trudności z pamięcią, skupieniem oraz upośledzenie zdolności intelektualnych. Jeśli objawy utrzymują się przez dłuższy czas, warto rozważyć diagnostykę laboratoryjną oraz konsultację neurologiczną lub internistyczną.
Mgła mózgowa a Hashimoto i choroby tarczycy
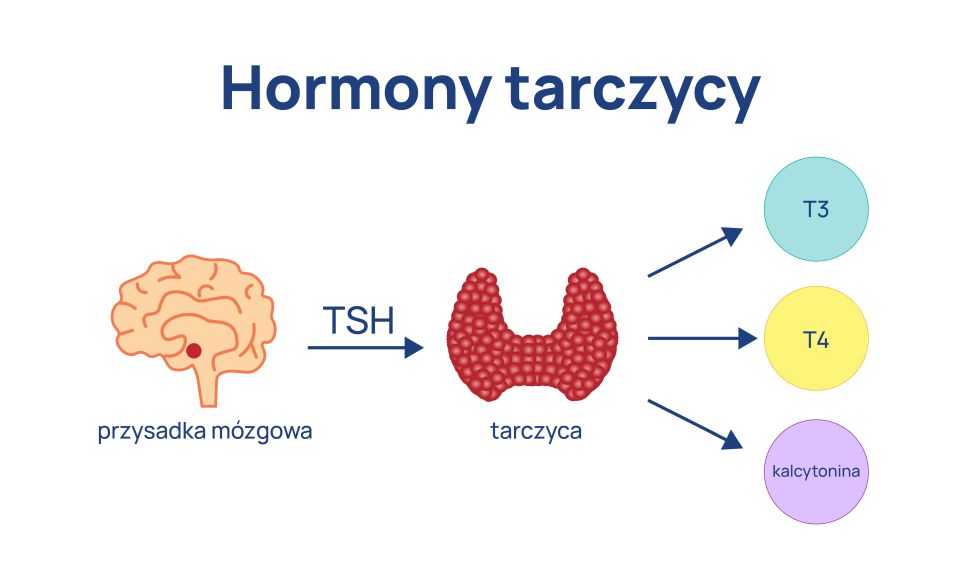
Jeśli chodzi o niedoczynność tarczycy i Hashimoto, mgła mózgowa może pojawić się w wyniku nieodpowiedniego poziomu hormonów w organizmie. Wahania hormonów tarczycowych przy zaburzeniach pracy tarczycy mogą wpływać na pamięć, koncentrację i tempo myślenia.
Uregulowanie poziomu TSH, FT3 i FT4 przynosi poprawę przy niedoczynności tarczycy. Mgła mózgowa może być ważnym objawem problemów z tarczycą i powodem, by w końcu zgłosić się do lekarza i przeprowadzić diagnostykę oraz leczenie.
>> Zobacz: Objawy niedoczynności tarczycy – maski Hashimoto
Mgła mózgowa przy depresji
Problemy z koncentracją i spowolnienie psychoruchowe są również typowymi objawami depresji. Mgła mózgowa to jeden z tych objawów, które pacjenci zauważają najwcześniej i skarżą się na „zamglenie umysłu”. W tym wypadku kluczowe jest leczenie przyczyny podstawowej za pomocą terapii, farmakoterapii lub ich połączenia, by złagodzić objawy poznawcze związane z depresją.

Jak objawia się mgła mózgowa?
Objawy mgły mózgowej są często bagatelizowane przez otoczenie i mogą być źródłem dużej frustracji. Obejmują przede wszystkim problemy z funkcjami poznawczymi, ale mogą towarzyszyć im także dolegliwości fizyczne. Oto najczęściej spotykane objawy, które mogą oznaczać mgłę mózgową:
- problemy z koncentracją: trudności w utrzymaniu uwagi na zadaniu lub w czasie rozmowy,
- osłabienie pamięci: zapominanie o terminach czy wykonywaniu codziennych czynności,
- trudności ze znalezieniem odpowiedniego słowa: problemy z szybkim nazwaniem przedmiotu czy wyrażeniem myśli,
- uczucie spowolnionego myślenia,
- uczucie dezorientacji lub zagubienia, szczególnie w nowych lub stresujących sytuacjach.
Masz wrażenie, że Twój mózg nie działa tak jak kiedyś i spowija go gęsta mgła? Jeśli powyższe objawy utrzymują się, najlepszym rozwiązaniem będzie konsultacja ze specjalistą.
Mgła mózgowa – jakie badania wykonać?
Zastanawiasz się, jakie badania na mgłę mózgową wykonać? Przede wszystkim musisz zdać sobie sprawę z tego, że mgła mózgowa jest objawem, a nie chorobą, więc kluczowe jest ustalenie jej pierwotnej przyczyny. Konieczna będzie zatem wizyta u lekarza i wykonanie odpowiednich badań laboratoryjnych. Co warto sprawdzić?
- Morfologia krwi, poziom ferrytyny i witaminy B12 – niedobory mogą prowadzić do anemii i problemów poznawczych
- Panet tarczycowy (FT-3, FT-4 i TSH) – w celu wykluczenia lub potwierdzenia niedoczynności tarczycy
- Poziom witaminy D – jej niedobór wiąże się z obniżonym nastrojem i funkcjami poznawczymi
- Markery stanu zapalnego (np. CRP) – aby ustalić, czy w organizmie nie toczy się przewlekły stan zapalny
- Glukoza na czczo i/lub HbA1c (ew. OGTT) – w kierunku zaburzeń gospodarki węglowodanowej; w wybranych sytuacjach lekarz może rozszerzyć diagnostykę.
- Test ciążowy – tzw. baby brain, czyli mgła mózgowa w ciąży, to drobne zaniki pamięci, zaburzenia koncentracji i ogólne roztargnienie. Takie objawy, oprócz porannych mdłości, mogą świadczyć o ciąży
- Badanie poziomu FSH, LH i estradiolu – u kobiet w okresie okołomenopauzalnym badania te wykonuje się w wybranych sytuacjach (np. przy nietypowych objawach, nieregularnych krwawieniach lub podejrzeniu przedwczesnej niewydolności jajników); w większości przypadków rozpoznanie menopauzy opiera się na wywiadzie i objawach. Mgła mózgowa w tym okresie jest dość częsta i bywa wiązana ze spadkiem stężenia estrogenów.
Mgła mózgowa – jak leczyć brain fog?
Leczenie mgły mózgowej polega przede wszystkim na usunięciu jej przyczyny. Mgła mózgowa po grypie wymaga głównie odpoczynku i regeneracji, natomiast w przypadku gdy problemem jest niedoczynność tarczycy, należy wdrożyć odpowiednie leczenie. Zdiagnozowane niedobory wymagają z kolei odpowiedniej suplementacji i diety. Niezależnie od przyczyny medycznej, możesz łagodzić objawy mgły mózgowej poprzez zadbanie o swój styl życia:
- Upewnij się, że śpisz 7-9 godzin na dobę: regeneracja organizmu jest kluczowa dla prawidłowej pracy mózgu.
- Zadbaj o swoją dietę: postaw na produkty bogate w kwasy omega-3 oraz warzywa i owoce – źródło antyoksydantów.
- Wprowadź regularną aktywność fizyczną: ruch poprawia krążenie krwi i wspiera prawidłową pracę mózgu.
- Ogranicz do minimum używki i nadmiar kofeiny.
>> Sprawdź: Medytacja – jak działa na stres? Czym jest medytacja, jak zacząć medytować?
Najczęstsze pytania o mgłę mózgową (FAQ)
Poniżej znajdziesz odpowiedzi na najczęściej zadawane pytania w związku z mgłą mózgową.
Tak, witamina B12 może pomóc w walce z mgłą mózgową, jeśli jest ona wynikiem niedoboru. Witamina B12 jest niezbędna do prawidłowego funkcjonowania układu nerwowego. Jeśli badanie potwierdzi jej zbyt niski poziom, lekarz może zlecić suplementację lub zastrzyki.
Często tak – zwłaszcza gdy uda się znaleźć i leczyć przyczynę (np. niedobór snu, niedokrwistość, zaburzenia tarczycy, depresję). Czas trwania jest jednak indywidualny; po COVID-19 objawy poznawcze mogą utrzymywać się dłużej i wymagają kontroli lekarskiej, jeśli istotnie utrudniają funkcjonowanie.
Nadmierne spożycie kofeiny może nasilać niepokój, zaburzać sen i prowadzić do tzw. „zjazdu” energetycznego, który może przypominać objawy mgły mózgowej.
Słabe krążenie oznacza mniejszą ilość tlenu i składników odżywczych dostarczanych do komórek nerwowych, co może powodować objawy mgły mózgowej. W tym wypadku zadbaj o zdrowie układu sercowo-naczyniowego oraz regularną aktywność fizyczną.
W chorobach autoimmunologicznych, takich jak toczeń, mogą występować objawy neurologiczne przypominające mgłę mózgową. W takiej sytuacji zwróć się po pomoc do specjalisty.
Mgła mózgowa to szereg dolegliwości obniżających jakość życia. Zazwyczaj ma konkretną przyczynę; jeśli zaobserwujesz u siebie wymienione wyżej objawy, nie czekaj i skonsultuj się z lekarzem, by wykonać niezbędne badania laboratoryjne. To pierwszy krok do odzyskania pełnej sprawności umysłowej!
Opieka merytoryczna: lek. Katarzyna Ciepłucha
Bibliografia
- Ocon, A. J. (2013). Caught in the thickness of brain fog: Exploring the cognitive symptoms of chronic fatigue syndrome. Frontiers in Physiology, 4, 63.
- Chasco, E. E., Dukes, K., Jones, D., Comellas, A. P., Hoffman, R. M., & Garg, A. (2022). Brain fog and fatigue following COVID-19 infection: An exploratory study of patient experiences of long COVID. International Journal of Environmental Research and Public Health, 19(23), 15499.
- Misiurewicz-Gabi, A. (2020). COVID-19 może prowadzić do poważnych uszkodzeń układu nerwowego. Kurier Medyczny.
- Szlufik, S. (2020). Rekomendacje Polskiego Towarzystwa Neurologicznego w związku z pandemią koronawirusa. Neurologia po Dyplomie.
- Problemy z koncentracją – z czego mogą wynikać i jak znaleźć przyczynę? https://www.alab.pl/centrum-wiedzy/problemy-z-koncentracja-z-czego-moga-wynikac-i-jak-znalezc-przyczyne/ (dostęp: 11.12.2025).
- Przybylak, M., Grabowski, J., & Bidzan, L. (2021). Wpływ zaburzeń sekrecji hormonów tarczycy na funkcje poznawcze. Psychiatria Polska, 55(2), 309–321.
- Talarowska, M., Florkowski, A., Orzechowska, A., Wysokiński, A., & Zboralski, K. (2008). Funkcjonowanie poznawcze chorych na cukrzycę typu 1 i 2. Diabetologia Praktyczna, 9(5).
- Orchard, E. R., Rutherford, H. J. V., Holmes, A. J., et al. (2023). Matrescence: Lifetime impact of motherhood on cognition and the brain. Trends in Cognitive Sciences, 27(3), 302–326.